
【题目】过氧化氢是重要的氧化剂、还原剂,它的水溶液又称为双氧水,常用作消毒、杀菌、漂白等。某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的含量,请填写下列空白:
(1)移取10.00mL密度为ρg/mL的过氧化氢溶液至250mL容量瓶中,加水稀释至刻度,摇匀。移取稀释后的过氧化氢溶液25.00mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样。
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式,请将相关物质的化学计量数及化学式填写在方框里。__________
![]() MnO4-+
MnO4-+![]() H2O2+
H2O2+![]() H+=
H+=![]() Mn2++
Mn2++![]() H2O+
H2O+![]()
![]()
(3)滴定时,将高锰酸钾标准溶液注入_____(填“酸式”或“碱式”)滴定管中。滴定到达终点的现象是________。
(4)复滴定三次,平均耗用cmol/LKMnO4标准溶液VmL,则原过氧化氢溶液中过氧化氢的质量分数为___________。
【答案】2、5、6、2、8、5O2↑ 酸式 溶液由无色变为浅紫色,30s内不褪色 ![]()
【解析】
(2)反应中Mn元素化合价从+7价降低到+2价,得到5个电子,双氧水中氧元素化合价从-1价升高到0价失去1个电子被氧化为氧气,根据电子得失守恒可知反应中转移10个电子,根据电荷守恒和原子守恒可知配平后的方程式为2MnO4-+5H2O2+6H+=2Mn2++8H2O+5O2↑;
(3)高锰酸钾具有强氧化性,滴定时,将高锰酸钾标准溶液注入酸式滴定管中;酸性高锰酸钾溶液显紫色,滴定到达终点的现象是溶液由无色变为浅紫色,30s内不褪色;
(4)复滴定三次,平均耗用c mol/L KMnO4标准溶液V mL,则根据方程式可知过氧化氢的物质的量2.5cV×10-3mol,则原过氧化氢溶液中过氧化氢的质量分数为![]() =
=![]() 。
。


科目:高中化学 来源: 题型:
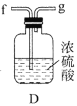
【题目】有一白色粉末X,对X检验时,所做实验和现象为:

(1)写出X的化学式___。
(2)在①步反应中H2SO4的作用是___。
①在水溶液中电离,并呈强酸性 ②具有高沸点、难挥发性 ③浓硫酸具有吸水性 ④浓硫酸具有脱水性 ⑤浓硫酸具有强氧化性
(3)写出④、⑤两步反应的离子方程式:___、___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钾(![]() )是一种新型、高效、多功能水处理剂,且不会造成二次污染。
)是一种新型、高效、多功能水处理剂,且不会造成二次污染。
查阅资料:
①![]() 为紫色固体,微溶于
为紫色固体,微溶于![]() 溶液,具有强氧化性,在酸性或中性溶液中快速产生
溶液,具有强氧化性,在酸性或中性溶液中快速产生![]() ,在碱性溶液中较稳定。
,在碱性溶液中较稳定。
②![]() 与
与![]() 溶液在20℃以下反应生成
溶液在20℃以下反应生成![]() ,在较高温度下则生成
,在较高温度下则生成![]() 。
。
(1)实验室常利用氯气制备![]() 后与
后与![]() 、
、![]() 反应制备
反应制备![]() 。根据下列仪器,请你组装合理、简洁的实验装置,所用装置的接口连接顺序是________。
。根据下列仪器,请你组装合理、简洁的实验装置,所用装置的接口连接顺序是________。





(2)写出装置A中发生反应的离子方程式________。
(3)三颈烧瓶用冰水浴的原因是________,A处盛放![]() 的仪器名称是________。
的仪器名称是________。
(4)将实验得到的![]() 再加入饱和
再加入饱和![]() 溶液中,可析出紫黑色的
溶液中,可析出紫黑色的![]() 粗晶体,其原因是________。
粗晶体,其原因是________。
(5)用滴定法测定所制粗![]() 的纯度(杂质与
的纯度(杂质与![]() 不反应):取
不反应):取![]() 粗
粗![]() 样品,加入足量硫酸酸化的
样品,加入足量硫酸酸化的![]() 溶液,充分反应后,用
溶液,充分反应后,用![]() 标准溶液滴定生成的I2,滴定消耗标准溶液的体积为
标准溶液滴定生成的I2,滴定消耗标准溶液的体积为![]() 。涉及的反应有:
。涉及的反应有:![]() ,
,![]() 。
。
①滴定时选用的指示剂是________,滴定终点的现象是________。
②制得粗![]() 的纯度是________。
的纯度是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请根据所学化学反应原理,解决以下问题:
(1)依据氧化还原反应:2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)设计的原电池,可以提供稳定的电流.装置如图所示,其中盐桥中装有琼脂-饱和KCl溶液。
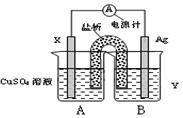
回答下列问题:
①电极X的材料和电解质溶液Y分别为________、________;
②盐桥中K+移向________(填A或B);
③银电极发生的电极反应式为________;
④该电池工作时,假设电路中有0.1mol电子转移,则X电极质量改变量为________克。
(2)已知:C(s)+O2(g)═CO2(g) △H1=-396.5kJmol-1;
H2(g)+![]() O2═H2O(g) △H2=-241.8kJmol-1;
O2═H2O(g) △H2=-241.8kJmol-1;
CO(g)+![]() O2(g)═CO2(g) △H3=-283.0kJmol-1.
O2(g)═CO2(g) △H3=-283.0kJmol-1.
根据盖斯定律写出单质碳和水蒸气生成水煤气的热化学方程式:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有下列化学仪器:①托盘天平;②玻璃棒;③药匙;④烧杯;⑤量筒;⑥容量瓶;⑦胶头滴管。
(1)现需要配制500 mL 1 mol/L硫酸溶液,需用质量分数为98%、密度为1.84 g/cm3的浓硫酸________mL。
(2)从上述仪器中,按实验使用的先后顺序,其编号排列是_______。
(3)容量瓶使用前检验漏水的方法是_______。
(4)若实验遇到下列情况,对硫酸溶液的物质的量浓度有何影响(填“偏高”、“偏低”或“不变”)
①未经冷却趁热将溶液注入容量瓶中,_______________;
②摇匀后发现液面低于刻度线再加水,_____________;
③容量瓶中原有少量蒸馏水,_______________;
④定容时观察液面俯视,_____________;
⑤未将洗涤液注入容量瓶中,_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】富硼渣中含有镁硼酸盐(2MgO·B2O3)、镁硅酸盐(2MgO·SiO2)及少量Al2O3、FeO 等杂质。由富硼渣湿法制备硫酸镁晶体和硼酸(H3BO3)晶体的一种工艺流程如下:
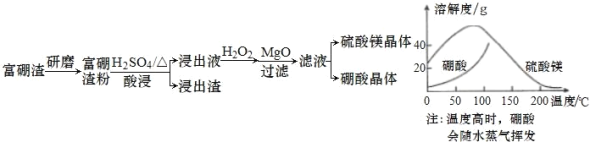
为了获得晶体,会先浓缩溶液接近饱和,然后将浓缩液放入高压釜中,控制温度进行结晶(硫酸镁与硼酸溶解度随温度的变化如图)。下列说法错误的是
A.该工艺流程中加快反应速率的措施有 2 种
B.在高压釜中,先降温结晶得到硼酸晶体,再蒸发结晶得到硫酸镁晶体
C.“酸浸”中镁硼酸盐发生反应2MgO·B2O3+2H2SO4+H2O![]() 2MgSO4+2H3BO3
2MgSO4+2H3BO3
D.加入“MgO”后过滤,所得滤渣主要是Al(OH)3 和Fe(OH)3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某可逆反应mA(g)+nB(g) ![]() pC(g)在密闭容器中进行,如图表示在不同反应时间t时,温度T和压强p与反应物B在混合气体中的体积分数B%的关系曲线,由曲线分析,下列判断正确的是
pC(g)在密闭容器中进行,如图表示在不同反应时间t时,温度T和压强p与反应物B在混合气体中的体积分数B%的关系曲线,由曲线分析,下列判断正确的是

A.T1<T2 p1<p2 m+n>p放热反应
B.T1>T2 p1<p2 m+n<p吸热反应
C.T1<T2 p1>p2 m+n>p放热反应
D.T1>T2 p1<p2 m+n>p吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三硫化磷(P4S3)是黄绿色针状晶体,易燃、有毒,分子结构之一如图所示,已知其燃烧时P被氧化为P4010,下列有关P4S3的说法中不正确的是

A. P4S3中磷元素为+3价
B. P4S3属于共价化合物
C. P4S3充分燃烧的化学方程式为P4S3+8O2=P4O10+3SO2
D. 1mol P4S3分子中含有9mol共价键
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com