
ЎѕМвДїЎїУРПВБР»ЇС§ТЗЖчЈєўЩНРЕММмЖЅЈ»ўЪІЈБ§°фЈ»ўЫТ©іЧЈ»ўЬЙХ±Ј»ўЭБїНІЈ»ўЮИЭБїЖїЈ»ўЯЅєН·µО№ЬЎЈ
(1)ПЦРиТЄЕдЦЖ500 mL 1 mol/LБтЛбИЬТєЈ¬РиУГЦКБї·ЦКэОЄ98%ЎўГЬ¶ИОЄ1.84 g/cm3µДЕЁБтЛб________mLЎЈ
(2)ґУЙПКцТЗЖчЦРЈ¬°ґКµСйК№УГµДПИєуЛіРтЈ¬Жд±аєЕЕЕБРКЗ_______ЎЈ
(3)ИЭБїЖїК№УГЗ°јмСйВ©Л®µД·Ѕ·ЁКЗ_______ЎЈ
(4)ИфКµСйУцµЅПВБРЗйїцЈ¬¶ФБтЛбИЬТєµДОпЦКµДБїЕЁ¶ИУРєОУ°Пм(МоЎ°Ж«ёЯЎ±ЎўЎ°Ж«µНЎ±»тЎ°І»±дЎ±)
ўЩОґѕАдИґіГИИЅ«ИЬТєЧўИлИЭБїЖїЦРЈ¬_______________Ј»
ўЪТЎФИєу·ўПЦТєГжµНУЪїМ¶ИПЯФЩјУЛ®Ј¬_____________Ј»
ўЫИЭБїЖїЦРФУРЙЩБїХфБуЛ®Ј¬_______________Ј»
ўЬ¶ЁИЭК±№ЫІмТєГжё©КУЈ¬_____________Ј»
ўЭОґЅ«ПґµУТєЧўИлИЭБїЖїЦРЈ¬_______________ЎЈ
Ўѕґр°ёЎї27.2 ўЭўЯўЬўЪўЮўЯўаўб НщИЭБїЖїДЪјУККБїЛ®Ј¬ИыєГЖїИыЈ¬УГКіЦё¶ҐЧЎЖїИыЈ¬УГБнТ»Ц»КЦµДОеЦёНРЧЎЖїµЧЈ¬°СЖїµ№Бў№эАґЈ¬ИзІ»В©Л®Ј¬°СЖїХэБў№эАґЈ¬Ѕ«ЖїИыРэЧЄ180ЎгєуИыЅфЈ¬ФЩ°СЖїµ№Бў№эАґЈ¬ИфІ»В©Л®Ј¬ІЕДЬК№УГ Ж«ёЯ Ж«µН І»±д Ж«ёЯ Ж«µН
ЎѕЅвОцЎї
(1)ТАѕЭc=![]() јЖЛгЕЁБтЛбµДОпЦКµДБїЕЁ¶ИЈ¬ёщѕЭИЬТєПЎКНЗ°єуИЬЦКµДОпЦКµДБїІ»±дАґБРКЅЅвґрЈ»
јЖЛгЕЁБтЛбµДОпЦКµДБїЕЁ¶ИЈ¬ёщѕЭИЬТєПЎКНЗ°єуИЬЦКµДОпЦКµДБїІ»±дАґБРКЅЅвґрЈ»
(2)ёщѕЭЕдЦЖТ»¶ЁОпЦКµДБїЕЁ¶ИИЬТєµДКµСйІЩЧчµДІЅЦиСЎФсТЗЖчЈ»
(3)ёщѕЭИЭБїЖїµД№№Фмј°ХэИ·К№УГ·Ѕ·ЁЅшРР·ЦОцЈ»
(4)·ЦОцІ»µ±ІЩЧч¶ФИЬЦКµДОпЦКµДБїєНИЬТєµДМе»эµДУ°ПмЈ¬ТАѕЭc=![]() ЅшРРОуІо·ЦОцЎЈ
ЅшРРОуІо·ЦОцЎЈ
(1)ЕЁБтЛбµДЕЁ¶Иc=![]() =
=![]() =18.4mol/LЈ¬ЕЁБтЛбПЎКНЗ°єуИЬЦКµДОпЦКµДБїІ»±дЈ¬ЙиЕЁБтЛбµДМе»эОЄVЈ¬ЛщТФ18.4mol/LЎБV=1mol/LЎБ0.5LЈ¬V=0.0136L=27.2mLЈ»
=18.4mol/LЈ¬ЕЁБтЛбПЎКНЗ°єуИЬЦКµДОпЦКµДБїІ»±дЈ¬ЙиЕЁБтЛбµДМе»эОЄVЈ¬ЛщТФ18.4mol/LЎБV=1mol/LЎБ0.5LЈ¬V=0.0136L=27.2mLЈ»
(2)ЕдЦЖ500ml1mol/LH2SO4ИЬТєІЅЦиОЄЈєјЖЛгЎўБїИЎЎўПЎКНЎўАдИґЎўТЖТєЎў¶ЁИЭЎўТЎФИЎўЧ°ЖїЎўМщЗ©Ј¬ТтґЛК№УГТЗЖчµДЛіРтОЄЈєўЭўЯўЬўЪўЮўЯўаўбЈ»
(3)јмІйИЭБїЖїКЗ·сВ©Л®µД·Ѕ·ЁОЄЈєНщИЭБїЖїДЪјУККБїЛ®Ј¬ИыєГЖїИыЈ¬УГКіЦё¶ҐЧЎЖїИыЈ¬УГБнТ»Ц»КЦµДОеЦёНРЧЎЖїµЧЈ¬°СЖїµ№Бў№эАґЈ¬ИзІ»В©Л®Ј¬°СЖїХэБў№эАґЈ¬Ѕ«ЖїИыРэЧЄ180ЎгєуИыЅфЈ¬ФЩ°СЖїµ№Бў№эАґЈ¬ИфІ»В©Л®Ј¬ІЕДЬК№УГЈ»
(4)ўЩОґѕАдИґЅ«ИЬТєЧўИлИЭБїЖїЦРЈ¬¶ЁИЭАдИґєуЈ¬ИЬТєµДМе»эЖ«РЎЈ¬ИЬТєµДЕЁ¶ИЖ«ёЯЈ»
ўЪТЎФИєу·ўПЦТєГжµНУЪїМ¶ИПЯФЩјУЛ®Ј¬ИЬТєµДМе»эЖ«ґуЈ¬ФтИЬТєЕЁ¶ИЖ«µНЈ»
ўЫИЭБїЖїЦРФУРЙЩБїХфБуЛ®Ј¬І»ёД±дИЬТєµДМе»эєНИЬЦКµДБїЈ¬ФтИЬТєЕЁ¶ИІ»±дЈ»
ўЬ¶ЁИЭК±№ЫІмТєГжё©КУЈ¬ИЬТєµДМе»эЖ«РЎЈ¬ФтИЬТєЕЁ¶ИЖ«ёЯЈ»
ўЭОґЅ«ПґµУТєЧўИлИЭБїЖїЦРЈ¬ИЭБїЖїИЬЦКЖ«µНЈ¬ФтИЬТєЕЁ¶ИЖ«µНЎЈ


 ±ёХЅЦРїјє®јЩПµБРґр°ё
±ёХЅЦРїјє®јЩПµБРґр°ё
| Дкј¶ | ёЯЦРїОіМ | Дкј¶ | іхЦРїОіМ |
| ёЯТ» | ёЯТ»Гв·СїОіМНЖјцЈЎ | іхТ» | іхТ»Гв·СїОіМНЖјцЈЎ |
| ёЯ¶ю | ёЯ¶юГв·СїОіМНЖјцЈЎ | іх¶ю | іх¶юГв·СїОіМНЖјцЈЎ |
| ёЯИэ | ёЯИэГв·СїОіМНЖјцЈЎ | іхИэ | іхИэГв·СїОіМНЖјцЈЎ |
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎї(I)ТСЦЄФЪ448 ЎжК±Ј¬·ґУ¦H2(g)Ј«I2(g)![]() 2HI(g)µДЖЅєвіЈКэK1ОЄ49Ј¬ФтёГОВ¶ИПВ·ґУ¦2HI(g)
2HI(g)µДЖЅєвіЈКэK1ОЄ49Ј¬ФтёГОВ¶ИПВ·ґУ¦2HI(g)![]() H2(g)Ј«I2(g)µДЖЅєвіЈКэK2ОЄ______Ј»·ґУ¦
H2(g)Ј«I2(g)µДЖЅєвіЈКэK2ОЄ______Ј»·ґУ¦![]() H2(g)+
H2(g)+![]() I2(g)
I2(g)![]() HI(g)µДЖЅєвіЈКэK3ОЄ________ЎЈ
HI(g)µДЖЅєвіЈКэK3ОЄ________ЎЈ
(II)ФЪТ»¶ЁМе»эµДГЬ±ХИЭЖчЦРЅшРР»ЇС§·ґУ¦ЈєCO2(g)Ј«H2(g)![]() CO(g)Ј«H2O(g)Ј¬Жд»ЇС§ЖЅєвіЈКэєНОВ¶ИµД№ШПµИзПВ±нЛщКѕЈє
CO(g)Ј«H2O(g)Ј¬Жд»ЇС§ЖЅєвіЈКэєНОВ¶ИµД№ШПµИзПВ±нЛщКѕЈє
t/Ўж | 700 | 800 | 830 | 1 000 | 1 200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
»ШґрПВБРОКМвЈє
(1)ёГ·ґУ¦µД»ЇС§ЖЅєвіЈКэ±нґпКЅОЄK=_____ЎЈ
(2)ёГ·ґУ¦ОЄ_____(МоЎ°ОьИИЎ±»тЎ°·ЕИИЎ±)·ґУ¦ЎЈ
(3)ДіОВ¶ИПВЈ¬ЖЅєвЕЁ¶И·ыєППВКЅЈєc(CO2)Ў¤c(H2)=c(CO)Ў¤c(H2O)Ј¬КФЕР¶ПґЛК±µДОВ¶ИОЄ_____ЎжЎЈ
(4)ФЪ800ЎжК±Ј¬·ўЙъЙПКц·ґУ¦Ј¬ДіТ»К±їМІвµГИЭЖчДЪёчОпЦКµДЕЁ¶И·Ц±рОЄc(CO2)=2molЎ¤L1Ј¬c(H2)=1.5molЎ¤L1Ј¬c(CO)=1molЎ¤L1Ј¬c(H2O)=3molЎ¤L1Ј¬ФтПВТ»К±їМЈ¬·ґУ¦Пт_____(МоЎ°ХэПтЎ±»тЎ°ДжПтЎ±)ЅшРРЎЈ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїЙиNAОЄ°ў·ьјУµВВЮіЈКэµДЦµЈ¬ПВБРЛµ·ЁХэИ·µДКЗ
A.17g-OHЦРє¬УРµДµзЧУКэОЄ10NA
B.25ЎгCК±Ј¬Ksp(BaSO4)=1ЎБ10-10Ј¬ФтBaSO4±ҐєНИЬТєЦРBa2+КэДїОЄ1ЎБ10-5NA
C.1L1molL-1CH3COONH4ИЬТєЦРCH3COO-УлNH4+КэДїѕщОЄNA
D.є¬0.5molѕ§°ы(ПВНј)µДCu2Oѕ§МеЦРCu2+µДКэДїОЄ2NA

Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎї±»іЖОЄЎ°№ъ·АЅрКфЎ±µДГѕ ,60%АґЧФєЈС󣬴ӺЈЛ®ЦРМбИЎГѕµДХэИ··Ѕ·ЁКЗ(ЎЎЎЎ)
A. єЈЛ®![]() Mg(OH)2
Mg(OH)2![]() Mg
Mg
B. єЈЛ®![]() MgCl2ИЬТєЁDЎъMgCl2(ИЫИЪ)
MgCl2ИЬТєЁDЎъMgCl2(ИЫИЪ)![]() Mg
Mg
C. єЈЛ®![]() Mg(OH)2
Mg(OH)2![]() MgO
MgO![]() Mg
Mg
D. єЈЛ®![]() Mg(OH)2
Mg(OH)2![]() MgCl2ИЬТєЁDЎъMgCl2(ИЫИЪ)
MgCl2ИЬТєЁDЎъMgCl2(ИЫИЪ)![]() Mg
Mg
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїДіИЬТєЦРє¬УРBa2+Ј¬Cu2+,Ag+Ј¬ПЦУГNaOHИЬТєЎўСОЛбєНNa2SO4ИЬТєЅ«ХвИэЦЦАлЧУЦрТ»іБµн·ЦАлЎЈЖдБчіМНјИзУТ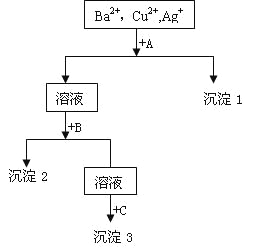
ЈЁ1Ј©іБµнµД»ЇС§КЅЈєіБµн1___________Ј¬іБµн2__________Ј¬іБµн3____________Ј»
ЈЁ2Ј©Рґіц»мєПТє+AµДАлЧУ·ЅіМКЅ________________________________________Ј»
ИЬТє+BµДАлЧУ·ЅіМКЅ_____________________________________ЎЈ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїУГЛ«ПЯЗЕ·ЦОцПВБРСх»Ї»№Ф·ґУ¦Ј¬Іў°ґТЄЗуМоїХЎЈ2AlЈ«3H2SO4 =Al2(SO4)3Ј«3H2Ўь_______
(1)Сх»ЇјБЈє________Ј¬Сх»ЇІъОпЈє________Ј»
(2)±кЧјЧґїцПВЈ¬ЙъіЙ3.36L H2Ј¬ІОјУ·ґУ¦µДAlµДЦКБїКЗ_______Ј¬ЧЄТЖµДµзЧУµДОпЦКµДБїОЄ_____Ј¬ИфИЬТєЦРH2SO4µДОпЦКµДБїЕЁ¶ИОЄ1.5 mol/LЈ¬ФтЗЎєГНкИ«·ґУ¦РијУИлµДH2SO4ИЬТєµДМе»э_____________ЎЈ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїДЖЎўВБєНМъКЗИэЦЦЦШТЄµДЅрКфЎЈЗл»ШґрЈє
(1)µ±З°Ј¬ІъБїЧоёЯЈ¬УГНѕЧо№гµДЅрКфКЗ_____________ЎЈ
(2)ХвИэЦЦЅрКфµДЅрКф»о¶ЇРФУЙЗїµЅИхµДЛіРтКЗ_______________ ЎЈ
(3)БтЛбМъУРѕ»Л®µДЧчУГЎЈРґіцБтЛбМъµДµзАл·ЅіМКЅЈє_____________ ЎЈ
(4)РЎїйЅрКфДЖН¶ИлЛ®ЦРЈ¬·ўЙъ·ґУ¦µД»ЇС§·ЅіМКЅОЄ_____________Ј»їЙ№ЫІмµЅµДКµСйПЦПуКЗ_____(МоЧЦДё)ЎЈ
a.ДЖіБµЅЛ®µЧ b.ДЖИЫіЙРЎЗт c.РЎЗтЛДґ¦УО¶Їd.Л®±дємЙ«
(5)ЧгБїµДВБУлЗвСх»ЇДЖИЬТє·ґУ¦єуµГµЅ±кЧјЧґїцПВµДЗвЖш2.24LЈ¬ФтІОјУ·ґУ¦µДВБµДЦКБїОЄ_____ ЎЈ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїТ»¶ЁОВ¶ИПВЈ¬ФЪИэёцМе»эѕщОЄ 1.0LµДєгИЭГЬ±ХИЭЖчЦР·ўЙъ·ґУ¦Јє2CH3OH(g) CH3OCH3(g) + H2O(g) ПВБРЛµ·ЁХэИ·µДКЗЈЁ Ј©
ИЭЖч ±аєЕ | ОВ¶И(Ўж) | ЖрКјОпЦКµДБї(mol) | ЖЅєвОпЦКµДБї(mol) | |
CH3OH(g) | CH3OCH3(g) | H2O(g) | ||
I | 387 | 0.20 | 0.080 | 0.080 |
II | 387 | 0.40 | ||
III | 207 | 0.20 | 0.090 | 0.090 |
A. ёГ·ґУ¦µДХэ·ґУ¦ОЄОьИИ·ґУ¦
B. ґпµЅЖЅєвК±Ј¬ИЭЖчIЦРµДCH3OHМе»э·ЦКэ±ИИЭЖчIIЦРµДРЎ
C. ИЭЖчIЦР·ґУ¦µЅґпЖЅєвЛщРиК±јд±ИИЭЖчIIIµДі¤
D. ИфЖрКјК±ПтИЭЖчIЦРідИл0.15mol µДCH3OHЎў0.15mol µДCH3OCH3єН0.10mol µДH2OЈ¬Фт·ґУ¦Ѕ«ПтХэ·ґУ¦·ЅПтЅшРР
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїУРИзНјЛщКѕAЎ«FБщЦЦТЗЖчЈє
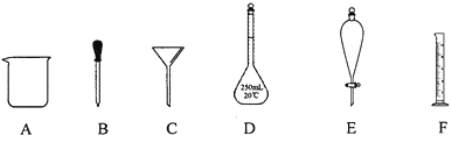
ЈЁ1Ј©CКЗ___ЈЁУГТЗЖчГыіЖМоїХЈ¬ПВН¬Ј©Ј¬DКЗ___Ј¬ДЬУГѕЖѕ«µЖјУИИµДКЗ___ЎЈ
ЈЁ2Ј©ПВБРКµСйІЩЧчЦРУГµЅТЗЖчEµДКЗ___ЈЁСЎМоПВБРСЎПоµД±аєЕЧЦДёЈ©ЎЈ
aЈ®·ЦАлЛ®єНCC14µД»мєПОп bЈ®·ЦАлЛ®єНѕЖѕ«µД»мєПОп cЈ®·ЦАлЛ®єНДаЙ°µД»мєПОп
ЈЁ3Ј©КµСйКТЕдЦЖТ»¶ЁОпЦКµДБїЕЁ¶ИµДСОЛбЈ¬РиУГГЬ¶ИОЄ1.25g mL-1Ўў 37%µДЕЁСОЛб4.5mLЎЈ
ўЩИЎУГ4.5mLСОЛбК±Ј¬РиТЄУГµЅЙПКцТЗЖчЦРµДFєН___ЈЁСЎМоТЗЖчµД±аєЕЧЦДёЈ©ЎЈ
ўЪИЎУГ4.5mLСОЛбЈ¬АыУГDЈЁ250mLЈ©µИТЗЖчЕдЦЖТ»¶ЁОпЦКµДБїЕЁ¶ИµДСОЛбЈ¬ХэИ·ІЩЧчЕдµГµДСОЛбОпЦКµДБїЕЁ¶ИОЄ___mol/LЈЁ±ЈБф2О»УРР§КэЧЦЈ©ЎЈ
ўЫПВБРЗйїцЦРЈ¬»бК№ЛщЕдИЬТєЕЁ¶ИЖ«ёЯµДКЗ___ЈЁМоРтєЕЈ©ЎЈ
AЈ®БїИЎЛщРиСОЛб№ЫІмТєГжК±СцКУ BЈ®ИЭБїЖїДЪУРЙЩБїХфБуЛ®
CЈ®јУХфБуЛ®К±Ј¬І»Йчі¬№эБЛїМ¶ИПЯ DЈ®¶ЁИЭК±СцКУїМ¶И
Ійїґґр°ёєНЅвОц>>
№ъјКѧУУЕСЎ - Б·П°ІбБР±н - КФМвБР±н
єю±±КЎ»ҐБЄНшОҐ·ЁєНІ»БјРЕПўѕЩ±ЁЖЅМЁ | НшЙПУРє¦РЕПўѕЩ±ЁЧЁЗш | µзРЕХ©ЖѕЩ±ЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРє¦РЕПўѕЩ±ЁЧЁЗш | ЙжЖуЗЦИЁѕЩ±ЁЧЁЗш
ОҐ·ЁєНІ»БјРЕПўѕЩ±Ёµз»°Јє027-86699610 ѕЩ±ЁУКПдЈє58377363@163.com