
【题目】某化学实验室以一种工业上的废渣(废渣主要含有MgCO3、MgSiO3和少量Fe、Al的氧化物)为原料,制备MgCO3·3H2O。实验流程如下图所示:

(1)为了加快废渣的酸溶速率,可采取的办法有_________(任写一点),酸溶时废渣中主要成分发生反应的离子方程式为___________________________________。
(2)加入30%H2O2的目的是__________________________________。
(3)用萃取分液的方法除去溶液中的Fe3+, 萃取分液完成后,检验水相中是否含有Fe3+的最佳试剂是_______。
(4)室温下,除去MgSO4溶液中的A13+(使Al3+浓度小于1×10-6mol/L)而不引入其它杂质,应加入的试剂X为_____________________。
(5)右图为不同反应温度下所得水合碳酸镁的X射线衍射谱图。由图可知,干燥时需控制温度范围为_______,温度较高时MgCO3·3H2O发生转化的化学方程式为_______________________________。

【答案】升高温度、搅拌、提高硫酸浓度等MgCO3+2H+=Mg2++H2O+CO2↑ MgSiO3+2H+=Mg2++H2SiO3将Fe2+氧化为Fe3+ ,便于除去KSCN溶液MgO、Mg(OH)2、MgCO3或Mg2(OH)2 CO3293K~313K(313K以下也可)MgCO3·3H2O =Mg5 (OH)2 (CO3)4·4H2O+CO2↑+10H2O
【解析】
(1)为了加快废渣的酸溶速率,可采取的办法有升高温度、搅拌、提高硫酸浓度等,酸溶时废渣中主要成分是碳酸镁和硅酸镁,发生反应的离子方程式为MgCO3+2H+=Mg2++H2O+CO2↑、 MgSiO3+2H+=Mg2++H2SiO3 ;(2)溶液中含有亚铁离子,双氧水具有强氧化性,能把亚铁离子氧化为铁离子,便于除去;(3)①检验溶液中是否含有Fe2+的最佳试剂是K3[Fe(CN)6]溶液;②萃取分液完成后,检验水相中是否含有Fe的最佳试剂是KSCN溶液;(4)室温下,除去MgSO4溶液中的A13+(使Al3+浓度小于1×10-6mol/L)而不引入其它杂质,应加入的试剂X为MgO、Mg(OH)2、MgCO3或Mg2(OH)2CO3。根据氢氧化铝的溶度积常数可知当铝离子浓度是1×10-6mol/L时,氢氧根的浓度是 ,又因为pH=8.5时,Mg(OH)2开始沉淀,所以应调节pH的范围为5.0<pH<8.5;(5)根据图像可知超过313K时碳酸镁晶体会发生化学变化,所以干燥时需控制温度范围为293K~313K,温度较高时MgCO3·3H2O发生转化生成Mg5(OH)2(CO3)4·4H2O,反应的化学方程式为5MgCO3·3H2O
,又因为pH=8.5时,Mg(OH)2开始沉淀,所以应调节pH的范围为5.0<pH<8.5;(5)根据图像可知超过313K时碳酸镁晶体会发生化学变化,所以干燥时需控制温度范围为293K~313K,温度较高时MgCO3·3H2O发生转化生成Mg5(OH)2(CO3)4·4H2O,反应的化学方程式为5MgCO3·3H2O![]() Mg5(OH)2(CO3)4·4H2O+CO2↑+10H2O。
Mg5(OH)2(CO3)4·4H2O+CO2↑+10H2O。


科目:高中化学 来源: 题型:
【题目】某兴趣小组模拟工业制漂白粉,设计了下列图5的实验装置。已知:①氯气和碱反应放出热量。②6Cl2+6Ca(OH)2![]() 5CaCl2+Ca(ClO3)2+6H2O。
5CaCl2+Ca(ClO3)2+6H2O。
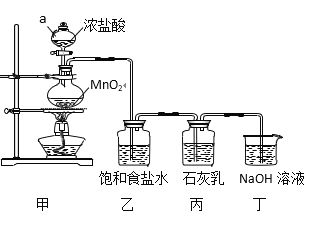
回答下列问题:
(1)甲装置中仪器a的名称是_______,MnO2在反应中所起的作用是(填“氧化剂”或“还原剂”)______________。
(2)装置乙中饱和食盐水的作用是____________________________。
(3)①制取漂白粉的化学方程式是____________________________。
②该小组制得的漂白粉中n(CaCl2) 远大于n[Ca(ClO)2],其主要原因是_________。
③为提高Ca(ClO)2的含量,可采取的措施是_______________(任写一种即可)。
(4)漂白粉应密封保存,原因是______________________(用化学方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分子式为C5H10O2的有机物为具有水果香味的油状液体,它与过量的NaOH溶液共热后蒸馏,若得到的有机物蒸气与氢气的摩尔质量之比为23,则有机物C5H10O2的结构简式可以是( )
A. HCOOCH2CH(CH3)2B. CH3CH2COOCH2CH3
C. CH3COOCH2CH2CH3D. CH3COOCH(CH3)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图表示细胞中四种有机化合物的组成及主要功能。回答下列问题:
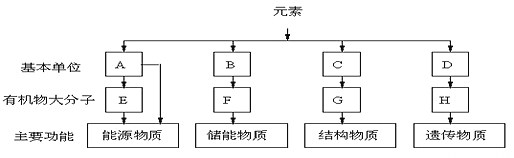
(1)图中的基本单位A是_________。利用A合成的E主要分布在人和动物的_________中,当人和动物血液中的A低于正常含量时,一些细胞中的E便分解产生A及时补充。
(2)与图中的E相比,F是细胞内更良好的储能物质,原因是____________。分布在内脏器官周围的F还具有_________的作用,可以保护内脏器官。
(3)图中的C在生物体中约有20种,其中有一部分在人体细胞不能合成,必须从外界环境中直接获取,这部分C叫做_________。由C形成G时,C分子之间通过_________(用化学结构简式表示)连接。
(4)图中H的中文名称是_________,烟草叶肉细胞的H彻底水解的产物是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】缩醛在有机合成中常用于保护羰基或作为合成中间体,同时还是一类重要的香料,广泛应用于化妆品、食物、饮料等行业。G是一种常用的缩醛,分子中含有一个六元环和一个五元环结构。下面是G的一种合成路线:
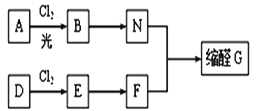
已知:①芳香烃A含氢元素的质量分数为8.7%,A的质谱图中,分子离子峰对应的最大质荷比为92; D的产重可以用来衡量一个国家的石油化工发展水平。
②同一个碳原子连接两个羟基不稳定,易脱水形成羰基。
③
回答下列问题:
(1)A的结构简式是_____________________,E的名称是____________________________。
(2)由D生成E的反应类型是________,E→F的反应条件是_________________________。
(3)由B生成N的化学方程式为___________________________。
(4)有研究发现,维生素C可以作为合成G物质的催化剂,具有价廉、效率高、污染物少的优点。维生素C的结构如右图。则维生素C分子中含氧官能团名称为_____________。

(5)缩醛G的结构简式为______________。G有多种同分异构体,写出其中能同时满足以下条件的所有同分异构体的结构简式:_________________________。
①既能发生银镜反应,又能与FeC13发生显色反应;②核磁共振氢谐为4组峰。
(6)写出用2-丁烯为原料(其他无机试剂任选)制备顺丁橡胶(顺式聚1,3-丁二烯)的合成路线:__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的数值。下列说法正确的是
A. 标准状况下,11.2L苯中含有分子的数目为0.5NA
B. 常温常压下,1.6g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1NA
C. 在过氧化钠与水的反应中,每生成0.1mol氧气,转移电子数目为0.4NA
D. 25℃时,pH=13的氢氧化钠溶液中含有OH-的数目为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于油脂的叙述正确的是 ( )
A.油脂有固定的熔、沸点
B.油脂是高级脂肪酸的甘油酯
C.油脂都不能使溴的四氯化碳溶液褪色
D.油脂分成油和脂肪,油的熔点高于脂肪
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.物质的量是物质所含微粒的数量B.阿伏加德罗常数是人们规定的数,没有单位
C.H2的摩尔质量等于NA个H2的质量之和D.标准状况下,H2的摩尔体积为22.4 L·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com