
����Ŀ��������Ϊ����������Դ֮һ���Ѿ��ܵ�����������ձ��ע����Ĵ洢������Ӧ�õ���Ҫƿ����Ŀǰ�����û������о�����Ҫ���ⷽ��������λ�⻯�ﴢ�⡢̼�ʲ��ϴ��⡢�Ͻ��⡢��ײ��ϴ���ȡ�
��ش�����������
��1��������( NH3BH3)��һ��DZ�ڵĴ�����ϣ���������Ԫ��״������(HB=NH)3ͨ��3CH4+2(HB=NH)3+6H2O=3CO2+6H3BNH3�Ƶ���
��B��C��N��O��һ�������ɴ�С��˳��Ϊ_____________��CH4��H2O��CO2�����ɴ�С��˳��Ϊ_________________��
��1��(HB=NH)3��������______����������(HB=NH)3��Ϊ�ȵ�����ķ���Ϊ________(�����ʽ)��
����Ӧǰ��̼ԭ�ӵ��ӻ�������ͷֱ�Ϊ__________��____________��
���������ڸ������ͷ�������ɵ�������������������ƽ��ʯ�Ľṹ�����۵�Ƚ��ʯ�ͣ�ԭ����___________________________��
��2��һ�ִ���Ͻ���������(La)������侧���ṹ��ͼ��ʾ��

��Ni �Ļ�̬ԭ�Ӻ�������Ų�ʽΪ_______________��
���þ���Ļ�ѧʽΪ_______________��
���þ�����ڲ����п�϶����ÿ�������Ŀ�϶�д���6����ԭ�ӱȽ��ȶ�����֪��a=m pm��c=n pm����״�����������ܶ�Ϊ��g��cm-3�������ӵ�������ֵΪNA������������ǰ��������仯����ô�����ϵĴ�������Ϊ______________�� (��������=![]() )
)
���𰸡� N>O>C>B CO2>CH4>H2O 12 C6H6 sp3 sp B��N���ļ�������C��C���ģ�����С��C��C����(ָ����������ܹ�ϵ������) 1s22s22p63s23p63d84s2��[Ar]3d84s2 LaNi5 ![]() ����
���� ��
��
����������1�������һ�����ܵĹ��ɡ����ǵĴ�С����ѧ����Ŀ���жϡ��ӻ����͵��жϣ������۷е�ߵ͵��жϣ���ͬ���ڴ������ҵ�һ����������IIA>IIIA��VA>VIA����˵�һ�����ܴ�С˳����N>O>C>B��CH4�ļ�����109��28�䣬H2O�ļ�����105�㣬CO2�ļ�����180�㣬˳����CO2>CH4>H2O���ڳɼ�ԭ�Ӽ�ֻ���γ�һ���Ҽ���(HB=NH)3Ϊ��Ԫ��״��������1��(HB=NH)3�к��ЦҼ�����Ϊ12�������ݵȵ�����ĸ����Լ�(HB=NH)3Ϊ��Ԫ��״������Ƴ��ȵ�����ķ���ΪC6H6���۷�ӦǰCΪsp3�ӻ�����Ӧ��̼ԭ��Ϊsp�ӻ�����������������������ƽ��ʯ�Ľṹ����������������Ϊԭ�Ӿ��壬�Ƚ�ԭ�Ӿ����۷е�ͨ�����������ܿ��ǣ�B��N���ļ�������C��C���ģ�����С��C��C�������������������۷е���ڽ��ʯ����2����������Ų�ʽ�������ļ��㣬��Niλ�ڵ�������VIII�壬28��Ԫ�أ�Ni�ĺ�������Ų�ʽΪ1s22s22p63s23p63d84s2��[Ar]3d84s2����Laλ�ڶ��㣬����Ϊ8��1/8=1��Niλ�����Ϻ����ģ�����Ϊ8��1/2��1=5����ѧʽΪLaNi5��������������Ϊ![]() g�����������Ϊ(m��10��10��m��10��10��n��10��10��sin60��)cm3��������������ܶ�Ϊ
g�����������Ϊ(m��10��10��m��10��10��n��10��10��sin60��)cm3��������������ܶ�Ϊ g/cm3����˴�����ϹʵĴ�������Ϊ
g/cm3����˴�����ϹʵĴ�������Ϊ![]() ����
����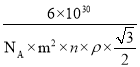 ����
����
�㾦��������ѵ��Ǵ��������ļ��㣬��Ȼ��Ŀ�и���ѧ��������������Ĺ�ʽ����ѧ���Դ�����������ܶ����ⲻ�������м��㣬��ʵ������������ܶȾ���������������������������뾧������ı�ֵ����ƽʱ��ϰ�����ܶȵļ�����һ���ģ�ֻ�����������������������������
�����͡�������
��������
12
����Ŀ��G��һ���������ϵ����ɷ�֮һ����ṹ�к���������Ԫ����G �ĺϳ�·������ͼ��ʾ(���ֲ���ͷ�Ӧ��������ȥ)��

��֪����RCH=CH2+CH2=CHR'![]() CH2=CH2+RCH=CHR'��
CH2=CH2+RCH=CHR'��
��B�ĺ˴Ź�������ͼ��ʾ��������6�ֲ�ͬ��������ԭ����
��D��F��ͬϵ�
��ش�����������
��1������ϵͳ��������(CH3)2C=CH2������Ϊ_____________��
��2��A��B��Ӧ�������漰�ķ�Ӧ���ͷֱ�Ϊ_______________��_________________��
��3������E�Ļ�ѧ����ʽΪ______________________________��
��4��G�Ľṹ��ʽΪ_________________��
��5��д��һ��ͬʱ��������������F��ͬ���칹��Ľṹ��ʽ��_________________��
����FeCl3��Һ������ɫ��Ӧ����������������ȡ��������C=O�������ܷ���ˮ�ⷴӦ�����˴Ź���������4��塣
��6��ģ���ɱ���ϩ�ϳ�F�ķ�����д���ɱ�ϩ��ȡa-�ǻ�����(![]() ) �ĺϳ�·����____________________________��
) �ĺϳ�·����____________________________��
���𰸡� 2-��-1-��ϩ(��2-����ϩ�������ϩ) ȡ����Ӧ �ӳɷ�Ӧ 
 ����
���� ��
�� ![]() (��
(��![]() )
) 
�������������л�����ƶϺͺϳɣ���1������ϩ��������ԭ��(CH3)2C=CH2������Ϊ2-��-1-��ϩ(��2-����ϩ�������ϩ)����2��������Ϣ�٣��Լ�A��Ӧ�IJ�����A�Ľṹ��ʽΪ ���Ա�A�Ͳ���Ľṹ��ʽ��A����
���Ա�A�Ͳ���Ľṹ��ʽ��A���� ��Ӧ����Ϊȡ����Ӧ���Աȷ���ʽ��
��Ӧ����Ϊȡ����Ӧ���Աȷ���ʽ�� ��B����һ��HCl�������ķ�Ӧ�Ǽӳɷ�Ӧ��B�Ľṹ��ʽ������
��B����һ��HCl�������ķ�Ӧ�Ǽӳɷ�Ӧ��B�Ľṹ��ʽ������ ����
����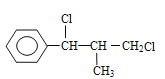 ����ΪB�ĺ˴Ź���������6�ֲ�ͬ��������ԭ�ӣ����B�Ľṹ��ʽΪ
����ΪB�ĺ˴Ź���������6�ֲ�ͬ��������ԭ�ӣ����B�Ľṹ��ʽΪ ��B����C����±������ˮ�ⷴӦ����C�Ľṹ��ʽΪ
��B����C����±������ˮ�ⷴӦ����C�Ľṹ��ʽΪ ��C����D����������Ӧ����D�Ľṹ��ʽΪ
��C����D����������Ӧ����D�Ľṹ��ʽΪ ������ϩ��HO��Br�����ӳɷ�Ӧ��E�Ľṹ��ʽΪ
������ϩ��HO��Br�����ӳɷ�Ӧ��E�Ľṹ��ʽΪ ��
�� ��ǰ�߱�������
��ǰ�߱������� �����߱�������
�����߱������� �����߲�������Ϣ��E�Ľṹ��ʽΪ
�����߲�������Ϣ��E�Ľṹ��ʽΪ ��E�IJ�����
��E�IJ����� ��F�Ľṹ��ʽΪ
��F�Ľṹ��ʽΪ ����3�����ݣ�2���ķ���������E�ķ�Ӧ����ʽΪ
����3�����ݣ�2���ķ���������E�ķ�Ӧ����ʽΪ ����4��G��������Ԫ��������G������������Ӧ����G�Ľṹ��ʽΪ/span>
����4��G��������Ԫ��������G������������Ӧ����G�Ľṹ��ʽΪ/span> ����
���� �� ����5����FeCl3������ɫ��Ӧ��˵�����з��ǻ���������������ȡ��������C=O�����ܷ���ˮ�⣬˵�������������˴Ź���������4����ԭ��������ȡ�������ڶ�λ�������������Ľṹ��ʽΪ
�� ����5����FeCl3������ɫ��Ӧ��˵�����з��ǻ���������������ȡ��������C=O�����ܷ���ˮ�⣬˵�������������˴Ź���������4����ԭ��������ȡ�������ڶ�λ�������������Ľṹ��ʽΪ![]() (��
(��![]() ) ����6����ϩ����HO��Br�����ӳɷ�Ӧ��Ȼ�������������ˮ�⣬���ϳ�·����
) ����6����ϩ����HO��Br�����ӳɷ�Ӧ��Ȼ�������������ˮ�⣬���ϳ�·���� ��
��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ƣ�CaO2����һ��������ˮ��������İ�ɫ���壬�㷺���ڹ��߱��ʡ�������������ˮ�����ȷ��档������һ���Ʊ��������Ƶ�ʵ�鷽����

�ش��������⣺
(1)��ͼ��ijѧ���Ĺ��˲���ʾ��ͼ����������淶����____��

a��©��ĩ�˾���δ�����ձ���
b���ò�������©������������Լӿ�����ٶ�
c������ֽʪ��ʹ�����©����
d����������������
(2)�������Ҫ�ڱ�ԡ�½��У�ԭ����_______��
(3)����ۼ��� CaO2�� 8H2O�Ƿ�ϴ���ķ����ǣ�ȡ���һ��ϴ��Һ�������Թ��У�_______��
(4)�Ʊ��������Ƶ���һ�ַ����ǣ���ʯ��ʯ���պ�ֱ�Ӽ���˫��ˮ��Ӧ�����˺�ɵõ��������Ʋ�Ʒ���ù��շ�����ȱ����_______��
(5)д���ڷ����Ļ�ѧ����ʽ_______��
(6)��֪CaO2��350��Ѹ�ٷֽ�����CaO��O2����ͼ��ʵ���Ҳⶨ��Ʒ��CaO2 ������װ�ã��г�װ��ʡ�ԣ���

����ȡ��Ʒ������ m g������������Ϊ V mL���ѻ���ɱ�״���������Ʒ��CaO2����������Ϊ_______������ĸ��ʾ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ�������£������ʵ������������ʷֱ���������Ũ���ᷴӦ������Cl2�����ʵ���������
A.MnO2B.KClO3C.KMnO4D.Ca(ClO)2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������л��������������ԣ�
���������գ�
��1�����ӡ������ᡢ̼���������ǿ������˳��Ϊ ��
��2�������������ʵ�����Է������ijһ����ﺬ���ӡ����״���������ͱ����������ʣ�����뷽������ͼ��
��֪�����״��������ᡢ��������ˮ���ұ����� ![]() �����м��ԣ�
�����м��ԣ�
A��B��C�ֱ��ǣ�A �� B �� C
���������У������Ƚ������������������������ʷֿ�����Ӧ���� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������̼���á�����Ϊ��ѧ���о�����Ҫ������Ϊ�˼��ٿ����е��������������ҳ�����ö�����̼��Դ����ѧ����������һϵ�в��ͷ�������̼�ķ�����
��1���п�ѧ�����������FeO���պ�����CO2������Ȼ�ѧ����ʽ������
6FeO(s)+CO2(g)=2Fe3O4(s)+C(s) ��H=-76.0 kJ��mol-1
��������Ӧ��ÿ����1 mol Fe3O4��ת�Ƶ��ӵ����ʵ���Ϊ_______mol��
����֪��C(s)+2H2O(g)=CO2(g)+2H2(g) ��H=+113.4kJ��mol-1����Ӧ��3FeO(s)+ H2O(g)= Fe3O4(s)+ H2(g)�ġ�H=__________��
��2���ð�ˮ���������е�CO2��������Ǽ���CO2�ŷŵĿ��д�ʩ֮һ��
�ٷֱ��ò�ͬpH�����ռ����������е�CO2��CO2�ѳ�Ч�������ռ���pH��ϵ��ͼ��ʾ����������CO2�ĺ��������������Ϊ12��������ͨ�백ˮ������Ϊ0.052 m3��h-1(��״��)����pHΪ12.81�İ�ˮ��������30min���ѳ���CO2�����ʵ������Ϊ____________(��ȷ��0.01)��

��ͨ��������¶����ߣ�CO2�ѳ�Ч����ߣ�������40��ʱ���ѳ�CO2Ч�ʽ��͵���Ҫԭ����______________��
��3��һ����������Pd-Mg/SiO2������ʹCO2�����黯���Ӷ����Ϊ�����䷴Ӧ������ͼ��ʾ��

���÷�Ӧ�Ļ�ѧ����ʽΪ______________________����Ӧ������̼Ԫ�صĻ��ϼ�Ϊ-2�۵��м�����_________________��
����һ�ݻ�Ϊ2 L�ĺ����ܱ������г���һ������CO2��H2����300��ʱ����������Ӧ���ﵽƽ��ʱ�����ʵ�Ũ�ȷֱ�ΪCO2��0.2 mol��L-1��H2��0.8 mol��L-1��CH4��0.8 mol��L-1��H2O��1.6 mol��L-1��CO2��ƽ��ת����Ϊ_________________��300��ʱ������Ӧ��ƽ�ⳣ��K=___________________��
����֪�÷�Ӧ����Ӧ���ȣ�����������ͬ�ĺ��ݾ���(���������������)�ܱ������������г���1molCO2��4molH2�������г���1molCH4��2molH2O(g)��300���¿�ʼ��Ӧ���ﵽƽ��ʱ������˵����ȷ����___________________(����ĸ)��
A.������������Ӧ������ͬ
B.��������CH4�����ʵ���������ͬ
C.��������CO2�����ʵ������������еĶ�
D.��������CO2��ת��������������CH4��ת����֮��С��1
���𰸡� 2 +18.7kJ��mol-1 0.13mol ̼��������ȷֽ����ɶ�����̼����ˮ���Ȼӷ� CO2+4H2![]() CH4+2H2O MgOCH2 80% 25 CD
CH4+2H2O MgOCH2 80% 25 CD
����������1�������ʧ���ӵļ��㡢�Ȼ�ѧ��Ӧ����ʽ�ļ��㣬�ٸ��ݷ�Ӧ����ʽ��ֻ��CO2��C�Ļ��ϼ۽��ͣ�����1molFe3O4ʱ����0.5molCO2����ת�Ƶ������ʵ���Ϊ0.5��4mol=2mol����6FeO(s)+CO2(g)=2Fe3O4(s)+C(s) �٣�C(s)+2H2O(g)=CO2(g)+2H2(g) �ڣ�(�٣���)/2���ó���H=(��76.0��113.4)/2kJ��mol��1=��18.7kJ��mol��1����2�����黯ѧ���㡢��ѧ��Ӧ������������pH=12.81����ʱ��CO2�ѳ�Ч��Ϊ91.6%���ѳ�CO2�����ʵ������Ϊ mol=0.13mol���ڰ�ˮ�����ӷ����¶ȹ��ߣ���ɰ�ˮ�ӷ�������CO2�������٣�CO2��NH3��Ӧ������NH4HCO3��NH4HCO3���ȷֽ⣬���CO2�ѳ�Ч�ʽ��ͣ���3�����黯ѧƽ��ļ��㡢��������ԭ�����ٸ��ݷ�Ӧ���������������м���������CO2��H2�����ɵ���CH4��H2O����˷�Ӧ����ʽΪCO2+4H2
mol=0.13mol���ڰ�ˮ�����ӷ����¶ȹ��ߣ���ɰ�ˮ�ӷ�������CO2�������٣�CO2��NH3��Ӧ������NH4HCO3��NH4HCO3���ȷֽ⣬���CO2�ѳ�Ч�ʽ��ͣ���3�����黯ѧƽ��ļ��㡢��������ԭ�����ٸ��ݷ�Ӧ���������������м���������CO2��H2�����ɵ���CH4��H2O����˷�Ӧ����ʽΪCO2+4H2![]() CH4+2H2O��MgΪ��2�ۣ�HΪ��1�ۣ�OΪ��2�ۣ���˱��֣�2�۵��м���ΪMgOCH2���� CO2+4H2
CH4+2H2O��MgΪ��2�ۣ�HΪ��1�ۣ�OΪ��2�ۣ���˱��֣�2�۵��м���ΪMgOCH2���� CO2+4H2![]() CH4+2H2O
CH4+2H2O
ƽ�⣺ 0.2 0.8 0.8 1.6
�仯��0.8 3.2 0.8 1.6
��ʼ��1 4 0 0��CO2��ת����Ϊ0.8/1��100%=80%������ƽ�ⳣ���Ķ��壬K= =25����A������Ӧ�Ƿ��ȷ�Ӧ����ӦI��������Ӧ������У��¶����ߣ���ѧ���ʿ죬��ӦII�����淴Ӧ������У������ȷ�Ӧ����������¶Ƚ��ͣ���ѧ��Ӧ���ʱ仺����A����B����ӦI������Ӧ������У��¶����ߣ�����Ϊ���ݾ��ȣ���������Ӧ������������ƣ��������������CH4������������ͬ����B����C������Bѡ���������C��ȷ��D����������Ǻ��º��ݣ���CO2��ת�����뷴ӦII��CH4��ת����֮��Ϊ1����Ϊ�Ǻ��ݾ���������ת���ʶ�Ҫ���ͣ��������ת���ʵĺ�С��1����D��ȷ��
=25����A������Ӧ�Ƿ��ȷ�Ӧ����ӦI��������Ӧ������У��¶����ߣ���ѧ���ʿ죬��ӦII�����淴Ӧ������У������ȷ�Ӧ����������¶Ƚ��ͣ���ѧ��Ӧ���ʱ仺����A����B����ӦI������Ӧ������У��¶����ߣ�����Ϊ���ݾ��ȣ���������Ӧ������������ƣ��������������CH4������������ͬ����B����C������Bѡ���������C��ȷ��D����������Ǻ��º��ݣ���CO2��ת�����뷴ӦII��CH4��ת����֮��Ϊ1����Ϊ�Ǻ��ݾ���������ת���ʶ�Ҫ���ͣ��������ת���ʵĺ�С��1����D��ȷ��
�㾦��������ѵ��ǣ�3���ۣ�ѧ��û��ע������Ǻ��ݾ��ȣ���ɴ�ѡ������������������������Ľ�������Aѡ�����I����Ӧ�Ƿ��ȷ�Ӧ��������Ӧ������У��¶����ߣ���ѧ��Ӧ������������II�������淴Ӧ������У��������ȷ�Ӧ������У��¶Ƚ��ͣ���ѧ��Ӧ���ʱ仺�����ƽʱ����ʱ������Ҫ�ҵ��ص㡣
�����͡�������
��������
11
����Ŀ��������Ϊ����������Դ֮һ���Ѿ��ܵ�����������ձ��ע����Ĵ洢������Ӧ�õ���Ҫƿ����Ŀǰ�����û������о�����Ҫ���ⷽ��������λ�⻯�ﴢ�⡢̼�ʲ��ϴ��⡢�Ͻ��⡢��ײ��ϴ���ȡ�
��ش�����������
��1��������( NH3BH3)��һ��DZ�ڵĴ�����ϣ���������Ԫ��״������(HB=NH)3ͨ��3CH4+2(HB=NH)3+6H2O=3CO2+6H3BNH3�Ƶ���
��B��C��N��O��һ�������ɴ�С��˳��Ϊ_____________��CH4��H2O��CO2�����ɴ�С��˳��Ϊ_________________��
��1��(HB=NH)3��������______����������(HB=NH)3��Ϊ�ȵ�����ķ���Ϊ________(�����ʽ)��
����Ӧǰ��̼ԭ�ӵ��ӻ�������ͷֱ�Ϊ__________��____________��
���������ڸ������ͷ�������ɵ�������������������ƽ��ʯ�Ľṹ�����۵�Ƚ��ʯ�ͣ�ԭ����___________________________��
��2��һ�ִ���Ͻ���������(La)������侧���ṹ��ͼ��ʾ��

��Ni �Ļ�̬ԭ�Ӻ�������Ų�ʽΪ_______________��
���þ���Ļ�ѧʽΪ_______________��
���þ�����ڲ����п�϶����ÿ�������Ŀ�϶�д���6����ԭ�ӱȽ��ȶ�����֪��a=m pm��c=n pm����״�����������ܶ�Ϊ��g��cm-3�������ӵ�������ֵΪNA������������ǰ��������仯����ô�����ϵĴ�������Ϊ______________�� (��������=![]() )
)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��H2��O2������Ӧ�Ĺ�����ģ��ͼʾ���£���������ʾ��ѧ����������˵������ȷ���ǣ������� 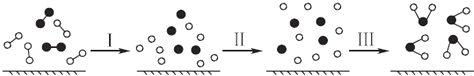
A.���̢������ȹ���
B.���̢�һ���Ƿ��ȹ���
C.�÷�Ӧ�������оɻ�ѧ�������ѣ����γ����»�ѧ��
D.�÷�Ӧ������ת����ʽֻ�������ܵ���ʽ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��2H2��O2![]() 2H2O��
2H2O��
��1���÷�Ӧ1g������ȫȼ�շų�����121.6kJ�����ж���1molH-H������436kJ������1molO=O������496kJ����ô�γ�1molH-O���ų�����____________________��
��2��ԭ�����ֱ�Ӱѻ�ѧ��ת��Ϊ���ܵ�װ�á�
I.���켼����ʹ�õ��⣭��ȼ�ϵ�ؾ��и��ܡ����Ͳ���Ⱦ�������ŵ㡣��ͼ���⣭��ȼ�ϵ�ص�װ��ͼ����

����Һ��OH-����________�缫������a������b������
��b�缫����pH_____________��(������С��)
�����H2��Ϊ��������缫��ӦʽΪ��������____________________________��������________________________________��
II.��пƬ����Ƭ����ϡ���������ԭ��أ����缫������һ�������������õ�������缫��������Ϊ60g������һ��ʱ���ȡ��пƬ����Ƭϴ���������أ�������Ϊ47g���Լ��㣺�������������___________________________________L������״����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʵ�������Ӧ�ù�ϵ����������ȷ���ǣ���
A.����þ���۵�ߣ������ʵ����²���
B.�������Ż𣬲�������ĭ��������
C.������ǿ�����ԣ���������Ư�������ɫ����
D.����������Ư���ԣ�������Ư��ë��˿��ֽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��W��X��Y��Z�����ֳ����Ķ���������Ԫ�أ���ԭ�Ӱ뾶��ԭ�������ı仯��ͼ��ʾ��

��֪Y��Z����Ԫ�صĵ����ǿ�������Ҫ�ɷ֣�Wԭ�ӵ�������������Neԭ�ӵ��������������1����ش��������⣺
��1��д������Ԫ�ص�Ԫ�ط��ţ�W________��X________��Y________��Z________��
��2������Ԫ�ص����л��ϼ��У�������ϼ�Ϊ________�ۣ���������ϼ�Ϊ________�ۡ�
��3�����ҷֱ�����W��X��Y��Z����Ԫ���е�����Ԫ����ɵij���������������������ɱ�����ã��仯ѧʽΪ________������������һ�ֳ����Ļ��ʣ��仯ѧʽΪ________��
��4��HYO3�����Ա�HWOǿ�����˾ݴ���ΪY�ķǽ�����ǿ��W������Ϊ���ֿ����Ƿ���ȷ��˵�����ɣ�________ ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com