
【题目】锌是一种常用金属,工业上利用锌焙砂(主要含ZnO、ZnFe2O4,还含有少量CaO、FeO、CuO、NiO 等)湿法制取金属锌的流程如图所示,回答下列问题。

已知:Fe的活泼性强于Ni。
(1)ZnFe2O4可写成ZnOFe2O3,则ZnFe2O4与H2SO4反应的化学方程式___。
(2)“净化Ⅰ”操作分为两步:
①将溶液中少量的 Fe2+氧化,下列试剂中可选用的是_____(填字母标号)。
A.新制氯水 B.30 % H2O2溶液 C.FeC13溶液 D.KMnO4溶液
②加入ZnO,调节溶液pH为3.3~6.7;加热到60℃左右并不断搅拌,加热搅拌主要目的是___。
(3)“净化Ⅰ”生成的沉淀中还含有溶液中的悬浮杂质,溶液中的悬浮杂质被共同沉淀的原因是____。
(4)“净化Ⅱ”中加入过量Zn的目的是______。
【答案】![]() B 促进三价铁离子水解转化为沉淀,并使过量的过氧化氢分解除去 氢氧化铁胶粒具有吸附性 使铜离子、镍离子转化为单质而除去
B 促进三价铁离子水解转化为沉淀,并使过量的过氧化氢分解除去 氢氧化铁胶粒具有吸附性 使铜离子、镍离子转化为单质而除去
【解析】
(1)根据信息ZnFe2O4可写成ZnOFe2O3可知,酸浸时ZnFe2O4会生成两种盐,分别为硫酸锌、硫酸铁,即ZnFe2O4与硫酸反应生成硫酸锌、硫酸铁、水,反应的化学方程式为:ZnFe2O4+4H2SO4═ZnSO4+Fe2(SO4)3+4H2O;
(2)①将溶液中少量的 Fe2+氧化,应选用氧化性较强且产物不会引入新杂质的物质,新制氯水的还原产物为氯离子,会引入新的杂质,氯化铁无法将Fe2+氧化,且会引入新的杂质,KMnO4溶液还原产物为二价锰离子,会引入新的杂质,因此应当加入过氧化氢,选B;
②加热搅拌的目的是促进三价铁离子水解转化为沉淀,并使过量的过氧化氢分解除去;
(3)因为Fe(OH)3胶粒具有吸附性,则净化Ⅰ生成的沉淀中还含有溶液中的悬浮杂质;
(4)加入稀硫酸后生成物中含有硫酸铁、硫酸亚铁、硫酸锌、硫酸铜、硫酸镍、硫酸钙,其中硫酸钙微溶于水,净化Ⅰ后除去Fe元素,所以净化Ⅱ中加入Zn的目的是使Cu2+、Ni2+转化为Cu、Ni而除去。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列关于晶体的说法中,正确的有( )
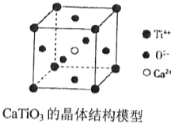
(图中Ca2+、O2-、Ti4+分别位于立方体的体心、面心和顶点)
①分子晶体中都存在共价键②在晶体中只要有阳离子就一定有阴离子③铯、钾、钠、钠-钾合金的熔点依次降低④离子晶体中只有离子键没有共价键,分子晶体中肯定没有离子键⑤CaTiO3晶体中(晶胞结构如上图所示)每个Ti4+和12个O2-相紧邻⑥12g石墨中含有的C-C键的个数为1.5NA(NA为阿伏加德罗常数)⑦晶体中分子间作用力越大,分子越稳定⑧离子晶体CaO的晶格能比KCl高,熔点KCl比CaO低
A. 2种B. 3种C. 4种D. 5种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国明崇祯年间《徐光启手迹》记载了《造强水法》 :“绿钒(FeSO47H2O)五斤,硝五斤,将矾炒去,约折五分之一,将二味同研细,次用铁作锅,…… 锅下起火,取气冷定,开坛则药化为水……。用水入五金皆成水,惟黄金不化水中,加盐则化。……强水用过无力……”。下列有关解释错误的是
A.“将矾炒去,约折五分之一”后生成FeSO44H2O
B.该方法所造“强水”为硝酸
C.“惟黄金不化水中,加盐则化”的原因是加人 NaCl溶液后氧化性增强
D.“强水用过无力”的原因是“强水”用过以后,生成了硝酸盐溶液,其氧化性减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从经济效益和环境保护考虑,大量制取硝酸铜最宜采用的方法是( )
A.Cu+HNO3(浓)→Cu(NO3)2
B.Cu+HNO3(稀)→Cu(NO3)2
C.Cu![]() CuO
CuO![]() Cu(NO3)2
Cu(NO3)2
D.Cu+AgNO3→Cu(NO3)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某碱性电池的总反应为:3HO2-+2Al=OH-+2AlO2-+H2O,工作原理如图所示。下列叙述错误的是
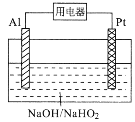
A.电子迁移方向:Al→用电器→Pt
B.电池工作时,负极附近溶液pH减小
C.正极反应式为:HO2-+3H+ +2e-=2H2O
D.负极会发生副反应:2Al+2OH-+2H2O=2AlO2-+3H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式如图所示,下列说法中不正确的是
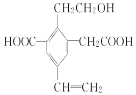
A.1 mol该有机物和过量的金属钠反应最多可以生成1.5 mol H2
B.可以用酸性KMnO4溶液检验其中的碳碳双键
C.该物质能够在催化剂作用下与H2反应,物质的量之比1∶4
D.该物质最多消耗Na、NaOH、NaHCO3的物质的量之比为3∶2∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列物质:① N2 ②Na2O2 ③NaOH ④HCl ⑤H2O2 ⑥MgF2 ⑦NH4Cl。
(1)只由非极性键构成的物质是__________________(填编号)。
(2)由离子键和极性键构成的物质是_______________。
(3)⑤H2O2的电子式为:_________________。
(4)用电子式表示⑥MgF2的形成过程:______________。
(5)下列说法不正确的是________。
①共价化合物中含共价键,也可能含离子键
②因为H2CO3酸性<H2SO3酸性,所以非金属性C<S
③含金属元素的化合物不一定是离子化合物
④由非金属元素组成的化合物一定是共价化合物
⑤熔融状态能导电的物质是离子化合物
⑥由分子组成的化合物中一定存在共价键
A. ①③⑤ B. ①②⑥ C. ①②④⑤ D. ①③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机化学的认识中,正确的是( )
A.![]() 分子中的四个碳原子可能在同一直线上
分子中的四个碳原子可能在同一直线上
B.淀粉和纤维素属于多糖,均可在人体内水解转化为葡萄糖,为人类提供能量
C.分子式为C4H10O且能和金属钠反应的有机物共有三种(不考虑立体异构)
D.有机物C4H8ClBr的同分异构体(不含立体异构)有12种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列的图示与对应的叙述不相符的是( )
A.图1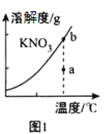 表示KNO3的溶解度曲线,图中a点表示的溶液通过恒温蒸发可以达到b点
表示KNO3的溶解度曲线,图中a点表示的溶液通过恒温蒸发可以达到b点
B.图2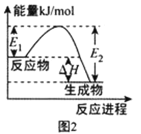 表示某一放热反应,若使用合适的催化剂,
表示某一放热反应,若使用合适的催化剂,![]() 、
、![]() 均减小,
均减小,![]() 不变
不变
C.图3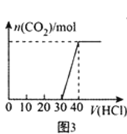 表示向Na2CO3和NaOH的混合溶液中滴加稀盐酸时,产生CO2的情况
表示向Na2CO3和NaOH的混合溶液中滴加稀盐酸时,产生CO2的情况
D.图4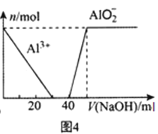 表示向100mL0.1mol/L的AlCl3和0.1mol/L的(NH4)2SO4混合溶液中滴加1mol/L的NaOH溶液时n(Al3+)和n(AlO2-)的变化情况
表示向100mL0.1mol/L的AlCl3和0.1mol/L的(NH4)2SO4混合溶液中滴加1mol/L的NaOH溶液时n(Al3+)和n(AlO2-)的变化情况
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com