
【题目】某有机物的结构简式如图所示,下列说法中不正确的是
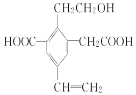
A.1 mol该有机物和过量的金属钠反应最多可以生成1.5 mol H2
B.可以用酸性KMnO4溶液检验其中的碳碳双键
C.该物质能够在催化剂作用下与H2反应,物质的量之比1∶4
D.该物质最多消耗Na、NaOH、NaHCO3的物质的量之比为3∶2∶2
【答案】B
【解析】
A. 1mol-OH和钠反应生成0.5mol的氢气,2mol-COOH和钠反应生成1mol的氢气,1 mol该有机物和过量的金属钠反应最多可以生成1.5 mol H2,A项正确;
B. 结构中的醇羟基,苯环的侧链均能和酸性高锰酸钾反应,所以不能用酸性KMnO4溶液检验其中的碳碳双键,B项错误;
C. 1mol苯环可以加成3mol H2,1mol碳碳双键可以加成1mol H2,该物质能够在催化剂作用下与H2反应,物质的量之比1:4,C项正确;
D. 1mol羟基和2mol羧基共消耗3mol钠,2mol羧基共消耗2molNaOH,2mol羧基共消耗2molNaHCO3,所以该有机物最多消耗Na、NaOH、NaHCO3的物质的量之比为3∶2∶2,D项正确;
答案选B。


科目:高中化学 来源: 题型:
【题目】利用如图所示装置进行以下实验,能得到相应实验结论的是
① | ② | ③ | 实验结论 |
| |
A | 浓氨水 | NaOH | 酚酞 | NaOH的碱性比 NH3H2O的强 | |
B | 浓盐酸 | MnO2 | 淀粉溶液 | 非金属性:氯元素大于碘元素 | |
C | 浓硝酸 | Na2CO3 | Na2SiO3 | 酸性:HNO3 > H2CO3 > H2SiO3 | |
D | 浓硫酸 | 蔗糖 | 溴水 | 浓硫酸具有脱水性、氧化性 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在短周期元素中:
①元素周期表IA族中金属性最强的元素(符号)是____,与水反应最剧烈的VIIA族中的非金属元素的(符号)是___;
②原子核外电子总数是其最外层电子数2倍的元素名称是__,最外层电子数为电子层2倍的元素名称有____。
(2)已知某主族元素的原子结构示意图如图,Y在周期表的位置为___。

(3)A2-原子核内有x个中子,其质量数为m,则ngA2-所含电子的物质的量为__。
(4)X、Y、Z均为短周期元素,它们在周期表中的相对位置如图所示。
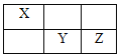
已知X、Y、Z三元素的原子序数之和为40,回答下列问题:
①Z元素的原子结构示意图为___。
②与Y同主族的下一周期元素的原子序数是___。
③X的气态氢化物与Y的最高价氧化物对应水化物发生的化学反应方程式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锌是一种常用金属,工业上利用锌焙砂(主要含ZnO、ZnFe2O4,还含有少量CaO、FeO、CuO、NiO 等)湿法制取金属锌的流程如图所示,回答下列问题。

已知:Fe的活泼性强于Ni。
(1)ZnFe2O4可写成ZnOFe2O3,则ZnFe2O4与H2SO4反应的化学方程式___。
(2)“净化Ⅰ”操作分为两步:
①将溶液中少量的 Fe2+氧化,下列试剂中可选用的是_____(填字母标号)。
A.新制氯水 B.30 % H2O2溶液 C.FeC13溶液 D.KMnO4溶液
②加入ZnO,调节溶液pH为3.3~6.7;加热到60℃左右并不断搅拌,加热搅拌主要目的是___。
(3)“净化Ⅰ”生成的沉淀中还含有溶液中的悬浮杂质,溶液中的悬浮杂质被共同沉淀的原因是____。
(4)“净化Ⅱ”中加入过量Zn的目的是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫代硫酸钠(Na2S2O3)是一种重要的化工产品,将SO2通入Na2CO3和Na2S混合溶液中可制得Na2S2O3。其制备装置如图所示。

(1)A中反应的化学方程式为_____。
(2)为保证Na2S和Na2CO3得到充分利用,两者的物质的量之比应为____。
(3)为了保证硫代硫酸钠的产量,实验中通人的SO2不能过量,原因是___。
(4)待Na2S和Na2CO3完全消耗后,结束反应。过滤B中的混合物,滤液经过__、___(填操作名称)、过滤、洗涤、干燥,得到Na2S2O35H2O晶体。
(5)称取10.0g产品(Na2S2O35H2O,相对分子质量为248),配成250mL溶液,取25.00mL溶液,以淀粉作指示剂,用 0.1000 mol/L碘的标准溶液滴定。(反应原理为:2S2O32-+I2 = S4O62-+2I-,忽略Na2SO3与I2反应)。
①滴定终点的现象为____。
②重复三次的实验数据如表所示,其中第三次读数时滴定管中起始和终点的液面位置如图所示,则x=____,产品的纯度为__。


查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关电解质溶液的说法正确的是
A. 向0.1 molL-1CH3COOH溶液中加入少量水,溶液中c(H+)/c(CH3COOH)减小
B. 用惰性电极电解MgCl2溶液,电解的离子方程式为: 2Cl-+2H2O![]() H2↑+Cl2↑+2OH-
H2↑+Cl2↑+2OH-
C. 向盐酸中加入氨水至中性,溶液中c(NH4+)/c(Cl-)>1
D. 将AgCl与AgBr的饱和溶液等体积混合,再加入足量AgNO3溶液,生成的沉淀AgCl多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图中的实验装置进行相应的实验,不能达到实验目的的是( )
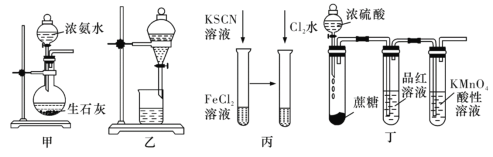
A.用图甲装置,可快速制取氨气
B.用图乙装置,分离饱和食盐水溶液中的食盐和水
C.用图丙装置操作方法,可检验Fe2+
D.用图丁装置,可说明浓H2SO4具有脱水性和强氧化性.,SO2具有漂白性和还原性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列模型分别表示C2H2、S8、SF6的结构,下列说法错误的是( )
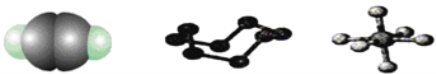
A. 32 g S8分子中含有0.125 mol σ键
B. SF6是由极性键构成的分子
C. 1 mol C2H2分子中有3 mol σ键和2 mol π键
D. S8中S的杂化方式为sp3杂化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com