
【题目】硫代硫酸钠(Na2S2O3)是一种重要的化工产品,将SO2通入Na2CO3和Na2S混合溶液中可制得Na2S2O3。其制备装置如图所示。

(1)A中反应的化学方程式为_____。
(2)为保证Na2S和Na2CO3得到充分利用,两者的物质的量之比应为____。
(3)为了保证硫代硫酸钠的产量,实验中通人的SO2不能过量,原因是___。
(4)待Na2S和Na2CO3完全消耗后,结束反应。过滤B中的混合物,滤液经过__、___(填操作名称)、过滤、洗涤、干燥,得到Na2S2O35H2O晶体。
(5)称取10.0g产品(Na2S2O35H2O,相对分子质量为248),配成250mL溶液,取25.00mL溶液,以淀粉作指示剂,用 0.1000 mol/L碘的标准溶液滴定。(反应原理为:2S2O32-+I2 = S4O62-+2I-,忽略Na2SO3与I2反应)。
①滴定终点的现象为____。
②重复三次的实验数据如表所示,其中第三次读数时滴定管中起始和终点的液面位置如图所示,则x=____,产品的纯度为__。


【答案】![]() 2:1 二氧化硫融入过多使溶液呈酸性,而
2:1 二氧化硫融入过多使溶液呈酸性,而![]() 可以与氢离子反应,导致产量降低 蒸发浓缩 冷却结晶 溶液由无色变为蓝色,且半分钟颜色不退去 18.10 89.28%
可以与氢离子反应,导致产量降低 蒸发浓缩 冷却结晶 溶液由无色变为蓝色,且半分钟颜色不退去 18.10 89.28%
【解析】
装置A为二氧化硫的发生装置,装置B为硫代硫酸钠的制备装置,装置C为尾气处理装置。
(1)A为二氧化硫的发生装置,反应的化学方程式为![]() ;
;
(2)装置B中发生的反应为![]() ,为保证Na2S和Na2CO3得到充分利用,两者的物质的量之比应为2:1;
,为保证Na2S和Na2CO3得到充分利用,两者的物质的量之比应为2:1;
(3)硫代硫酸钠在酸性条件下会发生水解,二氧化硫过量会使溶液呈酸性,导致产品产量减少,所以二氧化硫不能过量;
(4)过滤B中的混合物,滤液经过蒸发浓缩、冷却结晶、过滤、洗涤、干燥,得到Na2S2O35H2O晶体;
(5)①滴定所用指示剂是淀粉溶液,当达到滴定终点时,碘稍过量,碘遇淀粉变蓝色;所以溶液会由无色变为蓝色;
②由滴定管的读数可知,开始的刻度是0.50mL,后来的读数是18.60mL,所用溶液的体积是18.10mL,即x=18.10mL,实验序号1所得的体积与另外两组相差较大,舍去,则消耗标准液的平均体积为18.00mL,则碘的物质的量是0.0180L×0.1000mol/L,根据碘与硫代硫酸钠反应的方程式可知硫代硫酸钠的物质的量是0.0180L×0.1000mol/L×2×10=0.036mol,所以产品的纯度为![]() ×100%=89.28%。
×100%=89.28%。


 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】X、Y、Z三种短周期元素,原子半径的大小关系为r(Y)>r(X)>r(Z),原子序数之和为16。X、Y、Z三种元素的常见单质在适当的条件下可发生如图所示的变化,其中A为X、Y组成的双原子分子,B和C均为10电子分子。下列说法不正确的是
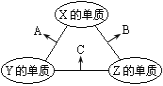
A.X元素位于第ⅥA族B.A不能溶于B中
C.A和C不可能发生氧化还原反应D.C溶于B形成的溶液呈碱性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对如图所示的两种化合物的结构或性质描述正确的是:
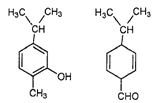
A. 均能与溴水反应B. 分子中肯定共平面的碳原子数相同
C. 不是同分异构体D. 可以用红外光谱区分,亦能用核磁共振氢谱区分
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随原子序数的递增,五种短周期元素原子半径与原子序数的关系如图所示。
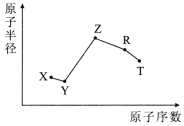
已知:TX2是现代光学及光纤制品的基本原料;ZY 能破坏水的电离平衡;Z3RY6在工业上常用作助熔剂。
(1)R在元素周期表中的位置是___。
(2)上述元素中的某两种元素可组成一种五原子共价化合物,该化合物的电子式为___。
(3)请用一个化学方程式比较X和Y的非金属性的强弱_____。
(4)工业上以Z3RY6作助熔剂的目的是____。
(5)已知11.5gZ的单质在X2中完全燃烧,恢复至室温,放出QkJ热量,该反应的热化学方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构简式如图所示,下列说法中不正确的是
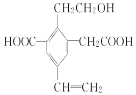
A.1 mol该有机物和过量的金属钠反应最多可以生成1.5 mol H2
B.可以用酸性KMnO4溶液检验其中的碳碳双键
C.该物质能够在催化剂作用下与H2反应,物质的量之比1∶4
D.该物质最多消耗Na、NaOH、NaHCO3的物质的量之比为3∶2∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验误差分析错误的是
A. 用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小
B. 滴定前滴定管内无气泡,终点读数时有气泡,所测体积偏小
C. 用润湿的pH试纸测稀碱溶液的pH,测定值偏小
D. 测定中和反应的反应热时,将碱缓慢倒入酸中,所测温度值偏小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如下图所示的装置,C、D、E、F、X、Y都是惰性电极。将电池接通后,向乙中滴入酚酞溶液,在F极附近溶液显红色。则以下说法正确的是

A.电源B极是正极
B.甲、乙装置的C、D、E、F电极均有单质生成,其物质的量之比为1∶2∶2∶1
C.欲用丙装置给铜镀银,H应该是Ag,电镀液是AgNO3溶液
D.装置丁中Y极附近红褐色变深,说明氢氧化铁胶粒带正电荷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:pKa=-lgKa,25℃时,H2A 的 pKa1=1.85,pKa2=7.19。常温下,用 0.1 mol/LNaOH 溶液滴定20 mL 0.1 mol/LH2A 溶液的滴定曲线如图所示。下列说法正确的是
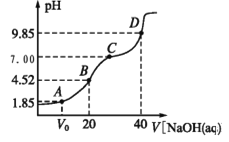
A. A 点所得溶液中:V0<10 mL
B. B 点所得溶液中:c(H2A)+c(H+)=c(HA-)+c(OH-)
C. C 点所得溶液中:c(A2-)= c(Na+)-c(HA-)-c(H2A)
D. D 点所得溶液中 A2-水解平衡常数 Kh1=10-7.19
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据杂化轨道理论和价电子对互斥模型判断,下列分子或者离子的中心原子杂化方式及空间构型正确的是( )
选项 | 分子或离子 | 中心原子杂化方式 | 价电子对互斥模型 | 分子或离子的立体构型 |
A. | SO2 | sp | 直线形 | 直线形 |
B. | HCHO | sp2 | 平面三角形 | 三角锥形 |
C. | NF3 | sp2 | 四面体形 | 平面三角形 |
D. |
| sp3 | 正四面体形 | 正四面体形 |
A. AB. BC. CD. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com