
【题目】下列各组物质的性质,从左到右依次递减的是
A.碱性:![]() 、
、![]() 、
、![]() B.还原性:
B.还原性:![]() 、
、![]() 、
、![]()
C.酸性:![]() 、
、![]() 、
、![]() D.稳定性:
D.稳定性:![]() 、
、![]() 、
、![]()
【答案】C
【解析】
A.金属性:Na>Mg>Al,元素的金属性越强,对应的最高价氧化物的水化物的碱性越强,则碱性:NaOH>Mg(OH)2>Al(OH)3,故A错误;
B.非金属性:Cl>Br>I,元素的非金属性越强,对应的简单氢化物的还原性越弱,则还原性:HI>HBr>HCl,故B错误;
C.同周期元素从左到右元素的非金属性逐渐增强,则非金属性:Cl>S>P,元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,则酸性:HClO4>H2SO4>H3PO4,故C正确;
D.非金属性:Cl>Br>I,元素的非金属性越强,对应的简单氢化物越稳定,则稳定性:HI<HBr<HCl,故D错误;
故答案为:C。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】某同学按照课本实验要求,用 50mL 0.50 mol·L-1 的盐酸与 50mL 0.50 mol·L-1 的NaOH溶液在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量计算反应热。下列 说法中,不正确的是( )
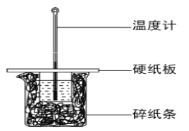
A.实验过程中有一定的热量损失
B.图中实验装置缺少环形玻璃搅拌棒
C.烧杯间填满碎纸条的主要作用是固定小烧杯
D.若将盐酸体积改为 60 mL,理论上所求反应热相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由下列实验及现象不能推出相应结论的是
选项 | 实验 | 现象 | 结论 |
A | 向添有KIO3的食盐中加入淀粉溶液、稀盐酸及KI | 溶液变蓝色 | 氧化性:IO3- >I2 |
B | 淀粉溶液在硫酸存在下加热一段时间后,再与新制的Cu(OH)2悬浊液混合,加热煮沸 | 无红色沉淀生成 | 淀粉没有水解 |
C | 常温下,向等体积、等浓度的NaHCO3和CH3COONa溶液中分别滴加2滴酚酞 | 两份溶液均变红,NaHCO3溶液红色更深 | 常温下的水解平衡常数:Kh(CH3COO-)<Kh(HCO3-) |
D | 常温时,用两支试管各取5 mL 0.1 mol/L 酸性KMnO4溶液,分别加入0.1 mol/L和0.2 mol/L H2C2O4溶液各2 mL | 两试管溶液均褪色,且加0.2 mol/L H2C2O4溶液的试管中褪色更快 | 其它条件不变,H2C2O4溶液的浓度越大,化学反应速率越大 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)有机物 用系统命名法命名:__。
用系统命名法命名:__。
(2)写出4—甲基—2—乙基—1—戊烯的结构简式:__。
(3)下列物质中属于同系物的是__。
①CH3CH2Cl②CH2=CHCl③CH3CH2CH2Cl④CH2ClCH2Cl⑤CH3CH2CH2CH3⑥CH3CH(CH3)2
A.①② B.①④ C.①③ D.⑤⑥
(4)0.1mol某烷烃燃烧,其燃烧产物全部被碱石灰吸收,碱石灰增39g。该烃的分子式为___;若它的核磁共振氢谱共有3个峰,则该烃可能的结构简式为___。(写出其中一种即可)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)在一定条件下,可逆反应:aA(g)+bB(g)![]() cC(g)+dD(g)达到平衡。
cC(g)+dD(g)达到平衡。
若其它条件不变,升高温度,则正反应速率________ (填“加快”或“减慢”,下同),逆反应速率________,重新达到平衡后c的质量增加,则正反应为_________(填“放热”或“吸热”)反应。
(2)把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是_______(填化学式)。
(3)pH = 3的醋酸和pH = 11的氢氧化钠溶液等体积混合后溶液呈________(填“酸”、“中”、“碱”)性,溶液中c(Na+) ______c(CH3COO-) (填“>”、“=”、“<”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用辉铜矿(主要成分为Cu2S,含少量Fe2O3、SiO2等杂质)制备Cu2(OH)2CO3,其工艺流程如下:
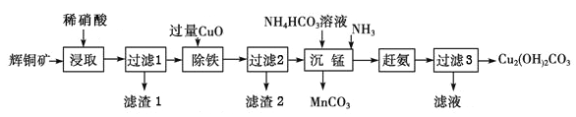
(1)“酸浸”过程中,将矿石粉碎,其目的是__________;加热能加快矿石粉“酸浸”速率,但温度不宜过高,其原因是__________。
(2)Cu2S和硝酸反应,其还原产物为NO。已知1 mol Cu2S完全反应时转移10 mol电子。写出该反应的离子方程式:_____________________。
(3)“除铁”中加入过量氧化铜发生反应的离子方程式为___________________。
(4)从过滤3得到的滤液中可提取一种肥料,它的化学式为__________;滤渣1的主要成分是__________(填化学式)。
(5)设计实验确认过滤2得到的滤液中是否有Fe3+:___________________________。
(6)取wg辉铜矿经上述流程转化,加入agCuO,滤渣2含bgCuO,最终得cmolCu2(OH)2CO3不考虑铜元素损失)。原辉铜矿含Cu2S的质量分数为____________。(用代数式表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,根据表中给出的10种元素,回答下列问题。
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
2 | C | N | O | F | Ne | |||
3 | Na | Al | P | S | Cl |
(1)单质的化学性质最不活沷的元素是__________;
(2)氧的原子结构示意图是__________;
(3)形成化合物种类最多的元素是__________;
(4)HF和H2O中,热稳定性较强的是__________;
(5)N和P中,原子半径较小的是__________;
(6)常温下,会在浓硫酸中发生钝化的金属是_________;
(7)元素最高价氧化物对应水化物中,碱性最强的是___(填化学式),酸性最强的是_____(填“H2SO4”或“ HClO4”);
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮及其化合物在工农业生产中具有重要作用.
(1)某小组进行工业合成氨![]() 的模拟研究,在1L密闭容器中,分别加入0.1molN2和0.3molH2,实验
的模拟研究,在1L密闭容器中,分别加入0.1molN2和0.3molH2,实验![]() 、
、![]() 、
、![]() 中
中![]() 随时间
随时间![]() 的变化如图所示.
的变化如图所示.
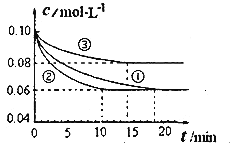
实验![]() 从开始到达到平衡状态的过程中,用
从开始到达到平衡状态的过程中,用![]() 表示的平均反应速率为 ___________.与实验
表示的平均反应速率为 ___________.与实验![]() 相比.实验
相比.实验![]() 所采用的实验条件可能为 ___________
所采用的实验条件可能为 ___________![]() 填字母
填字母![]() ,实验
,实验![]() 所采用的实验条件可能为 ___________
所采用的实验条件可能为 ___________![]() 填字母
填字母![]() .
.
![]() 增大压强
增大压强 ![]() 减小压强
减小压强 ![]() 升高温度
升高温度 ![]() 降低温度
降低温度 ![]() 使用催化剂
使用催化剂
(2)![]() 可用于处理废气中的氮氧化物,其反应原理为2NH3(g)+ NO(g)+ NO2(g)
可用于处理废气中的氮氧化物,其反应原理为2NH3(g)+ NO(g)+ NO2(g)![]() 2N2(g)+ 3H2O(g) △H<0,欲提高废气中氮氧化物的转化率,可采取的措施是 ___________
2N2(g)+ 3H2O(g) △H<0,欲提高废气中氮氧化物的转化率,可采取的措施是 ___________![]() 填字母
填字母![]()
![]() 升高温度
升高温度 ![]() 增大压强 c,增大
增大压强 c,增大![]() 的浓度
的浓度
(3)![]() 遇水发生水解反应,生成
遇水发生水解反应,生成![]() 的同时得到 ___________
的同时得到 ___________![]() 填化学式
填化学式![]() 是广谱高效消毒剂,制备原理为
是广谱高效消毒剂,制备原理为![]() 若转移1mol电子,则制取
若转移1mol电子,则制取![]() 的质量为 ___________.
的质量为 ___________.
(4)![]() 时,将
时,将![]() 的氨水与
的氨水与![]() 盐酸等体积混合,反应后溶液恰好显中性,则a ___________
盐酸等体积混合,反应后溶液恰好显中性,则a ___________![]() 填“
填“![]() ”、“
”、“![]() ”或“
”或“![]() ”
”![]() 用a、b表示
用a、b表示![]() 的电离平衡常数为 ___________.
的电离平衡常数为 ___________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下图所示的装置中,试管A、B中的电极为多孔的惰性电极;C、D为两个铂夹,夹在被Na2SO4溶液浸湿的滤纸条上,滤纸条的中部滴有一滴KMnO4;电源有a、b两极。若在A、B中充满0.01 mol/L 的KOH溶液后倒立于同浓度的KOH溶液的水槽中,断开K1,闭合K2、K3,通直流电,实验现象如下图所示,则:
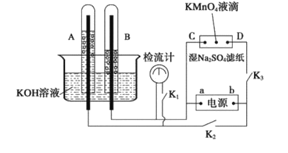
(1)断开K1,闭合K2、K3,通直流电,试管B中产生的气体为_________(填化学式)。
(2)在Na2SO4溶液浸湿的滤纸条中部的KMnO4处现象为_____________。
(3)断开K1,闭合K2、K3,通直流电较长一段时间后,KOH溶液pH变__________(填“变大”“变小”或“不变”)。
(4)电解一段时间后,A、B中均有气体包围电极。此时切断K2、K3,闭合K1,检流计有指数,此时该装置A试管中电极上发生的反应为_____________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com