
【题目】近年来,加“碘”食盐中添加较多的是碘酸钾(KIO3),碘酸钾在工业上可用电解法制取。以石墨和不锈钢为电极材料,以KI溶液为电解液,在一定条件下进行电解,反应的化学方程式为KI+3H2O![]() KIO3+3H2↑。下列有关说法不正确的是
KIO3+3H2↑。下列有关说法不正确的是
A. 加碘食盐不能使淀粉溶液变蓝
B. 电解时,石墨作阳极,不锈钢作阴极
C. 阳极的电极反应式为I-+3H2O+6e-=IO3-+6H+
D. 转移3 mol电子,理论上可制得107 g KIO3
【答案】C
【解析】
A.由于食盐中加入的是KIO3,没有加入I2,所以加碘食盐不能使淀粉溶液变蓝,A正确;
B.根据电池反应式知,阳极上I-失去电子生成IO3-,所以阳极应该为惰性电极石墨,阴极为铁,B正确;
C.电解时,阴极上氢离子放电生成氢气,阳极上碘离子放电生成KIO3,电极反应为:I--6e-+3H2O=IO3-+6H+,C错误;
D.根据反应的化学方程式为KI+3H2O![]() KIO3+3H2↑可知:每转移6mol e-时,理论上可制得KIO3的物质的量为1mol,即产生214g KIO3,所以转移3mol e-时,理论上可制得KIO30.5mol,即107g,D正确;
KIO3+3H2↑可知:每转移6mol e-时,理论上可制得KIO3的物质的量为1mol,即产生214g KIO3,所以转移3mol e-时,理论上可制得KIO30.5mol,即107g,D正确;
故合理选项是C。


科目:高中化学 来源: 题型:
【题目】下列有关实验装置及用途叙述完全正确的是

A. a装置检验消去反应后有丙烯生成
B. b装置检验酸性:盐酸>碳酸>苯酚
C. c装置用于实验室制取并收集乙烯
D. d装置用于实验室制硝基苯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组数据中,前者刚好是后者两倍的是 ( )
A. 2 mol H2O的摩尔质量和1 mol H2O的摩尔质量
B. 200 mL 1 mol·L-1氯化钙溶液中c(Cl-)和100 mL 2 mol·L-1氯化钾溶液中c(Cl-)
C. 64 g二氧化硫中氧原子数和标准状况下22.4 L一氧化碳中氧原子数
D. 20% NaOH溶液中NaOH的物质的量浓度和10% NaOH溶液中NaOH的物质的量浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z为原子序数依次增大的短周期主族元素,W和Y同族,X和Z同族,W和X可以形成能使湿润的紫色石蕊试纸变蓝的气体甲。下列说法正确的是
A. W和Y也能形成共价化合物B. 氧化物对应的水化物的酸性:![]()
C. 简单阳离子氧化性:![]() D. 甲分子中含有4对共用电子对
D. 甲分子中含有4对共用电子对
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,向容积固定为a L的密闭容器中充入1 mol X气体和2 mol Y气体,发生反应X(g)+2Y(g)![]() 2Z(g),此反应达到平衡状态的标志是
2Z(g),此反应达到平衡状态的标志是
A. 容器内气体密度不随时间变化
B. 容器内气体的平均相对分子质量不随时间变化
C. 容器内X、Y、Z的浓度之比为1∶2∶2
D. 消耗0.1 mol X的同时生成0.2 mol Z
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校探究性学习小组用已部分生锈的废铁屑制作印刷电路板的腐蚀剂,并回收铜。探究过程如下,请回答下列问题:

(1)步骤①的作用是清洗废铁屑表面的油污,其中加热的目的是____________。
(2)写出步骤②中生成![]() 的离子方程式______________________。(写一个即可)
的离子方程式______________________。(写一个即可)
(3)步骤③中“氯气”不引入杂质但有毒,可以用___________代替(填化学式)。
(4)若溶液B中只含有![]() 而不含
而不含![]() ,可证明该事实的实验操作是__________。
,可证明该事实的实验操作是__________。
(5)步骤⑤产生金属铜的化学方程式为______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相对分子质量为 M 的气态化合物 V L(标准状况),溶于 m g 水中,得到质量分数为 w、物质的量浓度为 c mol/L、密度为 ρg/mL 的溶液,下列说法正确的是
A.相对分子质量![]() B.物质的量浓度
B.物质的量浓度![]()
C.溶液的质量分数![]() D.溶液密度
D.溶液密度![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环之间共用一个碳原子的化合物称为螺环化合物,螺[2,2]戊烷(![]() )是最简单的一种。下列关于该化合物的说法错误的是
)是最简单的一种。下列关于该化合物的说法错误的是
A. 与环戊烯互为同分异构体
B. 二氯代物超过两种
C. 所有碳原子均处同一平面
D. 生成1 molC5H12至少需要2 molH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(一)镓、硒、硅等元素的化合物是生产第三代太阳能电池的重要材料。已知:SeO2在常温下是白色的晶体,熔点为340-350℃,则SeO2晶体属于____晶体,SeO2中Se原子采取的杂化类型为___。
(二)A、X、Y、Z、W、M、G等原子序数一次增大的前四周期元素
元素 | 相关信息 |
A | 原子核外电子总数与其周期数相同 |
X | 其羞态原子的L层中有3个未成对电子 |
Y | 荃态原子的2p轨道上有一个电子的自旋方向与2p轨道上其它电子的自旋方向相反 |
Z | 原子核外p电子数比s电子数多l个 |
W | 原子的第一至第四电离能(kJ·mol-1)分别是:I1=578,I2=1817 I3=2745 I4=11575 |
M | 元素的主族数与周期数相差4 |
G | 其基态原子最外层电子数为1,其余各电子层均充满电子 |
(1)画出W基态原子的核外电子排布图______。
(2)A2Y的VSEPR模型名称为____。
(3)已知为X2Y分子中Y原子只与一个X原子相连,请根据等电子原理,写出X2Y的电子式____。
(4)X、G形成的某种化合物的晶胞结构如图所示,则其化学式为______。
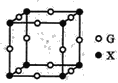
(5)已知Z和M形成的化合物的晶体密度为pg·cm-3,阿伏加德罗常效为NA,该晶体中两个距离最近的Z离子中心间距离为_____cm。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com