
【题目】某有机物的结构简式为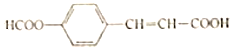 有关该化合物的叙述不正确的是( )
有关该化合物的叙述不正确的是( )
A.所有碳原子可能共平面
B.可以发生水解、加成和酯化反应
C.1mol该物质最多消耗2molNaOH
D.苯环上的二溴代物同分异构体数目为4种
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W 四种物质有如下相互转化关系(其中 Y、Z 为化合物,未列出反应条件)。

(1)若实验室经常用澄清石灰水来检验 X 的燃烧产物,W 的用途之一是计算机芯片,W 在周期表中的位置为 ___________,Y 的用途有 _________,写出Y与NaOH 溶液反应的离子方程式 _________。
(2)若 X、W 为日常生活中常见的两种金属,且 Y 常用作红色油漆和涂料,则该反应的化学方程式为___________。
(3)若 X 为淡黄色粉末,Y 为生活中常见液体,则:
①X 的电子式为 _______________,该反应的化学方程式为 ____________,生成的化合物中所含化学键类型有 ________________________。
② 若 7.8 克 X 物质完全反应,转移的电子数为 ___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用软锰矿(只含MnO2和MnO)、H2SO4(过量)和FeS2制备MnSO4·H2O的流程如下(已知流程中的FeS2、FeSO4、MnO2、MnO均完全反应):
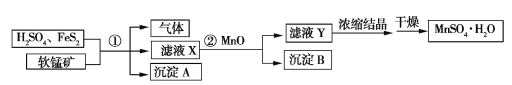
(1)已知①中只有三个反应,其中两个反应是
MnO+H2SO4MnSO4+H2O
FeS2+H2SO4FeSO4+H2S↑+S↓
完成第三个反应:
___MnO2+___FeSO4+___ ____________MnSO4+___ _________+___ _________
(2)沉淀A、B的化学式分别是____________________、__________________。
(3)滤液X中的溶质有__________;实验室中浓缩滤液Y时使用的玻璃仪器有___________________。
(4)若得到的沉淀A的质量和MnSO4·H2O的质量分别为96.0 g、321.1 g,②中加入的MnO为0.1 mol,则理论上软锰矿中MnO2和MnO的物质的量之比为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学欲用98%的浓H2SO4(ρ=1.84g/cm3)配制成500mL 0.5mol/L的稀H2SO4
(1)填写下列操作步骤:
①所需浓H2SO4的体积为____。
②如果实验室有10mL、20mL、50mL量筒,应选用___mL量筒量取。
③将量取的浓H2SO4沿玻璃棒慢慢注入盛有约100mL水的___里,并不断搅拌,目的是___。
④立即将上述溶液沿玻璃棒注入____中,并用50mL蒸馏水洗涤烧杯2~3次,并将洗涤液注入其中,并不时轻轻振荡。
⑤加水至距刻度___处,改用__加水,使溶液的凹液面正好跟刻度相平。盖上瓶塞,上下颠倒数次,摇匀。
(2)请指出上述操作中一处明显错误:____。
(3)误差(填偏高、偏低、无影响)
①操作②中量取时发现量筒不干净,用水洗净后直接量取,所配溶液浓度将___;
②问题(2)的错误操作将导致所配制溶液的浓度___;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是( )
A. 铁与稀硫酸反应:2Fe+6H+=2Fe3++3H2↑
B. 用氢氧化钠溶液吸收过量二氧化碳气体:CO2 +OH-=HCO3-
C. 制备氢氧化铁胶体:Fe3++3OH--Fe(OH)3↓
D. 醋酸除去水垢:2H+ +CaCO3=Ca2++CO2↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.相同条件下,N2和O3混合气体与等体积的N2所含的原子数相同
B.等物质的量的CH5+和OH-所含电子数相等
C.常温常压下,28gCO与22.4LO2所含分子数相等
D.16gCH4与18gNH4+所含质子数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镍具有良好的导磁性和可塑性,主要用于制作合金及催化剂。请回答下列问题
(1)基态镍原子的价电子排布图为____,同周期元素中基态原子与镍具有相同未成对电子的还有____种。
(2)四羰基合镍是一种无色挥发性液体,熔点-25℃,沸点43℃。则四羟基合镍中σ键和π键数目之比为___三种组成元素按电负性由大到小的顺序为____。
(3)[Ni(NH3)
4]SO4中N原子的杂化方式为____,写出与SO42-互为等电子体的一种分子和一种离子的化学式____,____;[Ni(
NH3)4]SO4中H-N-H键之间的夹角___(填“>”“<”或“=”)NH3分子中H-N-H键之间的夹角。
(4)已知NiO的晶体结构(如图1),可描述为:氧原子位于面心和顶点,氧原子可形成正八面体空隙和正四面体空隙,镍原子填充在氧原子形成的空隙中,则NiO晶体中原子填充在氧原子形成的____体空隙中,其空隙的填充率为____。
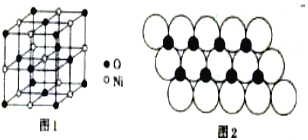
(5)一定温度下,NiO晶体可分散形成“单分子层”,O2-作单层密置排列,Ni2+填充O2-形成的正三角形空隙中(如图2),已知O2-的半径为αm,每平方米面积上分数的NiO的质量为___g。(用a、NA表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用除去表面氧化膜的细铝条紧紧缠绕在温度计上(如图),将少许硝酸汞溶液滴到铝条表面,置于空气中,很快铝条表面产生“白毛”,且温度明显上升。下列分析错误的是

A.Al和O2化合放出热量B.硝酸汞是催化剂
C.涉及了:2Al+3Hg2+→2Al3++3HgD.“白毛”是氧化铝
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将水分解制得氢气的一种工业方法是“硫﹣碘循环法”,依次涉及下列三步反应:
I.SO2+2H2O+I2=H2SO4+2HI
II.2HI(g)H2(g)+I2(g)
III.2H2SO4=2SO2+O2+2H2O
(1)一定温度下,向5L恒容密闭容器中加入1molHI,发生反应II,H2物质的量随时间的变化如图所示。0~2min内的平均反应速率v(HI)=___。相同温度下,若起始加入的HI改为2mol,反应达平衡时H2的量为___mol。
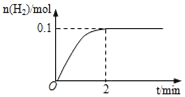
(2)分析上述反应,下列判断错误的是___(填写选项编号,只有一个正确选项)。
a.三步反应均为氧化还原反应
b.循环过程中产生1molH2,同时产生1molO2
c.在整个分解水的过程中SO2和I2相当于催化剂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com