
【题目】某研究性学习小组的甲、乙同学分别设计了以下实验来验证元素周期律。
(Ⅰ)甲同学在 a、b、c 三只烧杯里分别加入 50 mL 水,再分别滴加几滴酚酞溶液,依次加入 大小相近的锂、钠、钾块,观察现象。
①甲同学设计实验的目的是______
②反应最剧烈的烧杯是______(填字母);
③写出 b 烧杯里发生反应的离子方程式______
(Ⅱ)乙同学设计了下图装置来探究碳、硅元素的非金属性强弱,根据要求完成下列各小题
(1)实验装置:

(2)实验步骤: 连接仪器、______、加药品后,打开 a、然后滴入浓硫酸,加热。
(3)问题探究:(已知酸性强弱:亚硫酸>碳酸)
①铜与浓硫酸反应的化学方程式是______,装置 E 中足量酸性 KMnO4 溶液 的作用是______。
②能说明碳元素的非金属性比硅元素非金属性强的实验现象是______;
③试管 D 中发生反应的离子方程式是______。
【答案】验证锂、钠、钾的金属性强弱; c 2Na+2H2O=2Na++2OH+ H2↑ 检查装置气密性 Cu+2H2SO4(浓)![]() CuSO4+ 2H2O+ SO2↑ 除去CO2中混有的SO2 盛有硅酸钠溶液的试管出现白色沉淀; SO2+ HCO3= CO2+ HSO3
CuSO4+ 2H2O+ SO2↑ 除去CO2中混有的SO2 盛有硅酸钠溶液的试管出现白色沉淀; SO2+ HCO3= CO2+ HSO3
【解析】
乙同学设计实验探究碳、硅元素的非金属性强弱。先用浓硫酸和铜在加热条件下制备二氧化硫气体,通入D试管与饱和碳酸氢钠反应生成二氧化碳,混合气体通入试管E,除去混有的二氧化硫,剩余的二氧化碳通入试管F与硅酸钠溶液反应,会出现白色沉淀。该实验需要改良的地方尾气处理装置,以及防干扰装置(防止空气中的二氧化碳进入装置F,干扰实验结构,可以加一个球星干燥管,内盛放碱石灰)。
(Ⅰ)①由某研究性学习小组设计实验验证元素周期律可得,甲同学设计的实验目的是:验证锂、钠、钾的金属性强弱;
②金属性:K>Na>Li,金属性越强,单质与水反应越剧烈,故反应最剧烈的烧杯是c;’
③b 烧杯里发生反应的离子方程式:2Na+2H2O=2Na++2OH+ H2↑;
(Ⅱ)(2)实验步骤: 有气体参与反应,先连接仪器、检查装置气密性、加药品(先加固体,后加液体)后,打开 a、然后滴入浓硫酸,加热。
(3)①铜与浓硫酸反应的化学方程式是:Cu+2H2SO4(浓)![]() CuSO4+ 2H2O+ SO2↑;根据分析,高锰酸钾的作用是除去CO2中混有的SO2;
CuSO4+ 2H2O+ SO2↑;根据分析,高锰酸钾的作用是除去CO2中混有的SO2;
②非金属性越强,最高价氧化物的水化物酸性越强,若碳酸可以制得硅酸,则可以证明碳酸强于硅酸,从而可以证明二者非金属性的强弱,故能说明碳元素的非金属性比硅元素非金属性强的实验现象是:盛有硅酸钠溶液的试管出现白色沉淀;
③试管D用SO2与NaHCO3制备CO2,反应的离子方程式:SO2+ HCO3= CO2+ HSO3。


科目:高中化学 来源: 题型:
【题目】Y是合成香料、医药、农药及染料的重要中间体,可由X在一定条件下合成:

下列说法不正确的是
A. Y的分子式为C10H8O3
B. 由X制取Y的过程中可得到乙醇
C. 一定条件下,Y能发生加聚反应和缩聚反应
D. 等物质的量的X、Y分别与NaOH溶液反应,最多消耗NaOH的物质的量之比为3∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在测定某铁矿石中的含铁量时,可准确称取2.0g铁矿石溶解在酸溶液里,然后把其中的Fe3+还原成Fe2+,制得100mL待测液,再取出10mL该待测液于锥形瓶中,然后用0.020mol·L-1的KMnO4标准溶液进行滴定,发生反应的离子方程式如下:Fe2++MnO4-+ 8H+ = 5Fe3++Mn2++4H2O , 滴定结果平均消耗KMnO4溶液的体积刚好等于下图中所示的消耗KMnO4溶液的体积,试回答下列问题:
(1)把待测液中的Fe3+还原成Fe2+,应选用下列试剂____________, 充分反应再进行过滤洗涤,将洗涤液并入待测液中。
A.氯水 B. H2O2 C. Fe屑 D. Cu
(2)滴定开始和结束时,滴定管中的液面如图所示,则终点读数为______________mL

滴定过程中,用左手控制滴定管活塞,边滴边摇动锥形瓶,眼睛应注视______________________________,直至滴定终点。判断到达终点的现象是___________________________________________________________________________________
(3)下列操作会使测得样品中铁的质量分数偏高的是__________
A.滴定管用蒸馏水洗涤后,直接加入高锰酸钾标准溶液进行滴定。
B.锥形瓶用蒸馏水洗涤后,水未倒尽,就加入待测液进行滴定。
C.记录测定结果时,滴定前仰视液凹面最低处,滴定到达终点时又俯视读数。
(4)如果矿石是用盐酸溶解配制成待测液,则测定的结果矿石中含铁量______________(填偏高、偏低、无影响),原因是_________________________________________
(5)矿石中含铁的质量分数为 _________________ (已知铁的原子量为56)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】物质的类别和核心元素的化合价是研究物质性质的两个重要角度。请根据如图所示,回答下列问题:

(1)Y的化学式为__________________
(2)气体X和气体Y混合产生淡黄色的烟,写出该反应的化学方程式________。
(3)欲制备Na2S2O3,从氧化还原角度分析,合理的是______(填序号)。
a.Na2S +S b.Na2SO3+S c.Na2SO3+Na2SO4 d.SO2+Na2SO4
(4)如图为铜丝与W的浓溶液反应并验证其产物性质的实验装置。

①反应①中体现的浓硫酸的化学性质是________。想要立即终止①的反应,最恰当的方法是__________。
a.上移铜丝,使其脱离溶液 b.撤去酒精灯 c.拔去橡胶塞倒出溶液
②装置④中品红溶液的作用是________,棉花团的作用__________。
③反应停止后,待装置冷却,把③取下后向其中加入氯水,观察到白色沉淀生成,写出相关反应的离子方程式__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将4molSO2和2mol O2在2L的恒容密闭容器中混合,并在一定条件下发生如下反应: 2SO2(g)+ O2(g)![]() 2SO3(g),若经2s后测得SO3的浓度为0.6mol/L。下列说法中不正确的是
2SO3(g),若经2s后测得SO3的浓度为0.6mol/L。下列说法中不正确的是
A. 用SO2表示反应的平均速率为0.3mol/( L·s)
B. 用O2表示反应的平均速率为0.15mol/(L.s)
C. 2s时O2的浓度为0.7mol/L
D. 2s时SO2的转化率为70%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化镁纯品为无色单斜晶体,工业品通常呈黄褐色,有苦咸味。该物质可以形成六水合物,即六水氯化镁(MgCl2·6H2O),以下流程为由某混合物,制取纯净MgCl2·6H2O的生产过程:

已知:在本流程中,
Fe3+ | Fe2+ | Al3+ | Mg2+ | |
开始沉淀pH | 1.5 | 6.5 | 3.3 | 8.4 |
完全沉淀pH | 4.1 | 9.7 | 5.5 | 10.9 |
试回答下列问题:
(1)操作1所需玻璃仪器为____________________。
(2)流程中加入试剂2调节pH的范围是________;加入试剂2能形成沉淀的原因是___________________。
(3)操作3为加入足量的盐酸,然后经过___________、____________,过滤,洗涤,干燥;在操作不当的情况下,若MgCl2·6H2O受热则会发生水解形成碱式盐,则该反应的化学方程式为____________________。
(4)若25℃下,Ksp[Mg(OH)2]=4×10-12,则该温度下,将Mg(OH)2溶于水形成饱和溶液,则其饱 和溶液的pH=_________。(已知:lg5=0.7)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图用分类法表示了一些物质或概念之间的从属或包含关系,不正确的是( )
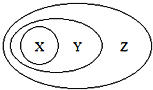
X | Y | Z | |
A | NaAlO2 | 盐 | 纯净物 |
B | 胶体 | 分散系 | 混合物 |
C | Al2O3 | 两性氧化物 | 氧化物 |
D | 单质参与反应 | 置换反应 | 氧化还原反应 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】t℃时CuSO4的溶解度是Sg,其饱和溶液密度为dg·cm-3,物质的量浓度为cmol·L-1。向足量饱和溶液中加入mg无水CuSO4或蒸发掉ng水后恢复t℃,均能获得Wg胆矾晶体,下列关系式正确的是
A. c=![]() mol·L-1 B. S=
mol·L-1 B. S=![]() g
g
C. m=![]() g D. W=
g D. W=![]() g
g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)下列几组物质中,互为同位素的是_______,互为同素异形体的是_______,互为同系物的是_______,互为同分异构体的是_______,属于同种物质的是_______。(用序号填空)
①O2 和O3 ②35Cl 和 37Cl ③CH3CH3 和 CH3CH2CH3④ 和
和 ⑤CH3(CH2)2CH3 和(CH3)2CHCH3
⑤CH3(CH2)2CH3 和(CH3)2CHCH3
(2)硫酸的性质有:A.高沸点;B.酸性;C.吸水性;D.脱水性;E.强氧化性。在下列硫酸的用途或化学反应中,硫酸可能表现上述的一个或者多个性质,试用字母填空:
①实验室干燥氢气_____;
②浓硫酸与金属铜的反应_____;
③浓硫酸使蔗糖变黑,且有刺激性气味的气体产生_____
(3)已知氯有 2 种常见同位素原子 35Cl、37Cl,氢有 3 种常见的同位素原子 H、D、T,氯气与氢气形成的氯化氢分子的相对分子质量可能有_____种。
(4)质量相同的 H2 16O 和 D2 16O 所含质子数之比为_____
(5)①CO2 ②CH3CH3 ③CaBr2 ④H2O2 ⑤NH4Cl ⑥AlCl3 ⑦NaOH ⑧NH3 ⑨Na2O2试用以上编号填空:既有极性键,又有非极性键的是_____;属于离子化合物的是_____;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com