
【题目】同温同压下,体积为VL两容器分别充满了CO气体和CO2气体,下列有关说法不正确的是( )
A.两容器含有气体分子数目相同
B.两容器气体密度之比为:7:11
C.两容器中所含氧原子个数之比为:1:2
D.两容器所含气体的物质的量均为:![]() mol
mol
科目:高中化学 来源: 题型:
【题目】化合物M是二苯乙炔类液晶材料的一种,最简单的二苯乙炔类化合物是![]() 。以互为同系物的单取代芳烃A、G为原料合成M的一种路线(部分反应条件略去)如下:
。以互为同系物的单取代芳烃A、G为原料合成M的一种路线(部分反应条件略去)如下:

回答下列问题:
(1)A的分子式为________;
(2)D中含有的官能团是________,分子中最多有________个碳原子共平面;
(3)①的反应类型是________,③的反应类型是________;
(4)⑤的化学方程式为________;
(5)B的同分异构体中能同时满足如下条件:a.苯环上有两个取代基,b.能发生银镜反应,共有______种(不考虑立体异构),其中核磁共振氢谱为5组峰,且峰面积比为6∶2∶2∶1∶1的是________(写结构简式);
(6)参照上述合成路线,设计一条由苯乙烯和甲苯为起始原料制备![]() 的合成路线:___。(其他试剂任用)(合成路线常用的表示方法:起始原料A
的合成路线:___。(其他试剂任用)(合成路线常用的表示方法:起始原料A![]() B……
B……![]() 目标产物)。
目标产物)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.(1)直接排放煤燃烧产生的烟气会引起严重的环境问题。
①假设用酸性高锰酸钾溶液吸收煤燃烧产生的SO2,该过程中高锰酸根被还原为Mn2+,请写出该过程的离子方程式______________。
②将燃煤产生的二氧化碳加以回收,可降低碳的排放。左图是通过人工光合作用,以CO2和H2O为原料制备HCOOH和O2的原理示意图,a电极名称:_____________(填“正极”或“负极”),b电极的反应式:________________________。

(2)如果采用NaClO、Ca(ClO)2作吸收剂,也能得到较好的烟气脱硫效果。
已知下列反应:
SO2(g)+2OH-(aq) ==SO32-(aq)+H2O(l) ΔH1
ClO-(aq)+SO32-(aq) ==SO42-(aq)+Cl-(aq) ΔH2
CaSO4(s)==Ca2+(aq)+SO42-(aq) ΔH3
则反应SO2(g)+ Ca2+(aq)+ ClO-(aq) +2OH-(aq) = CaSO4(s) +H2O(l) +Cl-(aq)的ΔH=_____。
II.(3)FeO42-在水溶液中的存在形态如图所示。

①若向pH=10的这种溶液中加硫酸至pH=2,HFeO4-的分布分数的变化情况是__________。
②若向pH=6的这种溶液中滴加KOH溶液,则溶液中含铁元素的微粒中,_________转化为_________(填微粒符号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应属于加成反应的是( )
A. CH3CH==CH2+Br2→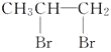
B. ![]() +HNO3
+HNO3![]()
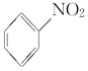 +H2O
+H2O
C. 2CH3CH2OH+O2![]() 2CH3CHO+2H2O
2CH3CHO+2H2O
D. CH3COOH+CH3CH2OH![]() CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向100mL0.lmol/LNH4Cl溶液中,逐滴滴加0.1mol/LNaOH溶液。NH4+和NH3H2O的变化趋势如图所示(不考虑生成NH3,已知NH3H2O的kb=1.8![]() 10-5),下列说法正确的是( )
10-5),下列说法正确的是( )

A.a=0.005
B.在M点时,n(H+)—n(OH—)=(0.005—a)mol
C.随着NaOH溶液的滴加, 不断增大
不断增大
D.当n((NaOH)) =0.01 mol 时,c ((NH3H2O)![]() c (Na+)
c (Na+)![]() c (OH-)
c (OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】世界能源消费依靠化学技术,作为燃料的H2通常来自水煤气。回答下列问题:
(1)己知:① C(s)+H2O(g)=CO(g)+H2(g)△H=akJ/mol②2C(s)+O2(g)=2CO(g) △H= -220 kJ/mol③2H2O(g)=2H2(g)+O2(g) △H=+480 kJ/mol,则 a=_____kJ/mol。
(2)某实验小组在实验室模拟反应C(s) +H2O (g)![]() CO (g) +H2 (g)能够说明该反应达到平衡状态的是____。
CO (g) +H2 (g)能够说明该反应达到平衡状态的是____。
a. v逆(H2O)=v正(CO) b.容器中物质的总质量不发生变化
c. n (H2O):n (H2)=1:1且不再改变 d.恒容容器中混合气体密度不变
(3)一定温度下,在2L盛有足量炭粉的恒容密闭容器中通入0.8molH2O发生反应①,6min时生成0.7 gH2则6 min内以CO表示的平均反应速率为 ______mol/Lmin-1 (保留2位有效数字)。
(4)燃料气中CO需氧化为CO2与氢气进行分离,使用CuO/CeO2做催化剂,并向其中加入不同的酸(HIO3 或H3PO4)后,CO的转化率随温度的变化如图所示。
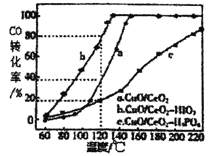
①加入H3PO4__________(填“促进”或,抑制”)CuO/CeO2的催化。
②CeO2可由草酸鋪[Ce2(C2O4)3]在空气中灼烧制备,同时只产生一种气体,写出该反应的化学方程式_____。
③恒温恒压下,在温度为120°C,催化剂为CuO/CeO2HIO3条件下反应,若起始时燃料气流速为1800mLmin-1,其中CO的体积分数为0.68%,则反应0.5h后剩余气体中CO的体积为__mL。
(5)有人将合成氨反应设计成原电池,装置如图所示。
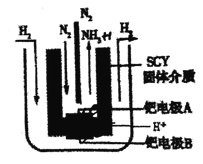
①正极反应式为 _______。
②己知该原电池的标准电动势![]() ,25°C时反应的平衡常数K与
,25°C时反应的平衡常数K与![]() 之间的关系为
之间的关系为![]() (n为原电池反应转移的电子数),则合成氨反应(N2 +3H2
(n为原电池反应转移的电子数),则合成氨反应(N2 +3H2![]() 2NH3)的平衡常数K为 ______(用含a的代数式表示,不需要化简)。
2NH3)的平衡常数K为 ______(用含a的代数式表示,不需要化简)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)写出下列物质在水溶液中的电离方程式:
①Ba(OH)2:_________;
②KHSO4:___________;
(2)写出下列物质在水溶液中的离子方程式:
③HNO3与醋酸钠(CH3COONa):____________;
④Na2CO3与澄清石灰水反应:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NaNO2可用作食品添加剂。测定粗产品中NaNO2的含量。称取m g粗产品,溶解后配制成250 mL溶液。取出25.00mL溶液,用cmolL-1酸性KMnO4溶液平行滴定三次,平均消耗的体积为V mL。
已知:2MnO4-+6H+ +5NO2-=5NO3-+2Mn2++3H2O
(1)配制溶液时,需使用的玻璃仪器除烧杯、玻璃棒外,还有___(填字母)。
A. 250 mL容量瓶 B. 量筒 C. 胶头滴管 D. 锥形瓶
(2)用____(填“酸式”或“碱式”)滴定管盛放高锰酸钾溶液。
(3)该实验___(填“需要”或“不需要”)加入指示剂。当观察到___时,滴定达到终点。
(4)粗产品中NaNO2的质量分数为____(用代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,关闭活塞,向甲、乙两刚性密闭容器中分别充入1molA、2molB,此时甲、乙的容积均为2L(连通管体积忽略不计)。在T℃时,两容器中均发生下述反应:A(g)+2B(g)![]() 2C(g)+3D(g)△H<0。达平衡时,乙的体积为2.6L,下列说法正确的是( )
2C(g)+3D(g)△H<0。达平衡时,乙的体积为2.6L,下列说法正确的是( )
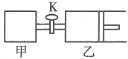
A. 甲中反应的平衡常数小于乙
B. 当乙中A与B的体积分数之比为1:2时,反应达到平衡状态
C. 平衡时甲容器中A的物质的量小于0.55mol
D. 若打开活塞K,达平衡时乙容器的体积为3.2L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com