
【题目】现有以下物质:①盐酸;②二氧化碳;③高锰酸钾;④铝;⑤自来水;⑥石墨;⑦液氧;⑧淀粉;⑨纯碱
(1)以上物质能导电的是_______________
(2)以上物质属于电解质的是___________
(3)以上物质属于非电解质的是_________
(4)从上述物质选出一种或几种进行反应,写出既是氧化还原反应,又是化合反应的化学方程式:____________。
【答案】①④⑤⑥ ③⑨ ②⑧ ![]() (点燃条件下或常温下均可)或
(点燃条件下或常温下均可)或![]()
【解析】
(1)含可自由移动电子或离子的物质能导电,据此回答;
(2) 在水溶液中或熔融状态下能导电的化合物叫做电解质,常见的酸、碱、盐大多是电解质,据此回答;
(3) 蔗糖、酒精等化合物,无论是在水溶液中还是在熔融状态下均以分子形式存在,因而不能导电,这样的化合物叫做非电解质,葡萄糖、淀粉、油脂等有机化合物大多是非电解质,据此回答;
(4) 石墨和氧气或者铝和氧气的反应符合,据此写化学方程式;
(1)铝、石墨因含可自由移动电子能导电,盐酸是电解质溶液,因含可自由移动的离子能导电,水是极弱的电解质,能导电;
答案为:①④⑤⑥;
(2) 在水溶液中或熔融状态下能导电的化合物叫做电解质,常见的酸、碱、盐大多是电解质,提供的物质中③高锰酸钾⑨纯碱都是盐,都属于电解质;
答案为:③⑨;
(3) 蔗糖、酒精等化合物,无论是在水溶液中还是在熔融状态下均以分子形式存在,因而不能导电,这样的化合物叫做非电解质,葡萄糖、淀粉、油脂等有机化合物大多是非电解质,虽然二氧化碳的水溶液能导电,但离子由碳酸电离产生而二氧化碳自身不直接电离出离子,故二氧化碳属于非电解质;
答案为:②⑧;
(4) 石墨和氧气或者铝和氧气的反应符合,则化学方程式为![]() (点燃条件下或常温下均可)或
(点燃条件下或常温下均可)或![]() ;
;
答案为:![]() (点燃条件下或常温下均可)或
(点燃条件下或常温下均可)或![]() 。
。


科目:高中化学 来源: 题型:
【题目】以高硫铝土矿(主要成分为Al2O3、Fe2O3,还含有少量FeS2)为原料,生产氧化铝并获得Fe3O4的部分工艺流程如图,下列叙述错误的是( )
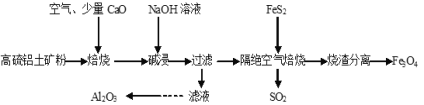
A.烧渣分离可以选择用磁铁将烧渣中的Fe3O4分离出来
B.隔绝空气焙烧时理论上反应消耗的n(FeS2)∶n(Fe2O3)=1∶5
C.向滤液中通入过量CO2、过滤、洗涤、灼烧沉淀可制得Al2O3
D.加入CaO可以减少SO2的排放同时生成建筑材料CaSO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组欲测定室温下(25 ℃、101 kPa)的气体摩尔体积。该小组设计的简易实验装置如图所示:
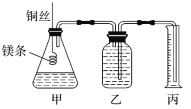
该实验的主要操作步骤如下:
①用已知浓度的浓盐酸配制100mL 1.0mol·L-1的盐酸(需要用到的仪器有量筒、烧杯、__________;
②用10mL的量筒量取8.0mL 1.0mol·L-1的盐酸加入锥形瓶中;
③准确称取a g已除去表面氧化膜的镁条,并系于铜丝末端,为使HCl全部参加反应,a的数值至少为_____;
④往广口瓶中装入足量水,按上图连接好装置,检查装置的气密性;
⑤反应结束后待体系温度恢复到室温,读出量筒中水的体积为V mL。
请回答下列问题:
(1)步骤①中,配制100mL 1.0mol·L-1的盐酸时,下列会使所配制溶液的浓度偏小的操作有____(填字母)。
A 用量筒量取浓盐酸时,俯视量筒的刻度线
B 容量瓶未干燥即用来配制溶液
C 浓盐酸在烧杯中稀释时,搅拌时间过长
D 定容完成后,将容量瓶倒置摇匀后,发现液面低于刻度线未做处理
E 在容量瓶中定容时俯视容量瓶刻度线
F 烧杯中有少量水
G 未冷却至室温即定容
(2)实验步骤⑤中应选用的量筒规格是_______
(3)读数时需要注意(至少写两点):______。
(4)忽略水蒸气影响,在该条件下测得气体摩尔体积的计算式为Vm=___L·mol-1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学电源在日常生活和高科技领域中都有广泛应用。下列说法正确的是
A.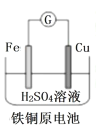 Fe 棒为负极,电极反应为 Fe-3e-= Fe3+
Fe 棒为负极,电极反应为 Fe-3e-= Fe3+
B.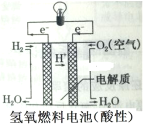 能够给用电器提供电势差,是由于两个电极上有得失电子能力不同的氢气和氧气
能够给用电器提供电势差,是由于两个电极上有得失电子能力不同的氢气和氧气
C. 锌筒作负极,发生还原反应,锌筒会变薄
锌筒作负极,发生还原反应,锌筒会变薄
D.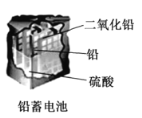 使用一段时间后硫酸铅沉淀在电极板上,溶液酸性减弱,导电能力下降
使用一段时间后硫酸铅沉淀在电极板上,溶液酸性减弱,导电能力下降
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】国际计量大会新修订了阿伏加德罗常数(NA=6.02214076×1023mol1),并于2019年5月20日正式生效。下列有关NA说法正确的是
A.22.4LCH2=CHCH3分子中含碳碳双键的数目为NA
B.1mol羟基(﹣OH)所含的电子总数为9NA
C.常温常压下,14g聚乙烯含有原子总数为3NA
D.64 g S2和S8混合物中含硫原子总数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯甲醛(微溶于水、易溶于有机溶剂,密度约等于水的密度)在碱性条件下发生歧化反应可以制备苯甲醇(在水中溶解度不大、易溶于有机溶剂,密度约等于水的密度)和苯甲酸。反应原理如下:2C6H5CHO+NaOH→C6H5CH2OH+C6H5COONa、C6H5COONa+HCl→C6H5COOH+NaCl,有关物质物理性质如表:
苯甲醛 | 苯甲醇 | 苯甲酸 | 苯 | |
沸点/℃ | 178 | 205 | 249 | 80 |
熔点/℃ | 26 | ﹣15 | 12 | 5.5 |
苯甲酸在水中的溶解度 | ||
17℃ | 25℃ | 100℃ |
0.21 g | 0.34 g | 5.9 g |
实验流程如下:
(1)第①步需连续加热1小时(如图1),其中加热和固定装置未画出。若将仪器B改为仪器C,效果不如B,说明原因________。

(2)操作中有关分液漏斗的使用不正确的是___。
A.分液漏斗在使用之前必须检查是否漏水
B.分液漏斗内的液体不能过多,否则不利于振荡
C.充分振荡后将分液漏斗置于铁架台上静置,分层后立即打开旋塞进行分液
D.分液时等下层液体放完后立即关闭旋塞,换一个烧杯再打开旋塞使上层液体流下
(3)操作③用沸水浴加热蒸馏,再进行操作④(如图2),收集___℃的馏分。图2中有一处明显错误,正确的应改为_______。
(4)抽滤时(如图3)烧杯中苯甲酸晶体转入布氏漏斗时,杯壁上还粘有少量晶体,用___冲洗杯壁上残留的晶体,抽滤完成后洗涤晶体。
(5)用电子天平准确称取0.244 0 g苯甲酸样品于锥形瓶中,加100 mL蒸馏水溶解(必要时可以加热),再用0.100 0 molL﹣1的标准NaOH溶液滴定,共消耗NaOH溶液19.20 mL,则苯甲酸样品的纯度为___%(保留4位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】填写甲烷与氯气光照时的取代反应现象
(1)试管内气体________________________
(2)试管壁出现_________________________
(3)试管中有少量_________________________
(4)水面___________,但____________(填“充满”“ 不充满”)整个试管。
(5)产物中共有_______ 种,其中____________的结构是正四面体(写名称)写出第一步取代反应:______________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】日本产业技术综合研究所发布的锂空气电池的设计构思是负极采用金属锂条,中间设有用于隔开正极和负极的锂离子固体电解质,正极的水性电解液使用碱性水溶性凝胶,与由微细化碳和廉价氧化物催化剂形成的正极组合,既可以用作充电电池也可用作燃料电池使用,结构如图所示。下列有关该锂空气电池说法不正确的是( )
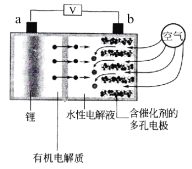
A.电池放电时,Li+穿过隔膜向b极移动得到LiOH溶液
B.放电时,外电路的电子由a经外电路流向b
C.充电时,a电极的电极反应为:Li+ + e- ═ Li
D.放电时,b极发生的电极反应为O2 - 4e- + 2H2O ═ 4OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求回答下列问题:
(1)在200℃、101kPa时,0.5molH2(g)与足量I2(g)完全反应放出7.45kJ的热量,该反应的热化学方程式表示为____。
(2)根据键能数据估算
化学键 | C—H | C—F | H—F | F—F |
键能/(kJ·mol-1) | 414 | 489 | 565 | 155 |
CH4(g)+4F2(g) =CF4(g)+4HF(g)的反应热ΔH为______kJ/mol
(3) 已知:①2CH3OH(l)+3O2(g) =2CO2(g)+4H2O(g) ΔH1=-a kJ/mol
②C(s)+O2(g)=CO2(g) ΔH2=-b kJ/mol
③2H2(g) + O2(g) = 2H2O(g) ΔH3 = -c kJ/mol
a、b、c均大于0 则:反应①中,ΔS______(选填“>”、“<”或“=”)0;
2C(s)+4H2(g)+O2(g) = 2CH3OH(l) ΔH=_______kJ/mol。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com