
����Ŀ�������Ԫ�����ڱ���һ���֣�����Ԫ���ڱ��е�λ�ã��ش��������⣺
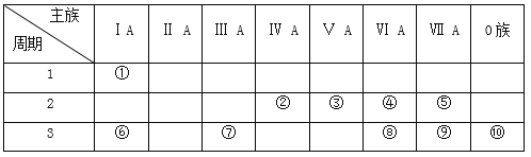
(1)����Ԫ������������Ӧˮ�����У�������ǿ����__________(�ѧʽ)��������ǿ����__________(�ѧʽ)�������Ե���__________(������)��
(2)��̬�⻯���У����ȶ�����__________(�ѧʽ)���ܢ��γɵ��⻯���зе���ߵ���__________(�ѧʽ),ԭ����__________________��
(3)�ֱܷ�͢١�������Ԫ�ص�ԭ�Ӱ�1:1��ɵij���������ĵ���ʽ�ֱ�Ϊ__________��_______���õ���ʽ��ʾ�ںܵ͢���ԭ�ӷ��ӵ��γɹ���____________��
(4)�ܢޢߢ�ļ����Ӱ뾶�ɴ�С��˳��Ϊ__________(�����ӷ��ź���������ʾ)��
(5)�͢ߵ�����������Ӧˮ����֮�䷢����Ӧ�Ļ�ѧ����ʽ___________����
(6)Ϊ��֤���͢�����Ԫ�صĽ�����ǿ��������˵����ʵ�����ṩ֤�ݵ���______��
A���Ƚ�����Ԫ�صĵ��ʵ��۵㡢�е�ߵ�
B��������Ԫ�صĵ��ʷֱ�����ˮ��Ӧ���۲췴Ӧ�ľ��ҳ̶�
C���Ƚ�����Ԫ�ص�����������Ӧ��ˮ����ļ���ǿ��
���𰸡�HClO4 NaOH �������� HF H2O �γ���� ![]()
![]()
![]() r(Cl-)> r(O2-)> r(Na+) > r(Al3+) NaOH + Al(OH)3 = NaAlO2 + 2H2O BC
r(Cl-)> r(O2-)> r(Na+) > r(Al3+) NaOH + Al(OH)3 = NaAlO2 + 2H2O BC
��������
(1)�ǽ�����Խǿ������������ˮ���������Խǿ��ͬ��������Ԫ���������ҷǽ�������ǿ��ͬ�������϶��·ǽ����Լ���������ͼʾԪ���зǽ�������ǿ��Ԫ��ΪF����O��F����Ԫ��û������������������������ˮ�����������ǿ����ClԪ�أ���Ӧ����ΪHClO4��������Խǿ������������ˮ����ļ���Խǿ����������ǿ��Ԫ��ΪNa����Ӧ�ļ�ΪNaOH��AlԪ�ص�����������ˮ�����������������ԣ�
(2)�ǽ���Խǿ��̬�⻯��Խ�ȶ����������ȶ���ΪHF���ܢ��γɵ��⻯��ֱ�ΪH2O��H2S����ˮ����֮���������������۷е����H2S��
(3)�ֱܷ�͢١�������Ԫ�ص�ԭ�Ӱ�1:1��ɵij���������ΪH2O2��Na2O2��˫��ˮΪ���ۻ��������ʽΪ![]() ����������Ϊ���ӻ��������ʽΪ
����������Ϊ���ӻ��������ʽΪ![]() ���ںܵ͢���ԭ�ӷ���ΪCO2�����γɹ���Ϊ
���ںܵ͢���ԭ�ӷ���ΪCO2�����γɹ���Ϊ![]() ��
��
(4)���Ӳ���Խ�����Ӱ뾶Խ���Ӳ�����ͬ���˵����ԽС�뾶Խ�����Ԣܢޢߢ�ļ����Ӱ뾶�ɴ�С��˳��Ϊr(Cl-)> r(O2-)> r(Na+) > r(Al3+)��
(5)�͢ߵ�����������Ӧˮ����ֱ�ΪNaOH��Al(OH)3�����߷�Ӧ����ƫ�����ƺ�ˮ������ʽΪNaOH + Al(OH)3 = NaAlO2 +H2O��
(6)A���͢ߵĵ��ʾ�Ϊ�������壬����������۷е�ͽ���������������������Ӱ뾶�йأ���������أ���A���������⣻
B��������Խǿ��ѧ����Խ���ã�����ˮ��ӦԽ���ң�Na����ˮ���ҷ�Ӧ��Al����ˮ����Ӧ��˵��Na�Ľ����Ա�Alǿ����B�������⣻
C��������Խǿ������������ˮ����ļ���Խǿ����C�������⣻
��������ѡBC��


 ����ѧУ�ֲ����ܲ�ϵ�д�
����ѧУ�ֲ����ܲ�ϵ�д� �ƸԺ���ȫ�����Ų��Ծ�ϵ�д�
�ƸԺ���ȫ�����Ų��Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�л���Ľṹ��ͼ��ʾ�����й��ڸ��л������������ȷ����
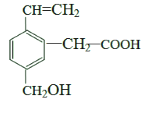
������̼ԭ�ӿ��ܹ��棻
����ʹ����KMnO4��Һ����ˮ��ɫ����ԭ����ͬ��
��1mol���л���ֱ�������Na��NaHCO3��Ӧ��������������ͬ�������������ȣ�
���ܷ���������Ӧ��
���ܷ����Ӿ۷�Ӧ��
��1mol���л�����ȫȼ������CO2��H2O����O2�����Ϊ280 L(��״��)
A. �٢�B. �ڢ�C. �ۢ�D. �ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ô�����̼�����ϡ���ᷴӦ��ȡ������̼���壬��ش�
��1��ʵ���������ͼ��ʾ�������жϣ�________�λ�ѧ��Ӧ������죬_______���ռ��Ķ�����̼������ࡣ

��2��Ϊ�˼���������Ӧ�����ʣ�������Һ�м����������ʣ�����Ϊ���е�����_____��
A.����ˮ B.�Ȼ��ƹ��� C.�Ȼ�����Һ D.Ũ����
��3���������������⣬����Ϊ�����Բ�ȡ��Щ��ʩ��������ѧ��Ӧ���ʣ������ٻش����֣�_______________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������װ�ã����ּг�װ�ü�ʯ������ʡ�ԣ�������ܴﵽʵ��Ŀ�ĵ���

A. ��װ�â�����ϩB. ��װ�âڷ��뱽�ͱ���
C. ��װ�â��Ʊ���������D. ��װ�â���֤���ᡢ̼�ᡢ��������ǿ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������ʵ�����������ʵ�������ȷ����(����)
ѡ�� | ʵ�� | ���� | ʵ����� |
A | ��ij��Һ���ȵμ�����ϡ���ᣬ�ٵμ�����BaCl2��Һ | ���ְ�ɫ���� | ԭ��Һ�к���SO42-��SO32-��HSO3-�е�һ�ֻ��� |
B | ��װ��Fe(NO3)2��Һ���Թ��м���ϡ���� | �ڹܿڹ۲쵽����ɫ���� | HNO3�ֽ����NO2 |
C |
| ��������Ϊ��ɫ���ұ������Ϊ��ɫ | �����ԣ�Cl2>Br2>I2 |
D | SO2��SO3�������ͨ��Ba(NO3)2��Һ | ���ְ�ɫ���� | �õ��ij���ֻ��BaSO4 |
A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������նȴ�ѧ�о�������һ���������غϽ��Ʊ��������¹���(��ͼ��ʾ)�������йظù��յ�˵���������(����)

A.���غϽ����ѭ��ʹ��
B.�ù����У�������ת����ʽֻ������
C.���غϽ���ˮ��Ӧ�Ļ�ѧ����ʽΪ��2Al��3H2O  Al2O3��3H2��
Al2O3��3H2��
D.�ܷ�ӦʽΪ2H2O 2H2����O2��
2H2����O2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����MN����ˮ������ͼ���̣������й�˵���в���ȷ����

A. �ù��̿ɱ�ʾMN��ˮ�����
B. ��ͬ�����½��H+������N->OH-
C. �ù���ʹ��Һ�е�c(OH-)>c(H+)
D. ��Һ�д���c(HN)=c(OH-)-c(H+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���25 mL 0.1 mol��L-1NaOH��Һ����εμ�0.2 mol��L-1��HN3(������)��Һ��pH�ı仯������ͼ��ʾ(��Һ���ʱ����ı仯���Բ��ƣ����������һԪ����)������˵����ȷ����

A. ��C�㣬�μӵ�V(HN3)=12.5 mL
B. ��B�㣬����Ũ�ȴ�СΪ c(OH-)>c(H+)>c (Na+)>c(N3-)
C. ˮ�������c(H+)��A��С��B��
D. ��D�㣬c(Na+)=2c(HN3)+2 c(N3-)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ס������ձ��и�ʢ��100 mL 3 mol��L��1�����������������Һ�������ձ��зֱ��������������ۣ���Ӧ���������ɵ�����������Ϊ�ס��ң�1��2����������۵�����Ϊ(����)
A.5.4 gB.3.6 gC.2.7 gD.1.8 g
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com