
【题目】某化学兴趣小组要完成中和热的测定实验。
(1)实验桌上备有烧杯(大、小两个烧杯)、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃玻璃棒、50 mL0.25 mol· L-1稀硫酸、50 mL 0.55mol· L-1NaOH溶液,尚缺少的实验玻璃用品是:__________________、__________________。
(2)某同学用该装置做实验,因有些操作不规范,造成所测中和热的数值偏低,请分析可能的原因是_________________(用标号字母填写)。
A.测量稀硫酸温度后,温度计没用水冲洗干净
B.把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓
C. 量取稀硫酸时仰视计数
D.将50mL0.55mol/L氢氧化钠溶液取成了50mL0.55mol/L的氨水
E.大烧杯的盖板中间小孔太大了
(3)实验得到表中的数据:
实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | |
盐酸 | NaOH溶液 | ||
1 | 20.2 | 20.3 | 23.7 |
2 | 20.3 | 20.5 | 23.8 |
3 | 21.5 | 21.6 | 24.9 |
假设0.55mol/LNaOH溶液和0.25mol/L硫酸溶液的密度都近似取1g/cm3,中和后所得溶液的比热容c =4.18 J/(g·℃)。则中和热ΔH =_____________ kJ/mol。
(4)如果用60mL0.25mol/L硫酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比,所放出的热量_________(填:“增多”、“不变”、“减少”),所求中和热_________(填:“相等”、“不相等”)。
(5)若用KOH代替NaOH,对测定结果_______________(填:“有” 或 “无”)影响。![]()
![]()
【答案】温度计 量筒(50mL) ABDE -51.83; 增多 相等 有
【解析】
(1)要做中和热的测定实验时,除了实验桌上备有的仪器还需要玻璃用品是温度计、 50mL的量筒。答案:温度计、 量筒(50mL)。
(2)A.测量盐酸的温度后,温度计没有用水冲洗干净,在测碱的温度时,会发生酸和碱的中和反应,温度计示数变化值减小,所以导致实验测得中和热的数值偏小,所以A正确;B、把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓,会导致一部分能量的散失,实验测得中和热的数值偏小,所以B正确;C、在量取稀硫酸时仰视计数,会使得实际量取体积高于所要量的体积,算过量,可以保证碱全反应,会使得中和热的测定数据偏高,故C错误;D、将50mL0.55mol/L氢氧化钠溶液取成了50mL0.55mol/L 的氨水,因为氨水是弱碱,电离时是吸热的过程,所以导致实验测得中和热的数值偏小,故D正确;E、大烧杯的盖板中间小孔太大,会导致一部分能量散失,所以测的数值降低,故F正确。所以ABDE选项是正确的。
(3)第1次实验硫酸和NaOH溶液起始平均温度为20.05![]() ,反应后温度为:23.2
,反应后温度为:23.2![]() ,温度差为: 3.15
,温度差为: 3.15![]() ;第2次实验硫酸和NaOH溶液起始平均温度为20.3
;第2次实验硫酸和NaOH溶液起始平均温度为20.3![]() ,温度差为:3.1
,温度差为:3.1![]() ;第3次实验硫酸和NaOH溶液起始平均温度为20.55
;第3次实验硫酸和NaOH溶液起始平均温度为20.55![]() ,温度差为:3.05
,温度差为:3.05![]() ;三次温度差平均值为:3.1
;三次温度差平均值为:3.1![]() ;用50 mL0.25 mol· L-1稀硫酸和50 mL 0.55mol· L-1NaOH溶液进行反应,生成水的物质的量为0.05L
;用50 mL0.25 mol· L-1稀硫酸和50 mL 0.55mol· L-1NaOH溶液进行反应,生成水的物质的量为0.05L![]() L-1=0.025mol,溶液的质量为100mL
L-1=0.025mol,溶液的质量为100mL![]() 1g/cm3=100g,温度变化的值为ΔT=3.1
1g/cm3=100g,温度变化的值为ΔT=3.1![]() ,则生成0.025mol水放出的热量为Q=mcΔT=100g
,则生成0.025mol水放出的热量为Q=mcΔT=100g![]() 4.18 J/(g·℃)
4.18 J/(g·℃)![]() =1295.8J,即1.2958J ,所以实验测得的中和热ΔH =1.2958J /0.025mol =51.83KJ/mol;因此,本题正确答案是: -51.83。
=1295.8J,即1.2958J ,所以实验测得的中和热ΔH =1.2958J /0.025mol =51.83KJ/mol;因此,本题正确答案是: -51.83。
(4)如果用60mL0.25mol/L硫酸与50mL0.55mol/LNaOH溶液进行反应,发生中和反应的酸碱量增多了,放出的热量也多了。但中和热指的是稀溶液中,酸跟碱发生中和反应生成1mol水时放出的热量,所以所求中和热相等。
(5)因为 KOH的溶解度比NaOH低,若用KOH代替NaOH,对测定结果有影响;答案:有。


 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案科目:高中化学 来源: 题型:
【题目】对于反应A (g)+ 3B(g) =2C(g) + 2D(g),下列数据表示反应进行得最快的是( )
A. v(A)=0.7mol/(L·s)B. v (B) =1.8mol/(L· s)
C. v (C)=1mol/(L·s)D. v (D) =1.6mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温时,改变饱和氯水的pH,得到部分含氯微粒的物质的量分数与pH的关系如图所示。下列叙述不正确的是

A. 该温度下,HClO![]() H++ClO-的电离常数Ka的对值lgKa= -7.54
H++ClO-的电离常数Ka的对值lgKa= -7.54
B. 氯水中的Cl2、ClO-、HClO均能与KI发生反应
C. pH=1的氯水中,c(Cl2)>c(Cl3-)>c(HClO)>c(ClO-)
D. 已知常温下反应Cl2(aq)+Cl-(aq)![]() Cl3-(aq)的K=0.191,当pH增大时,K减小
Cl3-(aq)的K=0.191,当pH增大时,K减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭恒容容器中,加入1molN2和3molH2发生反应:N2(g)+3H2(g)2NH3(g),下列叙述中能说明该反应达到平衡状态的是( )
A.![]() B.混合气体的密度保持不变
B.混合气体的密度保持不变
C.混合气体的平均相对分子质量保持不变D.![]() :
:![]() :
:![]() :3:2
:3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.明矾[KAl(SO4)2·12H2O] 在生产、生活中有广泛用途:饮用水的净化;造纸工业上作施胶剂;食品工业的发酵剂等。利用炼铝厂的废料——铝灰(含Al、 Al2O3及少量SiO2和FeO ·xFe2O3)可制备明矾。工艺流程如下:

已知生成氢氧化物沉淀的pH如下表所示:
Al(OH)3 | Fe(OH)2 | Fe(OH)3 | |
开始沉淀 | 3.4 | 6.3 | 1.5 |
完全沉淀 | 4.7 | 8.3 | 2.8 |
回答下列问题:
(1)明矾净水的原理是______________________________(用离子方程式表示)。
(2)操作Ⅱ是_______________、_________________、过滤、洗涤、干燥。
(3)检验滤液A中是否存在Fe2+的方法______________________________ (只用一种试剂)。
(4)在滤液A中加入高锰酸钾发生反应的离子方程式为:__________。
(5)调节pH=3的目的是_______________________ ,滤渣2含有的物质是______。
II.(6)取一定量含有Pb2+、Cu2+的工业废水,向其中滴加Na2S溶液,当PbS开始沉淀时,溶液中c(Pb2+)/c(Cu2+) =_________ (保留三位有效数字)。[已知Ksp(PbS)=3.4×10-28,
Ksp(CuS)=1.3×10-36]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硅及其化合物在材料领域中应用广泛。下列叙述不正确的是 ( )
选项 | 物质 | 用途 | 原理 |
A | 晶体硅 | 电脑芯片 | 熔点高、硬度大 |
B | 二氧化硅 | 光导纤维 | 透明无色固体 |
C | 硅酸钠 | 玻璃粘合剂 | 浓度高时是一种粘稠液体 |
D | 硅胶 | 吸水剂 | 具有疏松多孔的结构 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为元素周期表截取的短周期的一部分,即四种元素均为非稀有气体元素。下列关于这四种元素及其化合物的说法中正确的是 ( )
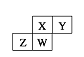
A.原子半径:W>Z>Y>X
B.气态氢化物的稳定性:Z>W>X>Y
C.W的最高正化合价与负化合价的绝对值可能相等
D.Z的最高价氧化物的水化物肯定为强碱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A.氨水使酚酞溶液变红是因为溶液中NH3H2O电离出OH-
B.KNO3溶于水电离出K+和NO3-
C.电离时生成的阳离子有H+的化合物不一定是酸
D.SO2溶于水能导电,所以SO2是电解质
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com