
| A、减小A或B的用量 |
| B、减小C的量 |
| C、增大B的量 |
| D、增大D的量 |
科目:高中化学 来源: 题型:
| A、2HClO═2HCl+O2↑ | ||||
| B、2Na2O2+2CO2═2Na2CO3+O2 | ||||
| C、4Fe(OH)2+O2+2H2O═4Fe(OH)3 | ||||
D、2NaHCO3
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、少量Na2SO4固体,v(H2)不变 |
| B、VmLNa2SO4溶液,v(H2)增大 |
| C、将稀硫酸改为浓硫酸,v(H2)增大 |
| D、VmL稀硝酸,v(H2)增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、一定温度下,15g甲醛和乙酸的混合物中O原子数为0.5NA |
| B、标准状况下,NO和O2各11.2L混合,所得混合气体的分子总数为0.75NA |
| C、14g分子通式为CnH2n的链烃中含有的C=C的数目为NA/n |
| D、在反应KIO3+6HI=KI+3I2+3H2O中,每生成3mol I2转移的电子数为6NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
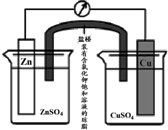
| A、在外电路中,电流从Zn极流向Cu极 |
| B、盐桥中的Cl-移向CuSO4溶液 |
| C、当负极减小65g时,正极增加65g |
| D、电池的总反应为 Zn+Cu2+=Zn2++Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在0.1 mol/L NaHCO3溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) |
| B、在0.1 mol/L Na2CO3溶液中:c(OH-)-c(H+)=c(HCO3-)+c(H2CO3) |
| C、向0.2mol/LNaHCO3溶液中加入等体积0.1 mol/LNaOH溶液:c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |
| D、0.2 mol/L的NaHCO3溶液中c(H+)+c(H2CO3)=c(CO32-)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、快速逃离火灾现场时,应用湿毛巾捂口鼻弯腰呼吸,因为许多易燃有机高分子材料燃烧时会释放出大量有毒气体,而且热气体的密度比空气轻 |
| B、吃米饭或馒头时,多加咀嚼会感到甜味,是因为淀粉发生水解反应生成了麦芽糖 |
| C、油脂是人类的主要食物之一,“地沟油”对人体的危害极大 |
| D、肥皂的去污原理与合成洗涤剂的去污原理不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
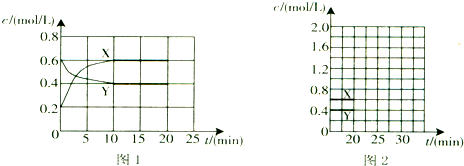
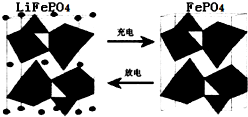
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com