
【题目】(1)某课外活动小组同学用如图装置进行实验,试回答下列问题:
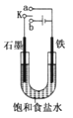
①若开关K与a连接,则铁发生电化学腐蚀中的_____腐蚀,石墨电极上的电极反应式为_____。
②若开关K与b连接,则电解反应的化学方程式为_____。
(2)该小组同学设想,如果模拟工业上离子交换膜法制烧碱的方法,用如下图所示装置电解硫酸钠溶液来制取氢气、氧气、硫酸和氢氧化钠,无论从节省能源还是从提高原料的利用率而言都更加符合绿色化学理念。
①该电解槽的阳极反应式为_____。
此时通过阴离子交换膜的离子数_____(选填“大于”、“小于”或“等于”)通过阳离子交换膜的离子数。
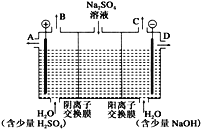
②通电开始后,阴极附近溶液pH_____(选填“增大”、“不变”或“减小”)。
③若将制得的氢气、氧气和氢氧化钠溶液组合为氢氧燃料电池,则电池负极的电极反应式为_____;已知H2的燃烧热为285.8 kJ/mol,则该燃料电池工作产生36 g 液态H2O时,理论上有_____kJ的能量转化为电能。
【答案】 吸氧 O2+2H2O+4e-=4OH- 2NaCl+2H2O=2NaOH+Cl2↑+H2↑ 4OH--4e-=2H2O+O2↑ 小于 增大 H2-2e-+2OH-=2H2O 571.6
【解析】(1)①开始时开关K与a连接,是原电池,铁为负极,发生氧化反应,失去电子生成亚铁离子,电极方程式为Fe-2e-=Fe2+,A极上氧气得电子被还原,电极方程式为O2+2H2O+4e-=4OH-,为铁的吸氧腐蚀;故答案为:吸氧;O2+2H2O+4e-=4OH- ;
②开关K与b连接,装置为电解池,铁为阴极,发生还原反应,氢离子得到电子生成氢气,电解饱和食盐水生成氢氧化钠、氢气和氯气,总反应式为2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑;故答案为:2NaCl+2H2O
2NaOH+H2↑+Cl2↑;故答案为:2NaCl+2H2O![]() 2NaOH+H2↑+Cl2↑;
2NaOH+H2↑+Cl2↑;
(2)①电解时,阳极上失电子发生氧化反应,溶液中的氢氧根离子的放电能力大于硫酸根离子的放电能力,所以阳极上氢氧根离子失电子生成水和氧气4OH--4e-=2H2O+O2↑;阳极氢氧根离子放电,因此硫酸根离子向阳极移动,阴极氢离子放电,因此钠离子向阴极移动,所以通过相同电量时,通过阴离子交换膜的离子数小于通过阳离子交换膜的离子数,故答案为:4OH--4e-=2H2O+O2↑;小于;
②通电开始后,阴极上氢离子放电生成氢气,氢离子来自于水,所以促进水的电离,导致溶液中氢氧根离子的浓度大于氢离子的浓度,所以溶液的pH值增大,故答案为:增大;
③氢气、氧气和氢氧化钠溶液组合为氢氧燃料电池,负极上氢气失去电子,负极反应式为:H2-2e-+2OH-=2H2O;H2的燃烧热为285.8kJ/mol,则2H2(g)+O2(g)=2H2O(l)△H=-571.6kJ/mol,该燃料电池工作产生36g H2O,n(H2O)=![]() =2mol,由燃烧的热方程式可知,生成2molH2O放出571.6kJ的热量,即理论上有571.6kJ的能量转化为电能;故答案为:H2-2e-+2OH-=2H2O;571.6。
=2mol,由燃烧的热方程式可知,生成2molH2O放出571.6kJ的热量,即理论上有571.6kJ的能量转化为电能;故答案为:H2-2e-+2OH-=2H2O;571.6。


 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案科目:高中化学 来源: 题型:
【题目】25 ℃时,用0.10 mol·L-1的氨水滴定10.00 mL a mol·L-1的盐酸,混合溶液的pH与氨水的体积(V)的关系如图所示。已知N点溶液中存在:c(H+)=c(OH-)+c(NH3·H2O),下列说法不正确的是( )
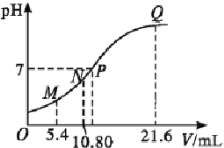
A. 图上四点分子种类相同
B. a=0.1
C. N、Q两点的![]() :N=Q
:N=Q
D. P点溶液中存在:c(Cl-)=c(NH4+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中I是一种高分子化合物,其合成路线如图:


已知:①![]()
②回答下列问题:
(1)A的名称为_______(系统命名法),G含有的官能团_____(写名称)。
(2)反应①的反应类型是________.
(3)I的结构简式为_____________________________;
(4)反应②的化学方程式为__________________________________。
(5)符合下列条件的G的同分异构体共有___________种。
①与G具有相同官能团; ②属于芳香族化合物
(6)参照上述合成路线,设计一条由乙醛、甲醇和J(E的同系物且相对分子质量比E小14)为主要原料(无机试剂任选)制备![]() 的合成路线______________。
的合成路线______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列我国科研成果所涉及材料中,主要成分为同主族元素形成的无机非金属材料的是
|
|
|
|
A.4.03米大口径碳化硅反射镜 | B.2022年冬奥会聚氨酯速滑服 | C.能屏蔽电磁波的碳包覆银纳米线 | D.“玉兔二号”钛合金筛网轮 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知H2的燃烧热为ΔH=-285.8 kJ·mol-1,CO的燃烧热为ΔH=-282.8 kJ·mol-1;现有H2和CO组成的混合气体5.6 L(标准状况),经充分燃烧后,放出总热量为71.15 kJ,并生成液态水。下列说法正确的是
A. CO燃烧的热化学方程式为2CO(g)+O2(g)===2CO2(g) ΔH=-282.8 kJ·mol-1
B. H2燃烧的热化学方程式为2H2(g)+O2(g)===2H2O(g) ΔH=-571.6 kJ·mol-1
C. 燃烧前混合气体中CO的体积分数为60%
D. 燃烧后的产物全部与足量的过氧化钠作用可产生0.125 mol O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关原子轨道的叙述中正确的
A.氢原子的2s轨道能量较3p轨道高
B.能层n=4的原子轨道最多可容纳16个电子
C.p能级的原子轨道呈哑铃形,随着能层序数的增加,p能级原子轨道也在增多
D.锂原子的2s与5s 轨道皆为球形分布
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按如图装置,持续通入X气体,可以看到a处有红色物质生成,b处变蓝,c处得到液体,则X气体是( )

A. (CH3)3COH (气)B. NH3C. CH3CH2CH2OH(气)D. CO和H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中只含有Na+、Al3+、Cl-、SO42-四种离子,已知前三种离子的个数比为3∶1∶2,则溶液中Al3+ 和SO42-的离子个数比为
A. 1∶2 B. 1∶4 C. 3∶4 D. 3∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚氯酸钠(NaClO2)是一种高效氧化、杀菌及漂白剂,其生产工艺如下:
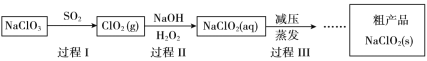
(1)NaClO2中氯元素的化合价是_________。从氧化还原角度推测NaClO2可能具有的化学性质是_________。
(2)过程I常伴有少量Cl2生成。
① Cl2的存在会造成产品中含有NaCl,请结合离子方程式解释其原因_________。
② 结合下面信息,请设计实验方案除去ClO2中的Cl2 ________。
ClO2 | Cl2 | |
在水中的溶解性 | 易溶 | 溶 |
在CCl4中的溶解性 | 难溶 | 溶 |
(3)过程II中H2O2的作用是________(填“氧化剂”或“还原剂”)。
(4)理论上每生成1 mol NaClO2,消耗SO2的体积是________L(标准状况下)。
(5)已知:
i. 压强越大,物质的沸点越高。
ii. NaClO2饱和溶液在温度低于38℃时析出NaClO23H2O
38~60℃时析出NaClO2晶体
高于60℃时分解成NaClO3和NaCl
① 过程III采用“减压蒸发”操作的原因是_____。
② 请将过程III的操作补充完整_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com