
【题目】化学是一门以实验为基础的自然科学,化学实验在化学学习中具有极其重要的作用。下列有关仪器的选择及试剂的保存正确的是
A. 用托盘天平称量5.75gNaCl固体
B. 用碱式滴定管量取20. 00mL KMnO4溶液
C. 在存放液溴的试剂瓶中加水进行液封
D. AgNO3溶液保存于无色细口瓶中
科目:高中化学 来源: 题型:
【题目】下列有关物质的分类或归类中正确的是( )
A. 化合物:HT、CaCl2、NaOH、盐酸
B. 纯净物:水玻璃、胆矾晶体、液氯、硫酸
C. 天然高分子化合物:淀粉、纤维素、蛋白质、聚氯乙烯
D. 同分异构体:CH3CH2CH2CH2CH3、CH3CH2CH(CH3)2、C(CH3)4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了验证SO2的性质,某同学利用输液管设计了如下微型实验:
回答下列问题:
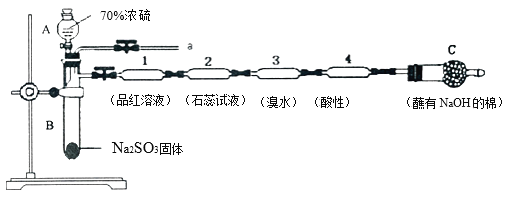
(1)仪器A的名称是__________。
(2)装置l中的现象是______;装置3中证明SO2具有______性。
(3)下列说法正确的是____________。
A.装置2中紫色石蕊试液变红的原因是SO2+H2O=H2SO3, H2SO3显酸性
B.实验结束后将输液管1加热溶液不变色
C.实验结束后,可由a导管向装置中加水,将气体赶出后再拆装置,防止残留的SO2有毒气体污染环境
D.在a导管处用向下排空气法收集SO2
(4)装置4中酸性高锰酸钾褪色,经测定反应后溶液中含有Mn2+和SO42—,请写出该反应的离子方程式__________。
(5)该学生还利用上图部分仪器组装成的装置(如图)证明S、C、Si非金属性强弱。可共选择的试剂有:硫酸、亚硫酸、硝酸、木炭、硅酸钠溶液。
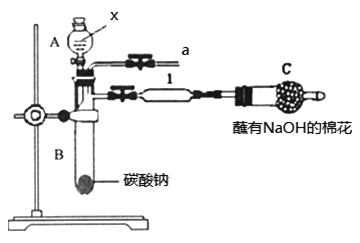
①装置A中试剂X是_______;装置1中反应的化学方程式是________。
②实验结论:因为酸性强弱是____>_____>_____(填化学式),故非金属性是S>C>Si。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关石油、煤、天然气的叙述正确的是
A. 石油经过催化重整可得到芳香烃
B. 煤中含有的苯、甲苯等可通过干馏得到
C. 石油的分馏、煤的气化和液化都属于化学变化
D. 石油、煤、天然气、可燃冰、沼气都属于化石燃料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有部分元素的性质、用途与原子(或分子)结构如表所示:
元素编号 | 元素性质与原子(或分子)结构 |
W | 周期表中原子半径最小的元素 |
X | 氢化物可与其最高价氧化物的水化物反应生成盐 |
Y | 一种核素在考古时常用来鉴定一些文物的年代 |
Z | M层比K层少1个电子 |
T | 存在两种同素异形体,其中一种可吸收紫外线 |
(1)元素Y在周期表中的位置第____,元素T的简单离子结构示意图_____。
(2)W、X、Z、T中有两种元素能形成既有离子键又有非极性共价键的化合物,写出该化合物的电子式____________。
(3)元素W与元素X、T可以分别形成多种核外电子总数为10的微粒,其中有四种微粒可以发生反应:甲 + 乙 ![]() 丙 + 丁,该反应为:_____________。
丙 + 丁,该反应为:_____________。
(4)元素X与元素W以原子个数比1∶2化合形成常用于火箭燃料的化合物戊,元素T和元素W以原子个数比为1∶1化合形成化合物己,戊与己能发生氧化还原反应,生成X单质和另一种液体化合物,写出该反应的化学方程式________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】FeCl3溶液、Fe(OH)3胶体共同具备的性质是( )
A. 都呈透明的红褐色
B. 分散质颗粒直径相同
C. 都较稳定,密封保存一段时间都不会产生沉淀
D. 当有光线透过时,都能产生丁达尔效应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中所含原子数相同的是
A.2 L CO和2 L O2
B.同温同压下,2LO2和N2与NO的混合气体2L
C.0.2 mol H2和4.48 L HCl
D.标准状况下2 mol CO2和44.8 L水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表的形式多种多样,下图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表,思考扇形元素周期表的填充规律,并回答下列问题:

(1)L元素在常见周期表中所处的位置是________,其单质与A2E反应的化学方程式为____________。
(2)元素F、G、J、K、M对应简单离子的离子半径由大到小的顺序是(用离子符号表示)___________。
(3)用电子式表示MO2的形成过程:_______________。
(4)B、F、G三种元素最高价氧化物对应的水化物碱性最强的是__________(填化学式)。比较元素C和J的非金属性强弱:C______J(填“强于”或“弱于”)。
(5)向元素B和N形成的化合物的水溶液中,加入元素K的单质,所发生的反应的离子方程式为_____;反应后,向溶液中加入C、K形成的化合物,现象为___________。
(6)均由A、B、E、J四种元素组成的两种化合物可相互反应,写出反应的化学方程式______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com