
【题目】在含有0.06 mol Cl-、0.07 mol SO42 -及一定量Mg2+和Al3+的混合溶液中,滴入2 mol/L NaOH溶液,产生沉淀情况如图。若反应前Al3+的物质的量为a mol,Al3+的物质的量与混合溶液中离子总物质的量的比值为x(不考虑Mg2+和Al3+水解及水的电离)。则下列说法错误的是

A.a的取值范围是0<a<1/15
B.图中m的取值范围5.2~5.8
C.A、B两点横坐标的数值均随x变化而变化
D.若B点横坐标数值为120 ,则a=0.04
【答案】C
【解析】
试题分析:A.若溶液中没有Mg2+,根据溶液呈电中性,0.06×1+0.07×2=a×3,解得a=1/15,所以a的取值范围是0<a<1/15,A项正确;B.若溶液中只有Al3+,则沉淀m=78×1/15=5.2,若溶液中只有Mg2+,根据溶液呈电中性,n(Mg2+)= (0.06×1+0.07×2)÷2=0.1mol,则沉淀m=58×0.1=5.8g,所以图中m的取值范围5.2~5.8,B项正确;C.溶液中的正电荷数为0.06×1+0.07×2=0.20mol,1mol正电荷对应1mol NaOH生成沉淀,所以A点的横坐标不随x的变化而变化,C项错误;D.B点是NaCl、Na2SO4和Na[Al(OH)4]的溶液,根据Na+守恒,n(Na[Al(OH)4])=0.12×2-0.06-0.07×2=0.04,即a=0.04,D项正确;答案选C。


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案科目:高中化学 来源: 题型:
【题目】M2O7x﹣离子和S2﹣在酸性溶液中发生反应:M2O7x﹣+3S2﹣+14H+=2M3++3S↓+7H2O,则M2O7x﹣离子中M的化合价是( )
A. +2 B. +3 C. +4 D. +6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】异丙苯是一种重要的有机化工原料.异丙苯的结构简式为 ![]() .
.
(1)异丙苯中至少有个碳原子共平面.
(2)异丙苯有多种同分异构体,其中一溴代物只有两种的芳香烃是(填结构简式).
(3)由异丙苯制备对溴异丙苯的化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释实验事实的离子方程式正确的是( )
A.纯碱溶液显碱性的原因:CO32﹣+2H2O ![]() H2CO3+2OH﹣
H2CO3+2OH﹣
B.氯化铁溶液腐蚀铜线路板Cu+Fe3+=Cu2++Fe2+
C.稀硫酸与氢氧化钡溶液恰好中和:Ba2++OH﹣+H++SO42﹣=BaSO4↓+H2O
D.氯气溶于水:Cl2+H2O=H++Cl﹣+HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分析原子的杂化方式,并根据等电子体原理判断下列各组分子中的所有原子,或者处于同一平面,或者在一条直线上的是( )
A.C2H2、HClO,C2H6
B.CO2、N2O,HC≡C﹣NH2
C.C6H5CH3、C3H4、CH4
D.C6H6、C2H4、HCN
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】称取一定质量的纯碱溶于水中,与适量的盐酸作用,下列关于盐酸的用量和气体产量的变化是(填偏大、偏小、不变)
(1)若纯碱中混有K2CO3,盐酸用量将____________;气体产量将_______________。
(2)若纯碱中混有NaHCO3,盐酸用量将___________;气体产量将_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制Cl2的反应为4HCl(浓)+ MnO2![]() MnCl2 + C12↑ + 2H2O。下列说法不正确的是
MnCl2 + C12↑ + 2H2O。下列说法不正确的是
A. 还原剂是HCl,氧化剂是MnO2
B. 每生成1 mol Cl2,该反应转移电子的物质的量为2 mol
C. 每消耗1 mol MnO2,被氧化的HCl的物质的量为4 mol
D. 该反应中,HCl既表现还原性又表现酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为一原电池的结构示意图,下列说法中,错误的是( ) 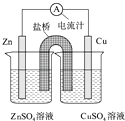
A.Cu电极为正电极
B.原电池工作时,电子从Zn电极流出
C.原电池工作时的总反应为:Zn+Cu2+=Zn2++Cu
D.盐桥(琼脂﹣饱和KCl溶液)中的K+移向ZnSO4溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com