
【题目】下列性质比较中不正确的是( )
A.沸点:CBr4>CF4
B.水溶性:HBr>Br2
C.硬度:镁>镁铝合金
D.熔点:金刚石>NaCl
科目:高中化学 来源: 题型:
【题目】在2A+B3C+5D反应中,表示该反应速率最快的是( )
A.v(A)═0.5 mol/(Ls)
B.v(B)═0.3mol/(Ls)
C.v(C)═0.8 mol/(Ls)
D.v(D)═1mol/(Ls)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积不变的密闭容器中进行反应:2SO2( g )+O2( g)2SO3(g );△H<O.如图表示当其它条件不变时,改变某一条件对上述反应的影响,其中分析正确的是( ) 
A.图Ⅰ表示温度对化学平衡的影响,且甲的温度较高
B.图Ⅱ表示t0时刻使用催化剂对反应速率的影响
C.图Ⅱ表示t0时刻通入氦气对反应速率的影响
D.图Ⅲ表示t0时刻增大O2的浓度对反应速率的影响
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下表中几种短周期元素的原子半径及主要化合价,回答下列问题:
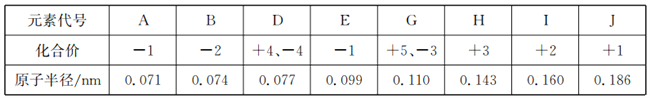
(1)元素D组成的常见单质有两种,分别是_______、________(写名称)。
(2)用电子式表示IE2的形成过程:_________________________。
(3)A、H、J的离子半径由大到小顺序是_________(用离子符号表示)。
(4)78 g J2B2与足量的水反应生成_______L(标准状况下)气体。
(5)元素E的单质与水反应的离子方程式为_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列框图分析,下列说法正确的是( ) 
A.E2+的氧化性比M2+的氧化性强
B.在③反应中加稀硫酸可抑制Fe2+的水解
C.反应④的离子方程式可表示为:E3++3SCN﹣E(SCN)3↓
D.在反应①中只能用浓硫酸,既表现了酸性、又表现了氧化性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ几种短周期元素的原子半径及主要化合价如下表:已知X是短周期中最活泼的金属,且与R同周期.(请用化学用语答题)
元素代号 | X | Y | Z | M | R |
原子半径/nm | 0.186 | 0.102 | 0.075 | 0.074 | 0.143 |
主要化合价 | +1 | +6﹣2 | +5﹣3 | ﹣2 | +3 |
(1)R的元素符号为; M在元素周期表中的位置为 .
(2)X与Y按原子个数比1:1构成的物质的电子式为;所含化学键类型 .
(3)X+ , Y2,M2离子半径由大到小的顺序为(用离子符号表示) .
(4)用Cu单质作阳极,石墨作阴极,X的最高价氧化物对应的水化物溶液作电解液进行电解,写出阳极的电极反应式 .
Ⅱ如图转化关系A ![]() B
B ![]() C,若B为白色胶状不溶物,则A与C反应的离子方程式为 .
C,若B为白色胶状不溶物,则A与C反应的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇﹣空气燃料电池(DMFC)是一种高效能、轻污染的车载电池,其工作原理如图.下列有关叙述正确的是( ) 
A.H+从正极区通过交换膜移向负极区
B.负极的电极反应式为:CH3OH(l)+H2O(l)﹣6e﹣=CO2(g)+6H+
C.d导出的是CO2
D.图中b、c分别是O2、甲醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生铁在pH=2和pH=4的盐酸中发生腐蚀.在密闭容器中,用压强传感器记录该过程的压强变化,如图所示.下列说法中,不正确的是( ) 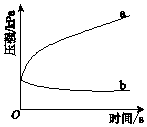
A.两容器中负极反应均为Fe﹣2e﹣═Fe2+
B.曲线a记录的是pH=2的盐酸中压强的变化
C.曲线b记录的容器中正极反应是O2+4e﹣+2H2O═4OH﹣
D.在弱酸性溶液中,生铁能发生吸氧腐蚀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com