
【题目】下列关于卤代烃的说法正确的是
A.在溴乙烷(CH3CH2Br)分子中,溴元素的存在形式为溴离子
B.在卤代烃中,卤素原子与碳原子形成共价键
C.聚四氟乙烯(塑料王)为高分子化合物,不属于卤代烃
D.卤代烃比相应的烷烃的沸点低
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】火力发电厂释放出大量氮的氧化物(NOx)、二氧化硫等气体会造成环境污染,对燃煤废气进行脱除处理。可实现绿色环保、低碳减排、废物利用等目的。
(1)己知:N2 (g) +O2 (g) =2NO (g) △H=+180.5kJ·mol-1
C (s) +O2 (g)=CO2 (g) △H=-393.5 kJ·mol-1
2C (s) +O2(g) =2CO (g)△H=-221 kJ·mol-1
若某反应的平衡常数表达式为: 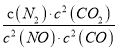 ,请写出此反应的热化学方程式_________。
,请写出此反应的热化学方程式_________。
(2)脱硝
利用甲烷与NO2反应,生成无污染的物质,则该反应的化学方程式为:___________。
(3)脱碳
将CO2转化为甲醇的热化学方程式为:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)△H3
CH3OH(g)+H2O(g)△H3
①取五份等体积CO2和H2的混合气体(物质的量之比均为1:3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数φ(CH3OH)与反应温度T的关系曲线(见如图1),则上述CO2转化为甲醇反应的△H3_____0(填“>”、“<”或“=”)。
②在一恒温恒容密闭容器中充入0.5molCO2和1.5molH2,进行上述反应.测得CO2和CH3OH(g)的浓度随时间变化如上图2所示.请回答:第10min后,若升温,该反应的平衡常数将_____(填“变大”、“变小”、“不变”);若向该容器中再充入1molCO2和3molH2再次达到平衡时,则CH3OH(g)的体积分数将___(“变大”、“变小”、“不变”)。
(4)脱硫
某种脱硫工艺中将废气经处理后,与一定量的氨气、潮湿的空气反应,生成硫酸铵和硝酸铵的混合物作为副产品化肥.设烟气中的SO2、NO2的物质的量之比为1:1,则该反应的化学方程式为__________。若在0.1mol/L的硝酸铵溶液中加入等体积的0.09mol/L氨水,配制了pH=8.2的溶液,则该溶液中微粒浓度由大到小的顺序为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实不能用勒夏特列原理解释的是
A. 实验室常用排饱和食盐水的方法收集氯气
B. 在硫酸亚铁溶液中,加入铁粉以防止氧化
C. 酯在碱性条件下水解的程度较为完全
D. 氨水应密闭保存,放置低温处
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T℃时,反应物和生成物均为气体的某反应,反应过程中浓度变化如图(Ⅰ)所示。若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如图(Ⅱ)所示,则下列结论正确的是
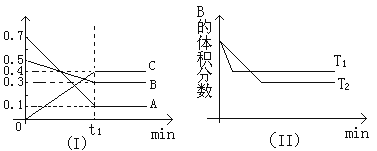
A.在t1时间内用B表示该反应的平均速率为:0.6mol·L-1·mim-1
B.在(t1+10)时,保持其他条件不变,增大压强,平衡向逆反应方向移动
C.T时,在相同容器中,若由0.1mol·L-1A、0.3mol·L-1B和0.4mol·L-1C反应,达到平衡后,C的浓度仍为0.4mol·L-1
D.在其他条件不变时,升高温度,正、逆反应速率均增大,且A的转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生 产MnO2和Zn的工艺简化流程如图所示(中间产物的固体部分已经略去):
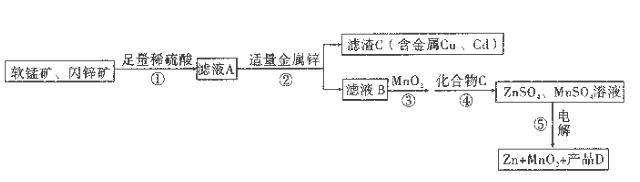
软锰矿: MnO2含量≥65%;Al2O3含量为4%。闪锌矿: ZnS含量≥80%; FeS、CuS、CdS含量各为2%。 滤液B中含金属离子: Zn2+、Mn2+、 Fe2+、Al3+。
试回答下列问题:
(1)步骤①中软锰矿、闪锌矿与硫酸溶液共热时可析出硫,且金属元素转化为相应的硫酸盐(铁元素以+3价存在)。 其中MnO2和FeS发生的离子方程式为___________________________。
(2)步骤③ 中的MnO2也可用下列___________________物质代替(不考虑Mn2+的反应)
A.KMnO4 固体 B.H2O2 C.浓硝酸 D.新制氯水
(3) 步骤⑤电解过程中阳极的电极反应式为___________________________。
(4)加入化合物C后可得纯净的ZnSO4 、MnSO4溶液,C可以是ZnO或Zn(OH)2,Mn (OH)2 或MnCO3,
则产品D为___________________________(填化学式)。
(5)I .将制得的MnO2(s)与KOH(s)、KClO3(s)(按比例混合,加热熔融(不断搅拌)可得KCl和K2MnO4的固体混合物;
II.再用5%的KOH溶液溶解得绿色(MnO42-)溶液;
III.向绿色溶液中通入适量的CO2后,将溶液加热,并趁热滤去残渣( 含MnO2(s)];
IV.将滤液蒸发浓缩、冷却结品、过滤、洗涤、干燥得紫色KMnO4晶体。
①第III步操作中“趁热过滤”的目的是___________________________。
② 写出III中生成KMnO4的化学程式__________________________________。
③III中需控制CO2的用量,若CO2过量,会使所得产品的纯度降低,原因可能是___________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】给你提供纯锌片、纯铜片和100 mL 0.5 mol/L的H2SO4溶液、导线、1 000 mL量筒。试用如图装置来测定锌和稀硫酸反应时在某段时间内通过导线的电子的物质的量。
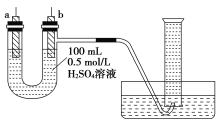
(1)如图所示,装置气密性良好,且1 000 mL量筒中已充满了水,则开始实验时,首先要____________________________。
(2)a电极材料为________,电极反应式为____________________________;b电极材料为________,电极反应式为________________________。
(3)当量筒中收集672 mL气体时(已折算到标准状况下),通过导线的电子的物质的量为________,________(填“a”或“b”)极质量减少________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. 白磷和红磷互为同素异形体 B. CH3-CH2OH和 CH3-O-CH3 互为同分异构体
C. ![]() 和
和![]() 互为同位素 D. 分子间作用力越大,分子越稳定。
互为同位素 D. 分子间作用力越大,分子越稳定。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列实验装置进行相应实验,设计正确且能达到实验目的的是

A. 用图1所示装置制取并收集少量纯净的氨气
B. 用图2 所示装置分离乙醇和乙酸乙酯的混合溶液
C. 用图3所示装置加热分解NaHCO3固体
D. 用图4 所示装置比较KMnO4、Cl2、Br2的氧化性强弱
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com