
a、b、c、d、e为元素周期表前3周期中的部分元素,它们在元素周期表中的相对位置如图所示。下列叙述正确的是( )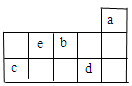
| A.b元素除0价外,只有一种化合价 |
| B.五种元素中,c元素的单质性质最稳定 |
| C.d气态氢化物的水溶液既有氧化性也有还原性 |
| D.e元素最高价氧化物对应的水化物是一种强酸,保存在无色试剂瓶里 |
C
解析试题分析:由题目提供的部分元素周期表可知:a是He;b是O;c是Si;d是Cl;e是N。A.O元素除0价外,还有-1、-2两种化合价。错误。B.在这五种元素中,a元素的原子由于处于最外层2个电子的温度结构,所以其单质性质最稳定.错误。C.Cl气态氢化物的水溶液HCl在与比较活泼的金属发生反应时,氢元素得到电子,表现氧化性,在浓HCl与MnO2或KMnO4发生反应时,Cl元素的原子失去电子,表现出还原性。故HCl既有氧化性也有还原性。正确。D.N元素最高价氧化物对应的水化物HNO3是一种强酸,同时也是一种不稳定的酸,见光容易分解,所以要保存在棕色试剂瓶里。错误。
考点:考查元素周期表元素周期律在元素形成化合物时的性质的应用的知识。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:单选题
甲、乙两种非金属,能说明甲比乙的非金属性强的是( )
①甲比乙容易与H2化合 ②甲原子能与乙阴离子发生置换反应 ③甲的最高价氧化物对应的水化物酸性比乙的最高价氧化物对应的水化物酸性强 ④与某金属反应时,甲原子得电子数目比乙的多 ⑤甲的单质熔、沸点比乙的低
| A.只有④ | B.只有⑤ | C.①②③ | D.①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
短周期元素X、Y、Z、W的原子序数依次增大,X 原子的最外层电子数是其内层电子总数的3 倍,Y 原子的最外层只有2 个电子,Z 单质可制成半导体材料,W与X属于同一主族。下列叙述正确的是
| A.元素W 的简单气态氢化物的热稳定性比X 的强 |
| B.元素W 的最高价氧化物对应水化物的酸性比Z 的弱 |
| C.化合物YX、ZX2、WX3中化学键的类型相同 |
| D.原子半径的大小顺序: r(Y)>r(Z)>r(W) >r(X) |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下表列出了某短周期元素R的各级电离能数据(用I1、I2表示,单位为kJ·mol-1)。
| | I1 | I2 | I3 | I4 | …… |
| R | 740 | 1 500 | 7 700 | 10 500 | …… |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
X、Y、Z、W为四种短周期元素,它们在周期表中的位置如图所示。Z元素原子核外第一层与第三层电子数相等。下列说法不正确的是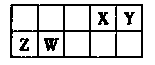
| A.与相同浓度的盐酸反应,Z单质比W单质更剧烈 |
| B.Y元素可以形成多种具有漂白性的化合物 |
| C.Y与Z、Y与W形成的化合物含有的化学键类型相同 |
| D.四种元素的离子半径大小为Z>W>X>Y |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列排列顺序正确的是
①热稳定性:H2O>HF>H2S
②原子半径:Na>Mg>F
③酸性:H3PO4>H2SO4>HClO4
④失电子能力:Na>Mg>Al
⑤晶体的熔点:SiO2>NaCl>CCl4>SO2
| A.②④⑤ | B.①②④ | C.②③⑤ | D.全部正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
短周期元素A、B、C、D的原子序数依次增大。A原子的最外层电子数是内层电子数的2倍,元素B在同周期的主族元素中原子半径最大,元素C的合金是日常生活中常用的金属材料,D位于第VIA族。下列说法正确的是
A.原子半径:D>B>C>A
B.元素A、B的氧化物具有相同类型的化学键
C.B、C、D的最高价氧化物对应的水化物能相互反应
D.元素B和C的最高价氧化物对应水化物的碱性:C>B
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
北京时间2012年9月14日,国外媒体报道,美国宇航局的“好奇”号火星车已经展开它的X射线分析器,并首次完成对火星物质元素成分的分析。下面这张图显示的是α粒子与X射线分光仪从某仪器获得的元素分析数据。多个峰值表明各种成分非常丰富,其中包括在火星大气里发现的氩,该仪器自身的铝,以及火星土壤微粒所含的硫黄和氯.
理解此图,判断下列说法错误的是
| A.峰值最高的过渡元素在周期表中的位置是第四周期第Ⅷ副族 |
B.上述元素分析图中,同一周期的两种主族元素可形成1∶1型离子化合物只有一种,其电子式为 |
| C.氯比硫的非金属性强的依据之一是HCl比H2S稳定 |
| D.工业上常用电解氧化铝的方法制备铝 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com