
【题目】一定条件下,CH4与H2O(g)发生反应:CH4(g)+H2O(g)![]() CO(g)+3H2(g),设起始
CO(g)+3H2(g),设起始![]() =Z,在恒压下,平衡时
=Z,在恒压下,平衡时![]() (CH4)的体积分数与Z和T(温度)的关系如图所示。下列说法正确的是( )
(CH4)的体积分数与Z和T(温度)的关系如图所示。下列说法正确的是( )
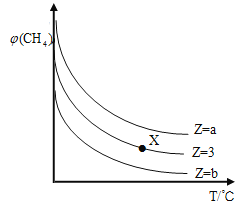
A.该反应的焓变△H﹤0
B.图中Z的大小为b >3> a
C.图中X点对应的平衡混合物中![]() =3
=3
D.温度不变时,图中X点对应的平衡在加压后![]() (CH4)减小
(CH4)减小
科目:高中化学 来源: 题型:
【题目】某同学发现,纯度、质量、表面积都相同的两铝片与c(H+)浓度相同的盐酸和硫酸在同温同压下反应时产生氢气的速率差别很大,铝与盐酸反应速率更快。他决定对其原因进行探究。
填写下列空白:
(1)该同学认为:由于预先控制了反应的其他条件,那么,两次实验时反应的速率不一样的原因,只有以下五种可能:
原因Ⅰ:Cl对反应具有促进作用,而![]() 对反应没有影响;
对反应没有影响;
原因Ⅱ:________________________________________;
原因Ⅲ:Cl对反应具有促进作用,而![]() 对反应具有阻碍作用;
对反应具有阻碍作用;
原因Ⅳ:Cl、![]() 均对反应具有促进作用,但Cl影响更大;
均对反应具有促进作用,但Cl影响更大;
原因Ⅴ:_____________________________。
(2)该同学设计并进行了两组实验,即得出了正确的结论。他取了两片等质量、外形和组成相同、表面经过砂纸打磨的铝片,分别放入到盛有同体积、c(H+)相同的稀硫酸和盐酸的试管(两试管的规格相同)中:
①在盛有硫酸的试管中加入少量NaCl或KCl 固体,观察反应速率是否发生变化;
②在盛有盐酸的试管中加入少量Na2SO4或K2SO4固体,观察反应速率是否发生变化。若观察到实验1中__________,实验2中__________,则说明原因Ⅲ是正确的。以此类推,该同学通过分析实验现象,得出了结论:Cl对反应具有促进作用。
(3)为了使实验”定量化”,使结果更精确,可以对实验进行如下改进:
①配制c(H+)相同的稀盐酸和稀硫酸:现有浓度为1 mol L1的盐酸和密度为1.225 g cm3、质量分数为20%的硫酸,若要准确量取该硫酸20.00 mL,需要用酸式滴定管(一种能够精确测量溶液体积的仪器)将量取的硫酸配制成c(H+)=l molL1的溶液,可得溶液的体积为________________________________。配制溶液时还需要用到的玻璃仪器有______________、烧杯、胶头滴管和量筒等。
②比较反应速率:反应时间可以用停表测定。如果要对上述实验中的反应速率进行比较,可以通过测定哪些物理量来确定?要求回答一种即可。_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图装置中,溶液体积均为200 ml ,开始时,电解质溶液的浓度均为0.1 mol·L-1 ,工作一段时间后,测得导线上通过了0.02 mol 电子,若不考虑溶液体积的变化,下列叙述中正确的是( )

A. (1)、(2)两装置均为电解池
B. (1)、(2)溶液的PH均减小
C. (1)中阳极电极反应式为:4OH--4e-===2H2O+O2↑
D. (1)中阴极上析出0.32 g Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 下列表述不正确的是( )
A.人造刚玉熔点很高,可用作高级耐火材料,主要成分是Al2O3
B.硅是制造太阳能电池的常用材料
C.四氧化三铁俗称铁红,可用于作油漆、红色涂料
D.分散系中分散质粒子的直径:Fe(OH)3 悬浊液>Fe(OH)3 胶体>FeCl3 溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学组装了如图所示的电化学装置,电极Ⅰ为Al,其他电极均为Cu,则下列叙述中正确的是

A.电极Ⅰ发生还原反应
B.电流方向:电极Ⅳ → ![]() → 电极Ⅰ
→ 电极Ⅰ
C.电极Ⅱ逐渐溶解
D.电极Ⅲ的电极反应:Cu2++2e-===Cu
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室迅速制备少量氯气可利用如下反应:KMnO4+HCl→KCl+MnCl2+Cl2+H2O(未配平)此反应不需要加热,常温下就可以迅速进行,而对盐酸浓度要求不高.结合本题,回答下列问题.
(1)上述反应中被氧化的物质是 , 还原产物是 .
(2)当反应有22.4LCl2(标准状况下)生成时,转移的电子的物质的量为 .
(3)Fe2+也能使KMnO4反应生成MnCl2 , 可推测Fe2+具有 . (填“氧化性”或“还原性”)
(4)如果该反应方程式中KMnO4和MnCl2的系数都是2,则HCl的系数是 .
(5)另知反应Cl2+2I﹣=I2+2Cl﹣ , 请按照氧化性由强到弱的顺序排列I2、Cl2、KMnO4三种物质: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碘是人体不可缺少的元素,为了防止碘缺乏,现在市场上流行一种加碘盐,就是在精盐中添加一定量的KIO3进去.某研究小组为了检测某加碘盐中是否含有碘,查阅了有关的资料,发现其检测原理是:在溶液中 KIO3+5KI+3H2SO4═3I2+3H2O+3K2SO4
(1)用双线桥表示该反应中电子转移的方向和数目________,该反应中还原产物与氧化产物的物质的量比是____,0.2mol KIO3参加反应时转移电子____mol。
(2)实验结束后分离I2和K2SO4溶液所用的试剂是_______。
A.CCl4 B.酒精 C.Na2SO4溶液 D.食盐水
所用的分离方法是______,所用主要玻璃仪器是_____________。
(3)上面实验中用到一定物质的量浓度的稀硫酸,若配制1mol/L的稀硫酸溶液480mL,需用18mol/L浓H2SO4____mL,配制中需要用到的主要玻璃仪器是(填序号)______。
(4)A.100mL量筒 B.托盘天平 C.玻璃棒 D.100mL容量瓶 E.50mL 量筒 F.胶头滴管 G.烧杯 H.500mL容量瓶
(5)下面操作造成所配稀硫酸溶液浓度偏高的是______________
A.溶解后溶液没有冷却到室温就转移
B.转移时没有洗涤烧杯、玻璃棒
C.向容量瓶加水定容时眼睛俯视液面
D.用量筒量取浓硫酸后洗涤量筒并把洗涤液转移到容量瓶
E.摇匀后发现液面低于刻度线,又加蒸馏水至刻度线.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com