
【题目】已知某“84消毒液”瓶体部分标签如图所示,该“84消毒液”通常稀释100倍(体积之比)后使用。请回答下列问题:

(1)某同学取10 mL该“84消毒液”,稀释后用于消毒,稀释后的溶液中c(Na+)=__________(保留2位有效数字)。
(2)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480 mL含NaClO质量分数为25%的消毒液。需要准备的实验仪器有托盘天平、药匙、烧杯、胶头滴管、__________、__________。
(3)配制时,其正确的操作顺序是__________。
A 盖好瓶塞,反复上下颠倒,摇匀
B 根据计算结果,称量NaClO固体
C 将称好的NaClO固体放入烧杯中,用适量蒸馏水溶解
D 将烧杯中的溶液注入容量瓶,用少量蒸馏水洗涤烧杯内壁2~3次,洗涤液均注入容量瓶,振荡
E 改用胶头滴管加水,使溶液凹液面恰好与刻度线相切
F 继续往容量瓶内小心加水,直到液面接近刻度线1~2 cm处
(4)下列操作使配制溶液浓度偏高的是________,使配制溶液浓度偏低的是_______,对配制溶液浓度无影响的是______(填序号)
①选用的容量瓶内有少量蒸馏水;
②定容时仰视容量瓶刻度线;
③定容时俯视容量瓶刻度线;
④烧杯中溶液倾倒完毕,忘记洗涤烧杯和玻璃棒;
【答案】0.040 500mL容量瓶 玻璃棒 BCDFEA ③ ②④ ①
【解析】
(1)c(NaClO)=![]() =
=![]() =4.0 mol/L-1,故答案为4.0;
=4.0 mol/L-1,故答案为4.0;
稀释后c(NaClO)=![]() ×4.0 mol/L-1=0.04 mol/L-1,c(Na+)=c(NaClO)=0.04 mol/L-1,
×4.0 mol/L-1=0.04 mol/L-1,c(Na+)=c(NaClO)=0.04 mol/L-1,
故答案为0.040;
(2)该同学参阅该“84消毒液”的配方,欲用NaClO固体配制480 mL含NaClO质量分数为25%的消毒液。需要准备的实验仪器有托盘天平、药匙、烧杯、胶头滴管、500ml容量瓶,玻璃棒;
故答案为500mL容量瓶,玻璃棒;
(3)一定物质的量浓度的配制步骤主要有计算,称量,溶解,冷却,转移,洗涤,定容,摇匀,故顺序是BCDFEA;
故答案为BCDFEA;
(4)①转移前,容量瓶内有蒸馏水,对实验结果没有影响;
②定容时仰视容量瓶刻度线,导致溶液体积偏大,浓度偏小;
③定容时俯视刻度线,导致溶液体积偏小,浓度偏大;
④烧杯中溶液倾倒完毕,忘记洗涤烧杯和玻璃棒,使溶质的物质的量减少,浓度偏小;
故答案为浓度偏高的是③;浓度偏低的是②④;浓度无影响的是①。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】氟的单质及含氟化合物用途非常广泛。回答下列问题:
(1)BF3常用作有机反应的催化剂,下列B原子电子排布图表示的状态中,能量最低和最高的分别为____________、_______________。(填标号)
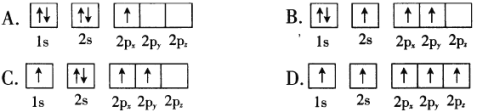
(2)NH4HF2(氟氢化铵)固态时包含的作用力有_______________(填标号)。
a.离子键 b.![]() 键 c.
键 c.![]() 键 d.氢键
键 d.氢键
(3)由反应2F2+2NaOH=OF2+2NaF+H2O可制备OF2。OF2的空间构型为___________,氧原子的杂化方式是_____________________________
(4)CsF是离子晶体,其晶格能可通过图(a)的born-Haber循环计算得到。
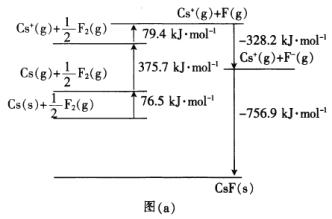
由图(a)可知,Cs原子的第一电离能为_______________________kJ·mol-1,F-F键的键能为________kJ·mol-1,CsF的晶格能为________kJ·mol-1。
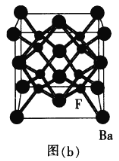
(5)BaF2晶胞是一种良好的闪烁晶体[如图(b)所示]。Ba2+的配位数为_________个;已知其密度为![]() ,则BaF2的晶胞参数为a=____________(设NA为阿伏加德罗常数的数值,列出计算式) nm。
,则BaF2的晶胞参数为a=____________(设NA为阿伏加德罗常数的数值,列出计算式) nm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】控制、治理氮氧化物对大气的污染是改善大气质量的重要方法。回答下列与雾霾治理有关的问题:
Ⅰ.(1)在催化剂作用下,甲烷可还原氮氧化物,从而达到治理氮氧化物污染的目的。已知:①CH4(g)+4NO2(g)= 4NO(g)+CO2(g)+2H2O(g) ΔH=-574 kJ·mol-1;②4NO2(g)+2N2(g)= 8NO(g) ΔH=+586 kJ·mol-1。则CH4(g)+4NO(g)= 2N2(g)+CO2(g)+2H2O(g) ΔH=________ kJ·mol-1。
(2)工业烟气中的氮氧化物可用NH3催化还原,反应原理如图所示。

其中X为一种无毒的气体,则NH3催化还原氮氧化物的化学方程式为______。
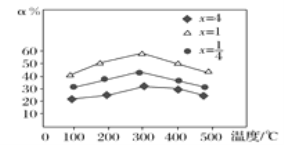
(3)用NH3催化还原烟气中的氮氧化物时,当![]() =x,用Fe作催化剂时,在NH3充足的条件下,不同x值对应的脱氮率α(被还原的氮氧化物的百分率)不同,在不同温度下其关系如图所示,当x=_____时,脱氮效果最佳,最佳的脱氮温度是____ ℃。
=x,用Fe作催化剂时,在NH3充足的条件下,不同x值对应的脱氮率α(被还原的氮氧化物的百分率)不同,在不同温度下其关系如图所示,当x=_____时,脱氮效果最佳,最佳的脱氮温度是____ ℃。
Ⅱ.(4)甲醇是一种绿色燃料,甲醇的工业合成方法较多,如CO(g)+2H2(g)![]() CH3OH(g)。在2 L恒容密闭容器中充入1 mol CO和2 mol H2混合原料气,充分反应达到平衡,测得平衡时混合物中CH3OH的体积分数与压强、温度的关系如图所示。
CH3OH(g)。在2 L恒容密闭容器中充入1 mol CO和2 mol H2混合原料气,充分反应达到平衡,测得平衡时混合物中CH3OH的体积分数与压强、温度的关系如图所示。
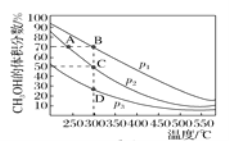
①图中压强p1、p2、p3的大小关系是_______。
②C点平衡常数K=___,A、B、D三点的平衡常数K(分别用KA、KB、KD表示)的大小关系是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家用氮化镓(GaN)材料与铜作电极组装如图所示的人工光合系统,成功地实现了以CO2和H2O合成CH4。下列说法不正确的是( )
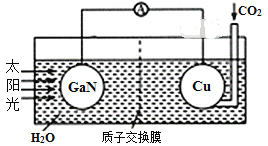
A.电子由GaN沿着导线流向Cu
B.电解液中H+从质子交换膜右侧向左侧迁移
C.GaN表面发生氧化反应,有O2产生
D.Cu表面电极反应式:CO2+8e-+8H+=CH4+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于乙醇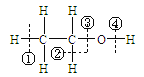 在化学反应中断键位置说法错误的是 ( )
在化学反应中断键位置说法错误的是 ( )
A. 乙醇与浓硫酸在170℃时,在②③位置断裂,以水分子的形式消去,属于消去反应。
B. 乙醇与钠反应,在④位置断裂,对比钠与水反应,乙醇比水更难失去氢离子。
C. 乙醇与浓硫酸在140℃时,在③或④位置断裂,该反应属于取代反应。
D. 乙醇在铜催化下与氧气反应,在②④位置断裂,所以只有与羟基直接相连的碳原子上有氢原子才能发生催化氧化。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在可逆反应:2A(g)+3B(g)![]() xC(g)+D(g)中,已知:起始浓度A为5mol/L,B为3mol/L,C的反应速率为0.5mol/(L·min),2min后,测得D的浓度为0.5mol/L。则关于此反应的下列说法正确的是( )
xC(g)+D(g)中,已知:起始浓度A为5mol/L,B为3mol/L,C的反应速率为0.5mol/(L·min),2min后,测得D的浓度为0.5mol/L。则关于此反应的下列说法正确的是( )
A. 2min末时A和B的浓度之比为5:3
B. x=1
C. 2min末时B的浓度为1.5mol/L
D. 2min末时A的消耗浓度为0.5mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一密闭容器中,反应aA(g)![]() bB(g)达到平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则( )
bB(g)达到平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则( )
A.平衡向正反应方向移动了
B.物质B的质量分数减小了
C.物质A的转化率减小了
D.a>b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从铝土矿(主要成分是Al2O3,含SiO2、Fe2O3、MgO等杂质)中提取氧化铝的两种工艺流程如下:
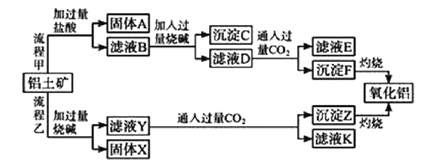
请回答下列问题:
(1)固体A的主要成分是______________(写名称)。
(2)铝土矿与过量烧碱反应的离子方程式为______________、________________。
(3)滤液D中的溶质有______________(填化学式)。
(4)指出流程乙的一个缺点是____________。
(5)氧化铝与焦炭的混合物在氮气中高温加热反应,制得新型非金属材料AlN与一种中学常见气体X。已知每转移6.02×1023个电子,有0.5mol化合物X生成,此反应的化学方程式___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com