
��������Ҫ�ɷ�ΪFeS2���ǹ�ҵ��ȡ�������Ҫԭ�ϣ������ղ���ΪSO2��Fe3O4��
��1����0.050molSO2(g)��0.030molO2(g)�����ݻ�Ϊ1L���ܱ������У���Ӧ��2SO2(g)+O2(g)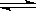 2SO3(g)��һ�������´ﵽƽ�⣬���c(SO3)=0.040mol/L������������·�Ӧ��ƽ�ⳣ��K��SO2��ƽ��ת���ʣ�д��������̣���
2SO3(g)��һ�������´ﵽƽ�⣬���c(SO3)=0.040mol/L������������·�Ӧ��ƽ�ⳣ��K��SO2��ƽ��ת���ʣ�д��������̣���
��2����֪������Ӧ�Ƿ��ȷ�Ӧ�����÷�Ӧ����ƽ��״̬ʱ�����������������£����д�ʩ�����������SO2ƽ��ת���ʵ��� ������ĸ��
A �����¶� B �����¶� C ����ѹǿ
D ��Сѹǿ E ������� G �Ƴ�����
��3��SO2β���ñ���Na2SO3��Һ���տɵõ���Ҫ�Ļ���ԭ�ϣ���Ӧ�Ļ�ѧ����ʽΪ
��
��4��������������ղ���Fe3O4����H2SO4�������ۣ����Ʊ�FeSO4�����ܹ������豣����Һ�㹻���ԣ���ԭ���� ��
���𰸡�
��1��1.6��103L/mol 80%����������ԣ�
��2��B��C
��3��SO2+H2O+Na2SO3=2NaHSO3
��4������Fe2+��Fe3+��ˮ�⣬��ֹFe2+��������Fe3+
��������������Ҫ���黯ѧƽ�ⳣ����ƽ��ת���ʵļ��㡣
2SO2(g)����+ O2(g)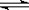 2SO3(g)
2SO3(g)
��ʼŨ��/mol��L��1 0.050 ������ 0.030 0
�仯Ũ��/mol��L��1 0.040 0.020 0.040
ƽ��Ũ��/mol��L��1 0.010 0.010 0.040
K=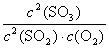 =
=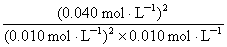 =1.6��103 L/mol
=1.6��103 L/mol
SO2��ת����=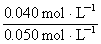 ��100%=80%
��100%=80%
����2SO2(g)+O2(g)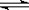 2SO3(g)������Ӧ�����������С�ķ�Ӧ��������Ӧ�Ƿ��ȷ�Ӧ��Ҫ���SO2ת����ʹƽ�������ƶ�����Ӧ�����¶Ȼ�����ѹǿ����H2SO4����Fe3+��Fe2+ˮ�⣬�ֹ���Fe��ֹFe2+��������Fe3+��FeSO4+2H2O
2SO3(g)������Ӧ�����������С�ķ�Ӧ��������Ӧ�Ƿ��ȷ�Ӧ��Ҫ���SO2ת����ʹƽ�������ƶ�����Ӧ�����¶Ȼ�����ѹǿ����H2SO4����Fe3+��Fe2+ˮ�⣬�ֹ���Fe��ֹFe2+��������Fe3+��FeSO4+2H2O Fe(OH)2+H2SO4,2Fe3++Fe===3Fe2+��
Fe(OH)2+H2SO4,2Fe3++Fe===3Fe2+��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�Ի�����Ϊԭ����������Ĺ�������ͼ���£�
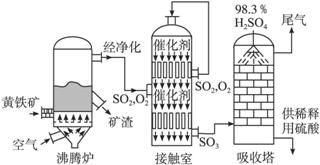
��1����ȼ�ջ�����Ļ�ѧ����ʽ��������
4________+11O2 2Fe2O3+8SO2
2Fe2O3+8SO2
(2)�Ӵ����з�����Ӧ�Ļ�ѧ����ʽ��__________________��
��3�����ݹ�������ͼ�ж�����˵����ȷ���ǣ�ѡ�������ĸ��___________��
a.Ϊʹ��������ȼ�գ��轫�����
b.�������������SO2��ת����
c.ʹ�ô��������SO2�ķ�Ӧ���ʺ�ת����
d.����¯�ų��Ŀ����ɹ�����
��4��ÿ160 g SO3������H2O���Ϸų�260.6 kJ���������÷�Ӧ���Ȼ�ѧ����ʽ��________��
��5���������ų���β�����ð�ˮ���գ�����Ũ���ᴦ�����õ��ϸ�Ũ�ȵ�SO2����Ρ�
��SO2 �ȿ���Ϊ���������ԭ��ѭ�������ã�Ҳ�����ڹ�ҵ������������ճ�ʪ�����е�Br2��SO2����Br2�����ӷ���ʽ��___________��
�ȿ���Ϊ���������ԭ��ѭ�������ã�Ҳ�����ڹ�ҵ������������ճ�ʪ�����е�Br2��SO2����Br2�����ӷ���ʽ��___________��
��Ϊ�ⶨ������е�Ԫ�ص���������������ͬ��������ηֱ���뵽50.00 mL��ͬŨ�ȵ�NaOH��Һ�У���ˮԡ����������ȫ���ݳ������¶�����β��ֽ⣩�������徭�������Ũ����������ȫ���ⶨŨ�������ӵ�������
���ֲⶨ�����
�������Ϊ10.00 g��20.00 gʱ��Ũ�������ӵ�������ͬ���������Ϊ30.00 gʱ��Ũ�������ӵ�����Ϊ0.68 g���������Ϊ40.00 gʱ��Ũ������������䡣���㣺������е�Ԫ�ص�����������___________%�����������Ϊ15.00 g��Ũ�������ӵ�����Ϊ___________����������������λС����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
������Һ��ʹ��ɫ���������ɫ���ǣ� ��
A.ϡ���� B.������ˮ
C.�Ȼ���ϡ��Һ D.������ˮ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A���ʺ�ʹ�ö��ڿθ��½̲ĵĿ������B���ʺ�ʹ��һ�ڿθĽ̲ĵĿ������
26.��A��ʵ����ģ��ϳɰ��Ͱ����������������£�

��֪ʵ���ҿ��ñ����������ƣ�NaNO2����Һ�뱥���Ȼ����Һ�����Ⱥ�Ӧ��ȡ������
��1������ͼ��ѡ����ȡ����ĺ���װ�ã�

���� ������
��2������������ͨ����װ�ã���װ�õ����ó��˽��������⣬���� �� 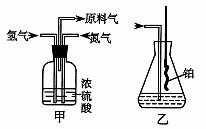
��3�����ϳ�����������ȴ����������ͨ����װ�õ�ˮ�����հ��� �����ᡱ���ᡱ������������ԭ���ǣ� ��
��4������װ������һ��ʱ�䰱����ͨ�������ͬʱ�������ȵIJ�˿������װ�õ���ƿ�ڣ���ʹ��˿���ֺ��ȵ�ԭ���ǣ� ����ƿ�л��ɹ۲쵽�������ǣ� ��
��5��д����װ���а������Ļ�ѧ����ʽ��
��6����Ӧ��������ƿ�ڵ���Һ�к���H+��OH���� �� ���ӡ�
��B��ij�����о�С�飬�ú��н϶����ʵ�ͭ�ۣ�ͨ����ͬ�Ļ�ѧ��Ӧ��ȡ����������Ƶ�ʵ�����Ϊ��
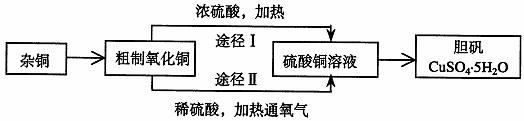
��1��ͭ�к��д������л���ɲ������յķ�����ȥ�л������ʱ������������
�ϣ����������������ı�����룬��ͬ����ȡ������Ӧʹ�� �����պ������Ӧ���� �ϣ�����ֱ�ӷ��������ϡ�
ʵ������������a ������ b ʯ���� c ������ d ������ e ����ǯ f �Թܼ�
��2����ͭ�����պ�õ��IJ���������ͭ������ͭ�Ļ���������ȡ���������պ�������ͭ�Ŀ���ԭ����
a ���չ����в�������ͭ����ԭ b ���ղ����ͭδ����ȫ����
c ����ͭ�ڼ��ȹ����зֽ�����ͭ d ��������ͭ������������
��3��ͨ��;����ʵ���ô�������ͭ��ȡ������������е�ʵ��������裺���ܡ�����ͨ���������ˡ� ����ȴ�ᾧ�� ����Ȼ����
��4���ɴ�������ͭͨ������;����ȡ��������;������ȣ�;���������Ե������ŵ��ǣ� ��
��5���ڲⶨ���õ�����CuSO4��xH2O���нᾧˮxֵ��ʵ������У������������ٽ��� ��
��6�����ⶨ���xֵƫ�ߣ����ܵ�ԭ����
a �����¶ȹ��� b ��������Ŀ����ϴ�
c ���Ⱥ���ڿ�������ȴ d �������岿�ַ绯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����г����۵�ij��ʳ�þ����ΰ�װ����������˵����
| ��Ʒ�� | GB5461 |
| ��Ʒ�ȼ� | һ�� |
| ���� | ʳ�Ρ�����ء������ |
| �⺬������I�ƣ� | 20��50mg/kg |
| ��װ���� | |
| ��װ��ҵ |
��1���������⻯�������������·������·�Ӧ����ƽ��ѧ����ʽ������ѧ���������ڿհ״�����
___KIO3+_____KI+_____H2SO4====_____K2SO4+_____I2+______H2O
��2��������Ӧ���ɵ�I2�������Ȼ�̼���顣�������Ȼ�̼��Һ�м���Na2SO3ϡ��Һ����I2��ԭ���Ի������Ȼ�̼��
��Na2SO3ϡ��Һ��I2��Ӧ�����ӷ���ʽ��_______________________________________��
��ijѧ����ƻ������Ȼ�̼�IJ�������Ϊ��
a.��������Ȼ�̼��Һ���ڷ�Һ©���У�
b.��������Na2SO3ϡ��Һ��
c.������²�Һ�塣
�����������©�IJ����������������е�λ����______________________________��
��3����֪��I2+2 ====2I-+
====2I-+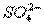 ��
��
ijѧ���ⶨʳ�þ����εĵ⺬�����䲽��Ϊ��
a.ȷ��ȡw gʳ�Σ�����������ˮʹ����ȫ�ܽ⣻
b.��ϡ�����ữ������Һ����������KI��Һ��ʹKIO3��KI��Ӧ��ȫ��
c.�Ե�����ҺΪָʾ������μ������ʵ���Ũ��Ϊ2.0��10-3 mol/L��Na2S2O3��Һ10.0 mL��ǡ�÷�Ӧ��ȫ��
���ж�c�з�Ӧǡ����ȫ���ݵ�������______________________________��
��b�з�Ӧ��������I2�����ʵ�����______________________________mol��
�۸�������ʵ��Ͱ�װ��˵�������⾫���εĵ⺬���ǣ��Ժ�w�Ĵ���ʽ��ʾ��
______________________________mg/kg��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ҵ����������ʱ�����ô�������Ӧ��SO2 ת��ΪSO3��һ���ؼ����衣ѹǿ���¶ȶ�SO2ת���ʵ�Ӱ�����±���ԭ�������ɷֵ��������Ϊ�� SO2 7% ��O2 11%��N2 82%����
SO2 7% ��O2 11%��N2 82%����
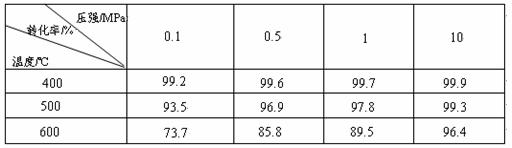
��1����֪SO2�������Ƿ��ȷ�Ӧ��������ñ��������ƶϴ˽��ۣ�
��
��2���ڴ�400��500��ʱ��SO2�Ĵ��������ó�ѹ�����Ǹ�ѹ����Ҫԭ���ǣ�
��
��3��ѡ�����˵Ĵ������Ƿ�������SO2��ת���ʣ� ����ǡ������Ƿ��������÷�Ӧ���ų��������� ����ǡ�����
��4��Ϊ���SO3�����ʣ�ʵ���������� ����SO3��
��5����֪��2SO2(g)+O2(g)��2SO3(g)����H����196.6kJ��mol��1������ÿ����1���98%��������Ҫ��SO3��������SO2������ЩSO3���ų���������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��ѧ�ҷ���C60�����ֺϳ����������η���(����ϩ)����C50��C70��C120��C540�����ǻ���Ϊ
A.ͬϵ�� B.ͬ���칹��
C.ͬ�������� D.ͬλ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�����ᣨHN3��������������ƣ����������д������
A��HN3ˮ��Һ����Ũ�ȴ�С˳��Ϊ��c(HN3)>c(H+)>c(N3¯)>c(OH¯)
B��HN3��NH3�������ɵĵ�������ǹ��ۻ�����
C��NaN3ˮ��Һ������Ũ�ȴ�С˳��Ϊ��c(Na+)>c(N3¯) >c(OH¯)>c(H+)
D��N3¯��CO2����ȵ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
NaNO2��һ��ʳƷ���Ӽ��������°�������KMnO4��Һ��NaNO2��Ӧ�����ӷ���ʽΪMnO4- + NO2- + H+ — Mn2+ + �� + H2O ��δ��ƽ��. ����������ȷ���ǣ� ��
A ��Ӧ����ҺpH�½� Bͨ���������ữ�ĸ��������Һ
C ����������ΪNO2 D. ������1 mol Mn2+ ������2.5 mol NO2-
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com