
| A、将浓度为0.1 mol?L-1HF溶液加水不断稀释过程中,c(H+)和c(OH-)都会减小 |
| B、25℃时,等体积、等pH的HCl、H2SO4、CH3COOH溶液分别与足量锌粉反应,H2SO4溶液产生的H2量最多 |
| C、Na2CO3溶液存在水解平衡:CO32-+H2O?HCO3-+OH-,加入NaOH固体会使平衡逆向移动,溶液pH减小 |
| D、25℃时,pH均为8的CH3COONa和NaOH溶液中,由水电解产生的c(OH-)之比为100:1 |
| 10 -14 |
| 10 -8 |
| 10 -8 |
| 10 -6 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 化学式 | AgCl | Ag2SO4 | Ag2S | AgBr | Agl |
| 溶度积 | 1.4×10-10 | 1.4×10-5 | 6.4×10-50 | 7.7×-13 | 8.51×10-16 |
| A、25℃时五种银盐的饱和溶液中,c(Ag+)最小的是Ag2S溶液 |
| B、25℃时,将Ag2S固体溶解到浓度为0.001mol?L-1的Na2S溶液中达到饱和,此时c(Ag+)=8.0×10-24mol?L-1 |
| C、25℃时,在等物质的量浓度的NaCl、CaCl2两溶液中加入足量的AgCl固体形成饱和溶液,则两溶液中AgCl的溶度积相同,且两溶液中c(Ag+)也相同 |
| D、AgBr沉淀可以转化成Agl沉淀,而Agl沉淀在一定条件下也可以转化成AgBr沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、已知 ,反应物X与产物Y互为同分异构体,可用溴水或FeBr3溶液鉴别X和Y ,反应物X与产物Y互为同分异构体,可用溴水或FeBr3溶液鉴别X和Y |
B、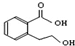 能发生的反应类型有:加成反应、取代反应、消去反应、酯化反应、水解反应 能发生的反应类型有:加成反应、取代反应、消去反应、酯化反应、水解反应 |
| C、3-甲基-3-乙基戊烷的一氯取代产物为5种 |
| D、相同条件下乙酸乙酯在水中的溶解度比在乙醇中的溶解度要大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、雾霜空气属于混合物 |
| B、微粒直径为2.5微米的细小颗粒物形成的分散系统能产生丁达尔效应 |
| C、实施绿化工程,实行汽车限行和使用清洁能源可以有效地防治PM2.5污染 |
| D、PM2.5表面积较大,能大量吸附空气中的有毒、有害物质进入人体造成伤害 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、具有还原性 |
| B、具有吸附性 |
| C、具有漂白性 |
| D、具有弱酸性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
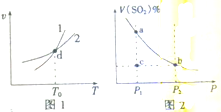 某恒容密闭容器中充入一定量SO2和O2进行反应:2SO2(g)+O2(g)?2SO3(g)△H<0.反应速率(v)与温度(T)、SO2的体积分数[v(SO2)%]与压强(P)的关系分别如图1、图2所示.下列说法不正确的是( )
某恒容密闭容器中充入一定量SO2和O2进行反应:2SO2(g)+O2(g)?2SO3(g)△H<0.反应速率(v)与温度(T)、SO2的体积分数[v(SO2)%]与压强(P)的关系分别如图1、图2所示.下列说法不正确的是( )| A、图1中,曲线Ⅰ表示逆反应速率与温度的关系 |
| B、图1中,d点表示温度为T0时,反应已经达到平衡 |
| C、图2中,温度恒定时,a、b两点对应的反应速率:va>vb |
| D、图2中,温度恒定时,c点的反应正在向逆反应方向进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 成分 | 质量(g) | 摩尔质量(g?mo-1) |
| 蔗糖 | 25.00 | 342 |
| 硫酸钾 | 0.348 | 174 |
| 阿司匹林 | 0.170 | 180 |
| 高锰酸钾 | 0.316 | 158 |
| 硝酸银 | 0.020 | 170 |
乙醇 | 9.200 | 46 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com