
【题目】某温度下,反应H2(g) + I2(g)![]() 2HI(g) + Q (Q > 0)在一带有活塞的密闭容器中达到平衡,下列说法错误的是 ( )
2HI(g) + Q (Q > 0)在一带有活塞的密闭容器中达到平衡,下列说法错误的是 ( )
A.恒容,升高温度,正反应速率减小B.恒容,充入H2(g),I2(g)的体积分数降低
C.恒压,充入He(g),逆反应速率减小D.恒温,压缩体积,平衡不移动,混合气体颜色加深
科目:高中化学 来源: 题型:
【题目】2019年是“国际化学元素周期表年”。1869年门捷列夫把当时己知的元素根据物理、化学性质进行排列,准确预留了甲、乙两种未知元素的位置,并预测了二者的相对原子质量,部分原始记录如下。

下列说法不正确的是
A.元素甲比Al的最高价氧化物的水化物的碱性弱B.原子半径比较:甲>乙>Si
C.元素乙位于现行元素周期表第四周期第ⅣA族D.推测乙可以用作半导体材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学在实验室中称取20gNaOH固体,配制500mL1mol·L-1的氢氧化钠溶液。
(1)该同学准备的实验用品有:托盘天平![]() 带砝码
带砝码![]() 、药匙、量筒、玻璃棒等,还缺少的玻璃仪器有__、__、___。
、药匙、量筒、玻璃棒等,还缺少的玻璃仪器有__、__、___。
(2)下列有关实验操作,正确的是__。(多选)
A.称量氢氧化钠固体时,应该放在称量纸上称量
B.某同学将称量的氢氧化钠固体溶解并冷却至室温,然后转移到容量瓶中
C.某同学在定容时,不小心加水超过刻度线,又将多余的液体吸出直至刻度线
D.某同学在溶解、转移完氢氧化钠溶液后,将溶解用的仪器洗涤2~3次,并将洗涤液转移到容量瓶中
(3)玻璃棒在该实验中的作用有①__,②___。
(4)若实验室遇到下列情况,对氢氧化钠溶液的物质的量浓度有何影响![]() 填“偏高”、“偏低”或“无影响”
填“偏高”、“偏低”或“无影响”![]()
①转移时,有少量的溶液洒落出容量瓶__。
②定容时,容量瓶中事先有洁净的蒸馏水,所配溶液的浓度___。
③定容时俯视溶液的凹液面___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用Na2FeO4溶液氧化废水中的还原性污染物M,为研究降解效果,设计如下对比实验探究温度、浓度、 pH、催化剂对降解速率和效果的影响,实验测得M的浓度与时间关系如图所示:
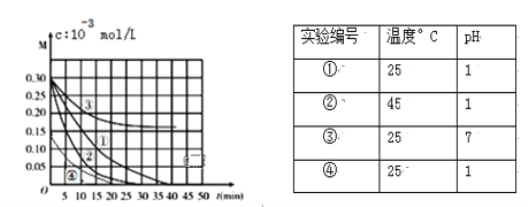
下列说法正确的是
A. 实验①在15 min内M的降解速率为1.33×10-2mol/(L·min)
B. 若其他条件相同,实验①②说明升高温度,M降解速率增大
C. 若其他条件相同,实验①③证明pH越高,越有利于M的降解
D. 实验②④说明M的浓度越小,降解的速率越慢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《我不是药神》中的“格列宁”是一种抗癌药。同样是抗癌药物"6-Azulenol”的结构简式如图所示,下列有关叙述错误的是 ( )
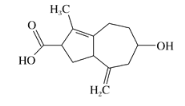
A.分子式为C13H18O3
B.能发生加成、氧化、酯化反应
C.能使溴水、酸性高锰酸钾溶液褪色
D.1mol该物质与足量的Na反应可产生11.2LH2(已换算成标准状况)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在微生物作用下,蛋白质在水中分解产生的氨能够被氧气氧化生成亚硝酸(HNO2),该反应的化学方程式为________;若反应中有0.3mol电子发生转移时,生成亚硝酸的质量为_______g (保留两位小数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】丙烯腈(CH2=CHCN)是一种重要的化工原料,工业上可用“丙烯氨氧化法”生产,主要副产物有丙烯醛(CH2=CHCHO)和乙腈(CH3CN)等,回答下列问题:
(1)用于生产丙烯腈的原料丙烯具有一定的危险性。某市化工园区曾发生一起丙烯储罐突然爆炸起火事件,大火产生的高温使消防队员难以靠近火场。已知丙烯的燃烧热为2049 kJ/mol,则其燃烧反应的热化学方程式为:____________________。
(2)图(a)为丙烯腈产率与反应温度的关系曲线,最高产率对应温度为460℃。低于460℃时,丙烯腈的产率________(填“是”或者“不是”)对应温度下的平衡产率,判断理由是_____________________;高于460℃时,丙烯腈产率降低的可能原因是________(双选,填标号)
A.催化剂活性降低 B.平衡常数变大 C.副反应增多 D.反应活化能增大
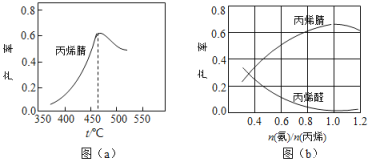
(3)丙烯腈和丙烯醛的产率与![]() 的关系如图(b)所示。由图可知最佳
的关系如图(b)所示。由图可知最佳![]() 约为________,理由是___________________。进料气氨、空气、丙烯的理论体积比约为________。
约为________,理由是___________________。进料气氨、空气、丙烯的理论体积比约为________。
(4)现以丙烯为原料,合成环状酯J。有关工艺流程图如下。已知:烯烃复分解反应是指在催化剂作用下,实现碳—碳双键两边基团换位的反应。如两个丙烯分子进行烯烃换位,生成丁烯和乙烯。
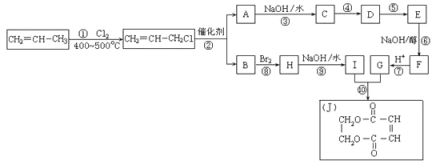
参考化学方程式:2CH2=CHCH3![]() CH3CH=CHCH3+CH2=CH2
CH3CH=CHCH3+CH2=CH2
i.①的反应类型是_____________,物质E的结构简式是___________。
ii.有机化合物C有多种同分异构体,请写出其中属于酯类且能发生银镜反应的所有同分异构体的结构简式__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤素的单质和化合物种类很多,我们可以利用所学物质结构与性质的相关知识去认识和理解它们。回答下列问题:
(1)溴原子的价层电子排布图为_______。根据下表提供的第一电离能数据,判断最有可能生成较稳定的单核阳离子的卤素原子是________(填元素符号)。
氟 | 氯 | 溴 | 碘 | |
第一电离能/ (kJ·mol-1) | 1 681 | 1 251 | 1 140 | 1 008 |
(2)氢氟酸在一定浓度的溶液中主要以二分子缔合[(HF)2]形式存在,使氟化氢分子缔合的相互作用是____________。碘在水中溶解度小,但在碘化钾溶液中明显增大,这是由于发生反应:I-+I2=I3-,CsICl2与KI3类似,受热易分解,倾向于生成晶格能更大的物质,试写出CsICl2受热分解的化学方程式:_________________________________。
(3)ClO2-中心氯原子的杂化轨道类型为________,与ClO2-具有相同立体构型和键合形式的物质的化学式为____________(写出一个即可)。
(4)如图甲为碘晶体晶胞结构,平均每个晶胞中有________个碘原子,碘晶体中碘分子的配位数为____________。
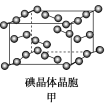
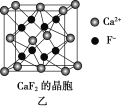
(5)已知NA为阿伏加德罗常数,CaF2晶体密度为ρ g·cm-3,其晶胞如图乙所示,两个最近Ca2+核间距离为a nm,则CaF2的相对分子质量可以表示为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】使一镁铝合金粉末在过量稀H2SO4中溶解,在所得溶液中加入NaOH溶液,生成沉淀的质量w和加入NaOH溶液的体积V的关系如图所示,则该合金中镁和铝的质量之比为( )
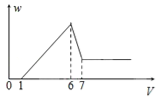
A. 2:3 B. 1:1 C. 4:3 D. 8:9
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com