
【题目】下列盐的水溶液呈酸性的是( )
A.NaClB.Na2CO3C.CH3COONaD.AlCl3
科目:高中化学 来源: 题型:
【题目】一定温度下,在三个体积均为2.0L的恒容密闭容器中分别加入一定量的X,发生反应:pX(g) ![]() Y(g)+Z(g),相关数据如下表所示:
Y(g)+Z(g),相关数据如下表所示:
容器编号 | 温度(℃) | 起始物质的量(mol) | 平衡物质的量(mol) | |
X(g) | Y(g) | Z(g) | ||
Ⅰ | 387 | 0.20 | 0.080 | 0.080 |
Ⅱ | 387 | 0.40 | 0.160 | 0.160 |
Ⅲ | T | 0.20 | 0.090 | 0.090 |
回答下列问题:
(1)若容器Ⅰ中反应经10min达到平衡,则前10min内Y的平均反应速率v(Y)=___________。容器Ⅰ和容器Ⅱ中起始时X的反应速率v(X)Ⅰ___________v(X)Ⅱ(填“大于”“小于”或“等于”)。
(2)已知该正反应为放热反应,则T___________387(填“大于”或“小于”),判断理由是___________。
(3)反应方程式中X的化学计量数p的取值为___________,容器Ⅱ中X的平衡转化率为___________。若起始时向容器Ⅰ中充入0.1molX、0.15molY和0.10molZ,则反应将向___________ (填“正”或“逆”)反应方向进行,判断理由是_____________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质按酸、碱、盐、氧化物顺序分类正确的是( )
A.硫酸、纯碱、石膏、铁红
B.醋酸、烧碱、纯碱、生石灰
C.碳酸、熟石膏、小苏打、三氧化硫
D.氯化氢、苛性钠、氯化钠、石灰石
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向某密闭容器中加入0.3molA、0.1molC和一定量的B三种气体.一定条件下发生反应,各物质浓度随时间变化如甲图所示(t0~t1阶段的c(B)变化未画出).乙图为t时刻后改变条件平衡体系中正、逆反应速率随时间变化的情况,且四个阶段都各改变一种反应条件(浓度、温度、压强、催化剂)且互不相同,t3~t4阶段为使用催化剂.下列说法中不正确的是
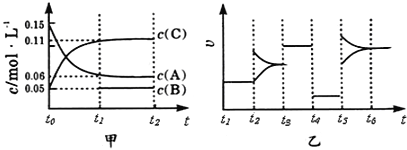
A. 若t1=15s,则用C的浓度变化表示的t0~t1段的平均反应速率为0.004molL-1s-1
B. t4~t5阶段改变的条件一定为减小压强
C. 该容器的容积为2L,B的起始物质的量为0.02mol
D. 该化学反应方程式为3A(g)B(g)+2C(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碲(Te)位于元素周期表第ⅥA族,该元素组成的物质可用作石油裂化的催化剂、电镀液的光亮剂、玻璃的着色材料及合金材料的添加剂等。精炼铜的阳极混含有Cu2Te、Au、Ag等,利用下列工艺流程可回收碲:
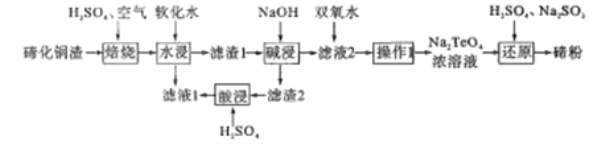
已知:TeO2熔点733℃,微溶于水,可溶于强酸和强碱。回答下列问题:
(1)Te与S的简单氢化物的稳定性强弱顺序为:__________(用氢化物的化学式表示)。
(2)“焙烧”的化学方程式__________(碲主要以TeO2形式存在)。
(3)“焙烧”后的固体用软化水“水浸”,该过程的有效物质的浸出率及浸出速率对该工艺流程很重要,写出两条提高“水浸”速率的措施:________。“滤液1”的溶质有________。
(4)“滤渣1”进行“碱浸”的目的是________
(5)“滤液2”加入双氧水,能否改用氯水或氯气,说明原因:_________
(6)“还原”制备碲粉的氧化产物是_________
(7)从环境保护和资源合理开发的可持续发展意识和绿色化学观念来看,分析“滤渣2”进行“酸浸”的意义:________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,某兴趣小组用下图装置在通风橱中进行如下实验:
实验 | 现象 |
| 试管中开始无现象,逐渐有微小气泡生成,越来越剧烈,液面上方出现浅红棕色气体,溶液呈蓝色. |
试管中剧烈反应,迅速生成大量红棕色气体, 溶液呈绿色;之后向绿色溶液中持续通入N2, 溶液变为蓝色. |
下列说法正确的是
A. 试管Ⅰ中浅红棕色气体为NO2,由硝酸还原生成
B. 等质量的 Cu 完全溶解时,Ⅰ中消耗的HNO3更多
C. 换成Fe之后重复实验,依然是试管Ⅱ中反应更剧烈
D. 试管Ⅱ中反应后溶液颜色与试管Ⅰ中的不同,是由于溶有NO2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com