
【题目】碲(Te)位于元素周期表第ⅥA族,该元素组成的物质可用作石油裂化的催化剂、电镀液的光亮剂、玻璃的着色材料及合金材料的添加剂等。精炼铜的阳极混含有Cu2Te、Au、Ag等,利用下列工艺流程可回收碲:
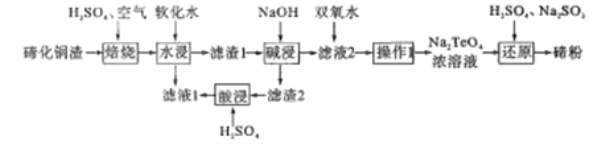
已知:TeO2熔点733℃,微溶于水,可溶于强酸和强碱。回答下列问题:
(1)Te与S的简单氢化物的稳定性强弱顺序为:__________(用氢化物的化学式表示)。
(2)“焙烧”的化学方程式__________(碲主要以TeO2形式存在)。
(3)“焙烧”后的固体用软化水“水浸”,该过程的有效物质的浸出率及浸出速率对该工艺流程很重要,写出两条提高“水浸”速率的措施:________。“滤液1”的溶质有________。
(4)“滤渣1”进行“碱浸”的目的是________
(5)“滤液2”加入双氧水,能否改用氯水或氯气,说明原因:_________
(6)“还原”制备碲粉的氧化产物是_________
(7)从环境保护和资源合理开发的可持续发展意识和绿色化学观念来看,分析“滤渣2”进行“酸浸”的意义:________
【答案】 H2S>H2Te Cu2Te+2H2SO4+2O2![]() 2CuSO4+TeO2+2H2O 固体粉碎、适当提高水的温度 CuSO4、H2SO4 制备TeO32-(或溶解TeO2) 不能,Na2TeO4中含NaCl杂质,且氯水或氯气有毒 Na2SO4 “酸浸”的滤液中含CuSO4,滤渣中的Au、Ag均能进行回收。符合绿色化学的现点
2CuSO4+TeO2+2H2O 固体粉碎、适当提高水的温度 CuSO4、H2SO4 制备TeO32-(或溶解TeO2) 不能,Na2TeO4中含NaCl杂质,且氯水或氯气有毒 Na2SO4 “酸浸”的滤液中含CuSO4,滤渣中的Au、Ag均能进行回收。符合绿色化学的现点
【解析】(1)同主族元素从上到下氢化物稳定性逐渐减弱,Te与S的简单氢化物的稳定性强弱顺序为H2S>H2Te ;(2)Cu2Te氧化成CuSO4和TeO2,“焙烧”的化学方程式Cu2Te+2H2SO4+2O2![]() 2CuSO4+TeO2+2H2O;(3)“焙烧”后的固体用软化水“水浸”,该过程的有效物质的浸出率及浸出速率对该工艺流程很重要,写出两条提高“水浸”速率的措施:固体粉碎、适当提高水的温度。“滤液1”的溶质有CuSO4、H2SO4;(4)TeO2是酸性氧化物,与碱反应生成盐和水,“滤渣1”进行“碱浸”的目的是制备TeO32-(或溶解TeO2);(5)“滤液2”加入双氧水,不能改用氯水或氯气,原因:Na2TeO4中含NaCl杂质,且氯水或氯气有毒;(6)用Na2SO3“还原”制备碲粉的氧化产物是Na2SO4;(7)从环境保护和资源合理开发的可持续发展意识和绿色化学观念来看,“滤渣2”进行“酸浸”的意义:“酸浸”的滤液中含CuSO4,滤渣中的Au、Ag均能进行回收。符合绿色化学的现点。
2CuSO4+TeO2+2H2O;(3)“焙烧”后的固体用软化水“水浸”,该过程的有效物质的浸出率及浸出速率对该工艺流程很重要,写出两条提高“水浸”速率的措施:固体粉碎、适当提高水的温度。“滤液1”的溶质有CuSO4、H2SO4;(4)TeO2是酸性氧化物,与碱反应生成盐和水,“滤渣1”进行“碱浸”的目的是制备TeO32-(或溶解TeO2);(5)“滤液2”加入双氧水,不能改用氯水或氯气,原因:Na2TeO4中含NaCl杂质,且氯水或氯气有毒;(6)用Na2SO3“还原”制备碲粉的氧化产物是Na2SO4;(7)从环境保护和资源合理开发的可持续发展意识和绿色化学观念来看,“滤渣2”进行“酸浸”的意义:“酸浸”的滤液中含CuSO4,滤渣中的Au、Ag均能进行回收。符合绿色化学的现点。


科目:高中化学 来源: 题型:
【题目】某化学研究小组探究外界条件对化学反应mA(g)+nB(g)![]() pC(g)的速率和平衡的影响图像如下,下列判断正确的是
pC(g)的速率和平衡的影响图像如下,下列判断正确的是

A. 由图1可知,T1<T2,该反应正反应为吸热反应
B. 由图2可知,该反应m+n<p
C. 图3中,点3的反应速率V正>V逆
D. 图4中,若m+n=p,则a曲线一定使用了催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,CH4与H2O(g)发生反应:CH4(g)+H2O(g)![]() CO(g)+3H2(g),设起始
CO(g)+3H2(g),设起始![]() =Z,在恒压下,平衡时
=Z,在恒压下,平衡时![]() (CH4)的体积分数与Z和T(温度)的关系如图所示。下列说法正确的是
(CH4)的体积分数与Z和T(温度)的关系如图所示。下列说法正确的是
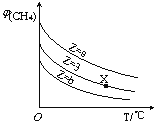
A.该反应的焓变△H>0
B.图中Z的大小为a>3>b
C.图中X点对应的平衡混合物中![]() =3
=3
D.温度不变时,图中X点对应的平衡在加压后![]() (CH4)减小
(CH4)减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,将4molA和3molB充入体积为1L的密闭容器中,发生如下反应:aA(g)+2B(g)![]() 3C(g)+D(g)。反应达到平衡后,C的浓度为3mol/L.压缩容器体积,使容器的体积减小一半,建立新的平衡时,B的浓度为2mol/L.则方程式中a的数值为
3C(g)+D(g)。反应达到平衡后,C的浓度为3mol/L.压缩容器体积,使容器的体积减小一半,建立新的平衡时,B的浓度为2mol/L.则方程式中a的数值为
A. 1 B. 2 C. 3 D. 4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有两种金属混合物3.4g,与足量的盐酸反应放出H22.24L(标况下),这两种金属可能是
A. 铜和铁 B. 镁和铝 C. 锌和铝 D. 锌和铁
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温同压下,等质量的 SO2气体和 SO3气体相比较,正确的说法是
A. 密度比为 4:5 B. 物质的量之比为 4:5
C. 体积比为 1:1 D. 原子数之比为 3:4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设N A 代表阿伏加德罗常数的值,下列说法正确的是
A. 1 mol Na在空气中完全燃烧,转移的电子数为2 N A
B. 常温下,2.7 g铝与足量NaOH溶液反应,消耗0.1 N A个OH-
C. 0.1 mol Fe 与足量水蒸气反应,生成H2的分子数为0.1 N A
D. 11.2 L Cl2含有的原子数为N A
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com