
【题目】合成氨工业对国民经济和社会发展具有重要的意义。其原理为:N2(g)+3H2(g) ![]() 2NH3(g) ΔH=-Q kJ/mol(Q>0)
2NH3(g) ΔH=-Q kJ/mol(Q>0)
据此回答以下问题:
(1)①该反应的化学平衡常数表达式为K=________。
②根据温度对化学平衡的影响规律可知,对于该反应,温度越高,其平衡常数的值越________。
(2)对于合成氨反应而言,下列有关图像一定正确的是(选填序号)________。
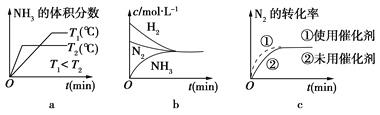
(3)某温度下,若把2 mol N2与6 mol H2置于体积为1 L的密闭容器内,反应达到平衡状态时,测得混合气体中氨的体积分数为20%,则该温度下反应的K=________(可用分数表示)。
(4)相同温度下,有恒容密闭容器A和恒压密闭容器B,两容器中均充入1 mol N2和3 mol H2,此时两容器的体积相等。在一定条件下反应达到平衡状态,A中NH3的体积分数为a,放出热量Q1 kJ;B中NH3的体积分数为b,放出热量Q2 kJ。则:a________b(填“>”、“=”或“<”,下同),Q1________Q2,Q1_______Q。
【答案】 ![]() 小 a、c 1/48 < < <
小 a、c 1/48 < < <
【解析】试题分析:(1)①化学平衡常数=![]() ;②该反应放热,升高温度平衡逆向移动;(2)该反应放热,升高温度平衡逆向移动,温度越高氨气的体积分数越小;达到平衡时氮气、氢气、氨气的浓度不一定相等;加入催化剂能加快反应速率,但平衡不移动;(3)利用“三段式”计算平衡常数;(4)合成氨反应,气体系数和减小,恒压密闭容器与恒容密闭容器相比,恒压密闭容器相当于加压;
;②该反应放热,升高温度平衡逆向移动;(2)该反应放热,升高温度平衡逆向移动,温度越高氨气的体积分数越小;达到平衡时氮气、氢气、氨气的浓度不一定相等;加入催化剂能加快反应速率,但平衡不移动;(3)利用“三段式”计算平衡常数;(4)合成氨反应,气体系数和减小,恒压密闭容器与恒容密闭容器相比,恒压密闭容器相当于加压;
解析:(1)①N2(g)+3H2(g) ![]() 2NH3(g) 化学平衡常数表达式
2NH3(g) 化学平衡常数表达式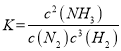 ;②该反应放热,升高温度平衡逆向移动,所以温度越高,其平衡常数的值越小;(2)该反应放热,升高温度平衡逆向移动,温度越高氨气的体积分数越小,根据图像a,
;②该反应放热,升高温度平衡逆向移动,所以温度越高,其平衡常数的值越小;(2)该反应放热,升高温度平衡逆向移动,温度越高氨气的体积分数越小,根据图像a, ![]() ,
, ![]() 时氨气的体积分数减小,故a正确;达到平衡时氮气、氢气、氨气的浓度不一定相等,故b错误;加入催化剂能加快反应速率,但平衡不移动,故c正确;
时氨气的体积分数减小,故a正确;达到平衡时氮气、氢气、氨气的浓度不一定相等,故b错误;加入催化剂能加快反应速率,但平衡不移动,故c正确;
(3)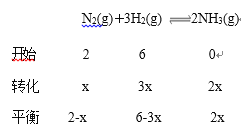
![]()
x=![]() ,
, 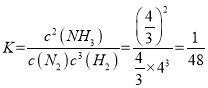 ;
;
(4)合成氨反应,气体系数和减小,恒压密闭容器与恒容密闭容器相比,恒压密闭容器相当于加压,加压平衡正向移动,所以a<b;生成氨气越多,放出的热量越多,所以Q1<Q2;反应可逆,所以1 mol N2和3 mol H2不能完全反应生成2mol氨气,所以Q1<Q。


 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案科目:高中化学 来源: 题型:
【题目】有机物M为海洋天然产物(一)-PavidolideB不对称全合成的中间体之一,结构简式如下图。下列有关M的说法不正确的是

A. 分子式为C10H14O
B. 可发生取代反应加成反应、聚合反应
C. 分子中所有碳原子都在同一平面上
D. 苯环上连有-OH和-C4H9的M的同分异构体有12种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上通过电化学原理在铝片表面形成氧化膜来提高其抗腐蚀能力,工作原理如下图所示。列说法正确的是
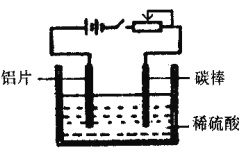
A. 碳棒可用任意金属代替,其作用是传递电流
B. 通电一段时间后,溶液的pH增大
C. 通电后电子被强制从碳棒流向铝片使铝表面形成氧化膜
D. 可通过调节滑动变阻器来控制氧化膜的形成速度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知热化学方程式:H+(aq)+OH-(aq)===H2O(l) ΔH1=-57.3 mol·L-1;![]() H2SO4(浓)+NaOH(aq)===
H2SO4(浓)+NaOH(aq)===![]() Na2SO4(aq)+H2O(l) ΔH2=m,下列说法不正确的是
Na2SO4(aq)+H2O(l) ΔH2=m,下列说法不正确的是
A. 上述热化学方程式中的计量数表示分子数。
B. ΔH1>ΔH2
C. ΔH2应为![]() H2SO4(浓)溶于水的能量变化与中和热之和。
H2SO4(浓)溶于水的能量变化与中和热之和。
D. |ΔH1|〈|ΔH2|
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为研究金属腐蚀的条件和速率,某课外小组学生用金属丝将三根大小相同的铁钉分别固定在图示的三个装置中,再放置于玻璃钟罩内保存一星期后,下列对实验结束时现象描述不正确的是( )

A. 装置Ⅰ左侧的液面一定会上升 B. 左侧液面装置Ⅰ比装置Ⅱ的低
C. 装置Ⅱ中的铁钉腐蚀最严重 D. 装置Ⅲ中的铁钉几乎没被腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业废气、汽车尾气排放出的SO2、NOx等,是形成雾霾的重要因素.霾是由空气中的灰尘、硫酸、硝酸、有机碳氢化合物等粒子形成的烟雾.
(1)SO2在烟尘的催化下形成硫酸的反应方程式是______________.
(2)NOx和SO2在空气中存在下列平衡:
2NO(g)+O2(g)2NO2(g)△H=﹣113.0kJmol﹣1
2SO2(g)+O2(g)2SO3(g)△H=﹣196.6kJmol﹣1
SO2通常在二氧化氮的存在下,进一步被氧化,生成SO3.
①写出NO2和SO2反应的热化学方程式为_________.
②随温度升高,该反应化学平衡常数变化趋势是_____.
(3)提高2SO2+O22SO3反应中SO2的转化率,是减少SO2排放的有效措施.
①T温度时,在1L的密闭容器中加入2.0mol SO2和1.0mol O2,5min后反应达到平衡,二氧化硫的转化率为50%,该反应的平衡常数是____.
②在①中条件下,反应达到平衡后,改变下列条件,能使SO2的转化率提高的是_____(填字母).
a.温度和容器体积不变,充入1.0mol He b.温度和容器体积不变,充入1.0mol O2
c.在其他条件不变时,减少容器的体积 d.在其他条件不变时,改用高效催化剂
e.在其他条件不变时,升高体系温度
(4)工业上利用氯碱工业产品治理含二氧化硫的废气.如图是氯碱工业中电解饱和食盐水的原理示意图。

①电解饱和食盐水的化学方程式是________________.
②用溶液A吸收含二氧化硫的废气,其反应的离子方程式是_________.
③用含气体B的阳极区溶液吸收含二氧化硫的废气,其反应的离子方程式是___________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com