
【题目】下列应用与盐类的水解无关的是( )
A.明矾净水B.配制FeCl3溶液时加入适量盐酸
C.NaCl可用作防腐剂和调味剂D.泡沫灭火器的灭火原理
科目:高中化学 来源: 题型:
【题目】某工业残渣主要成分为Fe2O3(含有少量FeO、Cu、Mg等杂质)。某课外兴趣小组利用该残渣制取Fe2O3粉末的流程如下:(说明:流程中“向黄色溶液加入MgO”的目的是调节溶液的酸碱性,使Fe3+生成沉淀而Mg2+不沉淀。)
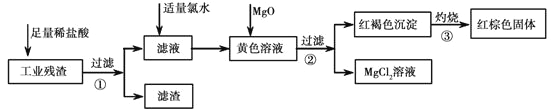
请回答下列问题:
(1)加入足量稀盐酸后,发生化学反应的类型有_____________(填写代号)。
A. 氧化还原反应 B.化合反应 C.分解反应 D.复分解反应
(2)加入适量氯水的作用是____________________________.
(3)写出灼烧红褐色沉淀时发生反应的化学方程式_____________________。实验室灼烧红褐色沉淀可选用的装置是__________(填序号)。

(4)若向黄色溶液中加入过滤①后的滤渣,发生反应的离子方程式为___________。
(5)检验黄色溶液中Fe3+是否完全沉淀的方法是:取过滤②后的少量滤液于试管中,____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于有机物的说法正确的是
A. 石油分馏可获得乙烯、苯及其衍生物
B. 苯、乙醇和乙烯都能发生加成反应
C. 用新制的Cu(OH)2悬浊液可检验尿液中的葡萄糖
D. 纤维素水解与淀粉水解得到的最终产物不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学查阅资料获悉:用KMnO4可以测定H2O2的物质的量浓度:取15.00mL H2O2溶液,用稀H2SO4酸化;逐滴加入0.003mol·L-1KMnO4溶液,产生气体,溶液褪色速率开始较慢后变快,至恰好完全反应时共消耗20.00 mL KMnO4溶液。该反应的离子方程式是:2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O;
(1)该反应体现了H2O2的__________(填“氧化性”、“还原性”或“氧化性和还原性”);
(2)KMnO4溶液褪色速率开始较慢,后变快的原因可能是某种物质对该反应起到了催化作用,则该物质最有可能是________;(填序号) a. MnO4- b.H+ c.Mn2+ d.K+
(3)判断完全反应的现象是_________________________________________________;
(4)该H2O2溶液的物质的量浓度是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A. 用铜作印刷电路是利用了铜的还原性
B. 利用铝热反应来焊接钢轨
C. 羊毛、蚕丝、棉花的主要成分都是纤维素
D. 生铁和普通钢都是铁碳合金
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组的同学利用如图所示的量热计完成中和反应反应热的测定实验。

实验用品:
浓硫酸、0.55 mol·L1的NaOH溶液、蒸馏水、自制量热计(如图)、烧杯、滴管、玻璃棒、量筒等。
实验步骤:
①配制0.25 mol·L1的硫酸溶液250 mL;
②分别量取0.25 mol·L1的硫酸、0.55 mol·L1的NaOH溶液各50 mL,并测量其起始温度;
③将二者于自制量热计中小心混合,测出反应过程中的温度,并作好记录;
④重复②、③步骤两次;
⑤处理数据得到如图所示曲线。

据此回答下列问题:
(1)量热计的插孔A中应插入的一种玻璃仪器是________。
(2)步骤①中除用到实验用品所列部分仪器外,还会用到的玻璃仪器是________。
(3)计算中和反应反应热ΔH时,所使用的温度数据Δt=________。
(4)若实验中用60 mL 0.25 mol·L1硫酸溶液和50 mL 0.55 mol·L1 NaOH溶液进行实验,与上述实验相比,所测得的中和反应反应热________(填“相等”或“不相等”);若用50 mL 0.50 mol·L1醋酸溶液代替硫酸溶液进行上述实验,测得反应前后溶液温度的变化值会________(填“偏大”“偏小”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在现行元素周期表中,所含元素种数最多的族和周期分别是( )
A. 第ⅠA族 第六周期
B. 第Ⅷ族 第六周期
C. 第ⅢB族 第六周期
D. 第ⅢA族 第六周期
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、有下列五种烃;①![]() ②
②![]() ③乙烷 ④戊烷 ⑤
③乙烷 ④戊烷 ⑤![]() ,其中互为同分异构体的是____________(填序号),②与⑤之间的关系为_____________,
,其中互为同分异构体的是____________(填序号),②与⑤之间的关系为_____________,
②③④⑤四种物质按它们的沸点由高到低的顺序排列正确的是_____________(填序号)
Ⅱ、某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A在一定条件下可发生如图所示的转化,请回答下列问题;

(1)写出A的电子式________,E的结构简式为______________
(2)写出下列反应化学方程式,并注明③⑤反应类型
② _____________________________________________
③ _____________________ ,反应类型________;
⑤ _____________________ ,反应类型________;
(3)除去B中混有的少量杂质A,所用的试剂为___________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com