
【题目】某化学兴趣小组的同学利用如图所示的量热计完成中和反应反应热的测定实验。

实验用品:
浓硫酸、0.55 mol·L1的NaOH溶液、蒸馏水、自制量热计(如图)、烧杯、滴管、玻璃棒、量筒等。
实验步骤:
①配制0.25 mol·L1的硫酸溶液250 mL;
②分别量取0.25 mol·L1的硫酸、0.55 mol·L1的NaOH溶液各50 mL,并测量其起始温度;
③将二者于自制量热计中小心混合,测出反应过程中的温度,并作好记录;
④重复②、③步骤两次;
⑤处理数据得到如图所示曲线。

据此回答下列问题:
(1)量热计的插孔A中应插入的一种玻璃仪器是________。
(2)步骤①中除用到实验用品所列部分仪器外,还会用到的玻璃仪器是________。
(3)计算中和反应反应热ΔH时,所使用的温度数据Δt=________。
(4)若实验中用60 mL 0.25 mol·L1硫酸溶液和50 mL 0.55 mol·L1 NaOH溶液进行实验,与上述实验相比,所测得的中和反应反应热________(填“相等”或“不相等”);若用50 mL 0.50 mol·L1醋酸溶液代替硫酸溶液进行上述实验,测得反应前后溶液温度的变化值会________(填“偏大”“偏小”或“无影响”)。
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案科目:高中化学 来源: 题型:
【题目】CO(NH2) 2(尿素)在工业生产中可用于制氢、脱硫脱硝等。回答下列问题:

(1)用惰性电极电解尿素制氢的装置如图所示。
①应将尿素加入该电解池的________(填“阳极”或“阴极”)。
②阴极的电极反应式为________。
③当生成1 mol H2时,消耗尿素________g。
(2)尿素/次氯酸钙溶液可用于脱硫脱硝。
①若脱硝时,尿素将等物质的量的N0和N02转化为N (次氯酸钙作催化剂),则 n(N0): n(N02):C0(NH2)2]=________。
②向尿素/次氯酸钙溶液中加入熟石灰可提高脱硫脱硝率,其原因是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列是物质的量概念及其相关计算的内容,完成相关填空:
(1)标准状况下,① 4 g氢气、②33.6 L甲烷、③6.02×1023个水分子中,含分子数最多的是(填序号,下同)_______,含原子数最多的是_________,质量最大的是___________,体积最小的是___________。
(2)在标准状况下,1L的密闭容器中恰好可盛放n个N2分子和m个H2分子组成的混合气体,则阿伏加德罗常数可表示为___________。
(3)19 g某二价金属的氯化物ACl2中含有0.4 mol Cl-,A的相对原子质量是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于构成细胞的化学元素的叙述,错误的是
A. 占细胞干重和鲜重百分比最多的元素分别是C和0
B. 不同生物细胞中的化学元素在种类上基本相同
C. 绿色植物缺Mg对其生命活动基本没有影响
D. 组成细胞的元素大多以化合物形式存在
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿魏酸在食品、医药等方面有着广泛用途。已知一种合成阿魏酸的反应可表为:

对以上反应说法正确的是
A. 可用酸性KMnO4溶液检测上述反应是否有阿魏酸生成
B. 香兰素、阿魏酸均可与Na2CO3、NaOH 、NaHCO3溶液反应
C. 通常条件下,香兰素、阿魏酸都能发生取代、加成、消去反应
D. 与香兰素互为同分异构体分子中有4种不同化学环境的氢,能消2molNaOH溶液且能发生银镜反应的酚类化合物共有2种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物的结构可用“键线式”简化表示。如CH3—CH=CH—CH3,可简写为![]() 。有机物X的键线式为
。有机物X的键线式为![]() 。下列说法不正确的是( )
。下列说法不正确的是( )
A. X的化学式为C8H8
B. 有机物Y是X的同分异构体,且属于芳香烃,则Y的结构简式可以为![]()
C. X能使高锰酸钾酸性溶液褪色
D. X与足量的H2在一定条件下反应可生成环状的饱和烃Z,Z的一氯代物有4种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属在化工生产及日常生活中有着广泛的应用,如铁、铬、镓等在现代工业中备受青睐。
(1)铬是一种硬而脆、抗腐蚀性强的金属,常招于电镀和制造特种钢。基态Cr原子中,未成对电子数有_______个,Cr3+的价电子排布式为________。
(2)Zn与Ga的第一电离能从大到小的顺序为_________。
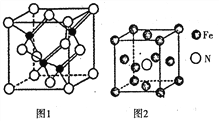
(3)镓与第VA族元素可形成多种新型人工半导体材料,砷化镓(GaAs)就是其中一种,其晶体结构如图1所示(白色球代表As原子)。在GaAs晶体中,距离每个Ga原子最近的As原子有_____个,距离每个As原子最近的As原子有_______个。
(4)铁的多种化合物均为磁性材料,氮化铁是其中一种,某氮化铁的晶胞结构如图2所示,则氮化铁的化学式为______;设晶胞边长为acm,阿伏加德罗常数为NA,该晶体的密度为 _____g.cm-3 (用含a和NA的式子表示)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com