
【题目】阿魏酸在食品、医药等方面有着广泛用途。已知一种合成阿魏酸的反应可表为:

对以上反应说法正确的是
A. 可用酸性KMnO4溶液检测上述反应是否有阿魏酸生成
B. 香兰素、阿魏酸均可与Na2CO3、NaOH 、NaHCO3溶液反应
C. 通常条件下,香兰素、阿魏酸都能发生取代、加成、消去反应
D. 与香兰素互为同分异构体分子中有4种不同化学环境的氢,能消2molNaOH溶液且能发生银镜反应的酚类化合物共有2种
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 油脂是食物组成中的重要部分,也是产生能量最高的营养物质
B. 蛋白质在人体内经过一系列的变化最终被转化为氨气的形式
C. 使用微生物降解塑料可以有效地治理“白色污染”
D. 氡是一种来自于天然石材的放射性气体,是人类健康的“隐形杀手”
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学查阅资料获悉:用KMnO4可以测定H2O2的物质的量浓度:取15.00mL H2O2溶液,用稀H2SO4酸化;逐滴加入0.003mol·L-1KMnO4溶液,产生气体,溶液褪色速率开始较慢后变快,至恰好完全反应时共消耗20.00 mL KMnO4溶液。该反应的离子方程式是:2MnO4-+5H2O2+6H+=2Mn2++5O2↑+8H2O;
(1)该反应体现了H2O2的__________(填“氧化性”、“还原性”或“氧化性和还原性”);
(2)KMnO4溶液褪色速率开始较慢,后变快的原因可能是某种物质对该反应起到了催化作用,则该物质最有可能是________;(填序号) a. MnO4- b.H+ c.Mn2+ d.K+
(3)判断完全反应的现象是_________________________________________________;
(4)该H2O2溶液的物质的量浓度是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组的同学利用如图所示的量热计完成中和反应反应热的测定实验。

实验用品:
浓硫酸、0.55 mol·L1的NaOH溶液、蒸馏水、自制量热计(如图)、烧杯、滴管、玻璃棒、量筒等。
实验步骤:
①配制0.25 mol·L1的硫酸溶液250 mL;
②分别量取0.25 mol·L1的硫酸、0.55 mol·L1的NaOH溶液各50 mL,并测量其起始温度;
③将二者于自制量热计中小心混合,测出反应过程中的温度,并作好记录;
④重复②、③步骤两次;
⑤处理数据得到如图所示曲线。

据此回答下列问题:
(1)量热计的插孔A中应插入的一种玻璃仪器是________。
(2)步骤①中除用到实验用品所列部分仪器外,还会用到的玻璃仪器是________。
(3)计算中和反应反应热ΔH时,所使用的温度数据Δt=________。
(4)若实验中用60 mL 0.25 mol·L1硫酸溶液和50 mL 0.55 mol·L1 NaOH溶液进行实验,与上述实验相比,所测得的中和反应反应热________(填“相等”或“不相等”);若用50 mL 0.50 mol·L1醋酸溶液代替硫酸溶液进行上述实验,测得反应前后溶液温度的变化值会________(填“偏大”“偏小”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E五种物质焰色反应均为黄色,它们按图所示关系相互转化.
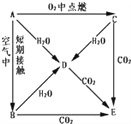
(1)这五种物质中,A: ___________、 C: ___________.
(2)将CO2通入E的饱和溶液中,该反应的离子方程式为______________________________.
(3)写出A→D、C→D、C→E反应的化学方程式
A→D:___________________________.
C→D:___________________________.
C→E:___________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在现行元素周期表中,所含元素种数最多的族和周期分别是( )
A. 第ⅠA族 第六周期
B. 第Ⅷ族 第六周期
C. 第ⅢB族 第六周期
D. 第ⅢA族 第六周期
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质分类正确的是( )
A. SiO2、NO2均为酸性氧化物 B. 稀豆浆、淀粉溶液均为胶体
C. 烧碱、乙醇均为电解质 D. 水玻璃、冰醋酸均为混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面有关晶体的叙述中,不正确的是( )
A. 金刚石网状结构中,由形成的碳原子环中,最小的环上有6个碳原子
B. 12g石墨中含有σ键的个数为2NA (NA表示阿伏伽德罗常数)
C. 氯化铯晶体中,每个CS+周围紧邻8个C1-
D. 干冰晶体中,每个CO2分子周围紧邻12个CO2分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)工业上常用氨气为原料制备硝酸,其中有一步非常重要的反应为:4NH3+5O2![]() 4NO+6H2O,该反应的氧化剂为______,还原剂为______。用单线桥法表示该氧化还原反应电子转移的方向和数目: _____________。若有标准状况下V L氨气完全反应,并转移n个电子,则阿伏加德罗常数(NA)可表示为______ (写出含字母的表达式)。
4NO+6H2O,该反应的氧化剂为______,还原剂为______。用单线桥法表示该氧化还原反应电子转移的方向和数目: _____________。若有标准状况下V L氨气完全反应,并转移n个电子,则阿伏加德罗常数(NA)可表示为______ (写出含字母的表达式)。
(2)写出下列反应的离子方程式。
①铝片与硝酸汞溶液反应_______________。
②向MgCl2溶液中滴加氨水(NH3·H2O)生成Mg(OH)2沉淀_______________。
(3)向MgCl2溶液中滴加氨水,过滤得到Mg(OH)2沉淀,用蒸馏水对沉淀进行洗涤,洗涤方法是向过滤器中注入蒸馏水,直至没过沉淀,然后等待液体从漏斗底部流出,重复操作2~3次(以除去吸附溶液中的其它离子)。检验该沉淀已经洗净的操作为_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com