
【题目】2015年雾霾天气多次肆虐我国中东部地区.其中,汽车尾气和燃煤尾气是造成空气污染的原因之一.
(1)汽车尾气净化的主要原理为:2NO(g)+2CO (g) ![]() 2CO2 (g)+N2 (g)在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如图1所示.
2CO2 (g)+N2 (g)在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如图1所示. 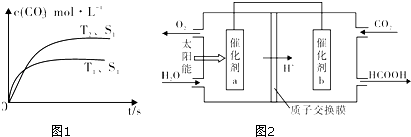
据此判断:
①该反应的平衡常数表达式为 .
②该反应的△H0(选填“>”、“<”).
③当固体催化剂的质量一定时,增大其表面积可提高化学反应速率.若催化剂的表面积S1>S2 , 在右图中画出c(CO2)在T2、S2条件下达到平衡过程中的变化曲线.
(2)直接排放煤燃烧产生的烟气会引起严重的环境问题.
①煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染.
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H=﹣867kJmol﹣1
2NO2(g)N2O4(g)△H=﹣56.9kJmol﹣1
写出CH4催化还原N2O4(g)生成N2(g)、CO2(g)和H2O(g)的热化学方程式 .
②将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的.图2是通过光电转化原理以廉价原料制备新产品的示意图.写出上述光电转化过程的化学反应方程式 . 催化剂a、b之间连接导线上电子流动方向是(填a→b或b→a).
【答案】
(1)K= ![]() ;<
;<
(2)CH4(g)+N2O4(g)=N2(g)+CO2(g)+2H2O(g)△H=﹣810.1kJ/mol;2CO2+2H2O ![]() 2HCOOH+O2;a→b
2HCOOH+O2;a→b
【解析】解:(1)①2NO(g)+2CO(g) ![]() 2CO2 (g)+N2 (g)的平衡常数表达式为生成物浓度系数次幂的乘积与反应物浓度系数次幂乘积的比值,即:K=
2CO2 (g)+N2 (g)的平衡常数表达式为生成物浓度系数次幂的乘积与反应物浓度系数次幂乘积的比值,即:K= ![]() ,所以答案是:K=
,所以答案是:K= ![]() ;
;
②由图示可知,温度T1先到达平衡,故温度T1>T2 , 温度越高平衡时,二氧化碳的浓度越低,说明升高温度平衡向逆反应移动,故正反应为放热反应,即:△H<0,
所以答案是:<;
③接触面积越大反应速率越快,到达平衡的时间越短,催化剂的表面积S1>S2 , S2条件下达到平衡所用时间更长,但催化剂不影响平衡移动,平衡时二氧化碳的浓度与温度T1到达平衡时相同,故c(CO2)在T1、S2条件下达到平衡过程中的变化曲线为 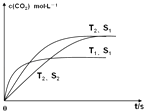 ,所以答案是:
,所以答案是:  ;
;
(2.)①已知:ⅠCH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O(g)△H1=﹣867kJ/mol
Ⅱ2NO2(g)N2O4(g)△H2=﹣56.9kJ/mol
根据盖斯定律,Ⅰ﹣Ⅱ得:CH4(g)+N2O4(g)=N2(g)+CO2(g)+2H2O(g),故△H=﹣867kJ/mol﹣(﹣56.9kJ/mol)=﹣810.1kJ/mol,
即:CH4(g)+N2O4(g)=N2(g)+CO2(g)+2H2O(g)△H=﹣810.1kJ/mol,
所以答案是:CH4(g)+N2O4(g)=N2(g)+CO2(g)+2H2O(g)△H=﹣810.1kJ/mol.
②体系中进入的物质为:CO2和H2O,则反应物为:CO2和H2O,得到的物质为:HCOOH和O2 , 生成物为:HCOOH和O2 , 利用氧化还原方程式的配平写出化学方程式为:2CO2+2H2O ![]() 2HCOOH+O2;体系中氢离子从 a→b,则电流的方向为:b→a,电子的流向为:a→b,所以答案是:2CO2+2H2O
2HCOOH+O2;体系中氢离子从 a→b,则电流的方向为:b→a,电子的流向为:a→b,所以答案是:2CO2+2H2O ![]() 2HCOOH+O2;a→b.
2HCOOH+O2;a→b.
【考点精析】通过灵活运用化学平衡状态本质及特征,掌握化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效)即可以解答此题.


 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】用铅蓄电池电解苦卤水 (含C1﹣、Br﹣、Na+、Mg2+)的装置如图所示 (a、b为石墨电极).下列说法中正确的是( ) 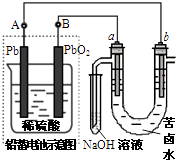
A.铅蓄电池负极的反应式为:Pb﹣2e ﹣→Pb2+
B.铅蓄电池放电时,该电池两极质量均减少
C.铅蓄电池充电时,B极应与外电源负极相连
D.电解苦卤水时,a电极首先放电的是Br﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生用中和滴定法测定某NaOH溶液的物质的量浓度,选酚酞作指示剂.
用盐酸滴定待测液NaOH,滴定终点时的颜色变化是;若滴定前平视读数,滴定终点时俯视读数,则会使所测NaOH溶液的浓度值(填“无影响”、“偏高”或“偏低”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“物质的量”是联系宏观世界和微观世界的桥梁。下列说法正确的是
A. 任何气体的“气体摩尔体积”均为22.4L/mol
B. 1molO2的质量是32g/mol
C. “摩尔”是 “物质的量”的单位
D. 10mL2mol/LH2SO4溶液中取出的5mL溶液,其浓度为1mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】判断下列反应的熵值的变化,在每小题后面的横线上填上“增加”“减小”或“无明显变化”。
(1)2H2(g)+O2(g)![]() 2H2O(l) 。
2H2O(l) 。
(2)H2(g)+Cl2(g)![]() 2HCl(g) 。
2HCl(g) 。
(3)(NH4)2CO3(s)![]() NH4HCO3(s)+NH3(g) 。
NH4HCO3(s)+NH3(g) 。
(4)Cu(s)+Cl2(g)![]() CuCl2(s) 。
CuCl2(s) 。
(5)将少量KNO3晶体溶解在水中 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于如图所示转化关系(X代表卤素),说法不正确的是( ) 
A.2H(g)+2X(g)=2HX(g)△H3<0
B.途径Ⅰ生成HX的反应热与途径无关,所以△H1=△H2+△H3
C.途径Ⅰ生成HBr放出的热量比生成HCl的少,说明HBr比HCl稳定
D.Cl、Br、I的非金属性依次减弱,所以途径Ⅱ吸收的热量依次减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在t℃时,AgBr在水中的沉淀溶解平衡曲线如图所示.又知t℃时AgCl的Ksp=4×10﹣10 , 下列说法不正确的是( ) 
A.在t℃时,AgBr的Ksp为4.9×10﹣13
B.在AgBr饱和溶液中加入NaBr固体,可使溶液由c点到b点
C.图中a点对应的是AgBr的不饱和溶液
D.向组成为c点的溶液中加入等体积的0.1 mol/L的氯化钠溶液,可产生AgCl沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,A是由导热材料制成的密闭容器,B是一耐化学腐蚀且易于传热的透明气囊.关闭K2 , 将各1mol NO2通过K1、K3分别充入A、B中,反应起始时A、B的体积相同均为a L. 
①B中可通过判断可逆反应2NO2N2O4已经达到平衡.
②若平衡后在A容器中再充入0.5mol N2O4 , 则重新到达平衡后,平衡混合气中NO2的体积分数(填“变大”“变小”或“不变”).
③若容器A中到达平衡所需时间t s,达到平衡后容器内压强为起始压强的0.8倍,则平均化学反应速率v(NO2)等于
④若打开K2 , 平衡后B容器的体积缩至0.4a L,则打开K2之前,气球B体积为L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列萃取与分液结合进行的操作(用CCl4为萃取剂从碘水中萃取碘)中错误的是
A.饱和碘水和CCl4加入分液漏斗中后,塞上上口部的塞子,用左手压住分液漏斗上口部,右手握住活塞部分,把分液漏斗倒转过来振荡
B.静置,分液漏斗中溶液分层,下层呈紫红色,上层几乎无色
C.打开分液漏斗的活塞,使全部下层液体沿承接液体的烧杯内壁慢慢流出
D.最后继续打开活塞用另一个烧杯承接上层液体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com