
化学中常用图像直观地描述化学反应的进程或结果。下列图像描述正确的是( )
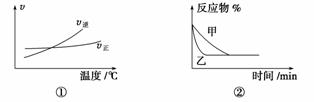

A.根据图①可判断可逆反应A2(g)+3B2(g) 2AB3(g)的ΔH>0
2AB3(g)的ΔH>0
B.图②表示压强对可逆反应2A(g)+2B(g) 3C(g)+D(s)的影响,甲的压强大
3C(g)+D(s)的影响,甲的压强大
C.图③可表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化
D.根据图④,若除去CuSO4溶液中的Fe3+可采用向溶液中加入适量CuO至pH在4左右
科目:高中化学 来源: 题型:
下图表示由短周期元素组成的一些物质之间的转化关系(某些反应产物已略去)。各方框表示有关的一种反应物或生成物(某些物质已经略去),其中A、B、D在常温下均为无色无刺激性气味的气体,C是使湿润的红色石蕊试纸变蓝的气体,M是最常见 的无色液体。
的无色液体。

⑴ 物质F的化学式_ ⑵ 物质B的电子式__________
⑶ 写出C→E的化学方程式______________________________
⑷ 写出G→E的离子方程式______________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
用如图所示装置进行下列实验,能达到实验目的的是 ( )。
A.瓶中盛有适量浓H2SO4,从A口进气来干燥NH3
B.从B口进气,用排空气法收集CO2
C.瓶中盛满水,从B口进气,用排水法收集NO2
D.瓶中装满水,A口连接导管并伸入量筒中,从B口进气,用排水法测量 生成H2的体积

查看答案和解析>>
科目:高中化学 来源: 题型:
氢氧燃料电池已用于航天飞机。以30%KOH溶液为电解质溶液的这种电池在使用时的电极反应如下:2H2 + 4OH- - 4e- = 4H2O;O2 + 2H2O + 4e- = 4OH-。据此作出判断,下列说法中错误的是:
A.H2在负极发生氧化反应
B.供电时的总反应为:2H2+O2=2H2O
C.产物为无污染的水,属于环境友好电池
D.燃料电池的能量转化率可达100%
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、C、D四种短周期元素,原子序数依次增大,A原子的最外层上有4个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,能生成一种淡黄色的固体E;D的L层电子数等于K、M两个电子层上的电子数之和。
(1)A为 ,B为 ,C为 ,D为 。(填元素符号)
(2)D的最高价氧化物的水化物的化学式是 ,E的电子式是 。
(3)写出由A、B组成的化合物与E反应的化学方程式: 。
(4)请用电子式表示出C和D形成的化合物F的形成过程: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌。以下是过氧化氢法生产亚氯酸钠的工艺流程图:

已知:①NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2•3H2O。
②纯ClO2易分解爆炸,一般用稀有气体或空气稀释到10%以下安全。
③160 g/L NaOH溶液是指160 gNaOH固体溶于水所得溶液的体积为1L。
⑴ 160 g/L NaOH溶液的物质的量浓度为 。
⑵ 发生器中鼓入空气的作用可能是 (选填序号)。
a.将SO2氧化成SO3,增强酸性; b.稀释ClO2以防止爆炸;
c.将NaClO3氧化成ClO2
⑶ 吸收塔内的反应的化学方程式为 。
吸收塔的温度不能超过20℃,其目的是 。
⑷ 在碱性溶液中NaClO2比较稳定,所以吸收塔中应维持NaOH稍过量,判断NaOH是否过量的简单实验方法是 。
⑸ 吸收塔中为防止NaClO2被还原成NaCl,所用还原剂的还原性应适中。除H2O2外,还可以选择的还原剂是 (选填序号)。
a.Na2O2 b.Na2S c.FeCl2
⑹ 从滤液中得到NaClO2•3H2O粗晶体的实验操作依次是 (选填序号)。
a.蒸馏 b.蒸发 c.灼烧 d.过滤 e.冷却结晶
要得到更纯的NaClO2•3H2O晶体必须进行的操作是 (填操作名称)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述不正确的是
A.水受热不易分解,与水分子之间存在氢键无关
B.有化学键断裂的变化不一定是化学变化
C.熔化状态下能导电的物质不一定是离子化合物
D.易溶于水的物质一定是电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,某恒定容积的密闭容器中发生如下可逆反应:CO(g)+H2(g)  C(s)+H2O(g);ΔH>0,以1 mol CO和2 mol H2为起始反应物,t1时达到平衡,生成0.5mol H2O(g)。t2时改变反应条件,化学反应速率(v)与时间(t)的关系如图所示。下列叙述正确的是
C(s)+H2O(g);ΔH>0,以1 mol CO和2 mol H2为起始反应物,t1时达到平衡,生成0.5mol H2O(g)。t2时改变反应条件,化学反应速率(v)与时间(t)的关系如图所示。下列叙述正确的是
A.t2时改变的条件可能是升高了温度或增大了压强
B.平衡后若加入少量炭,平衡向逆反应方向移动
C.平衡后若加入氢气,上述反应的ΔH会增大
D.起始时刻和达平衡后容器的压强之比为5∶6

查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、M、N是短周期主族元素,且原子序数依次增大。已知X的最外层电子数是电子层数的3倍,X、M同主族,Y的原子在短周期主族元素中原子半径最大。下列说法正确的是
A.M与X形成的化合物对应的水化物一定是强酸
B.Y2X和Y2X2中化学键类型完全相同
C.X、Y的简单离子半径:r(X2-)>r(Y+)
D.M的气态氢化物比N的气态氢化物稳定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com