
°æƒø°ø«‚∆¯ «“ª÷÷«ÂΩý∏þ–ßµƒ–¬–ՃБ¥£¨»Á∫Œæ≠º√ µ”√µƒ÷∆»°«‚∆¯≥…Œ™÷ÿ“™øŒÃ‚°£
(1)¡Úµ‚—≠ª∑∑÷Ω‚ÀÆ «“ª÷÷∏þ–ß°¢ª∑±£µƒ÷∆«‚∑Ω∑®£¨∆‰¡˜≥ÃÕº»Áœ¬£∫
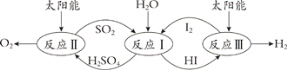
“—÷™£∫
∑¥”¶I£∫SO2(g) + I2(g) + 2H2O(l) = 2HI(aq) + H2SO4(aq) ¶§H1=©Å213 kJ°§mol-1
∑¥”¶II£∫H2SO4(aq) = SO2(g) + H2O(l) +1/2O2(g) ¶§H2= +327 kJ°§mol-1
∑¥”¶III£∫2HI(aq) = H2(g) + I2(g) ¶§H3= +172 kJ°§mol-1
‘Ú∑¥”¶2H2O(l) = 2H2(g)+O2(g) ¶§H= ________°£
(2)H2Sø…”√”⁄∏þ–ß÷∆»°«‚∆¯£¨∑¢…˙µƒ∑¥”¶Œ™2H2S(g)S2(g)£´2H2(g)°£
¢Ò.»Ù∆ º ±»ð∆˜÷–÷ª”–H2S£¨∆Ω∫‚ ±»˝÷÷ŒÔ÷ µƒŒÔ÷ µƒ¡ø”Ρ—Ω‚Œ¬∂»µƒπÿœµ»ÁÕº£∫
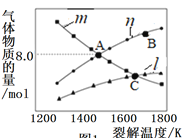
¢ŸÕº÷–«˙œþ1±Ì 浃ŒÔ÷ «________________(Ãѧ Ω)°£
¢⁄Aµ„ ±H2Sµƒ◊™ªØ¬ Œ™__________________°£
¢€Cµ„ ±£¨…Ë»ð∆˜ƒ⁄µƒ◊ЗπŒ™pPa£¨‘Ú∆Ω∫‚≥£ ˝Kp=________(”√∆Ω∫‚∑÷—π¥˙ÃÊ∆Ω∫‚≈®∂»º∆À„£¨∑÷—π£Ω◊Ð—π°¡ŒÔ÷ µƒ¡ø∑÷ ˝)°£
II.»Ù‘⁄¡Ω∏ˆµ»Ãª˝µƒ∫„»ð»ð∆˜÷–∑÷±º”»Î2.0mol H2S°¢1.0mol H2S£¨≤‚µ√≤ªÕ¨Œ¬∂»œ¬H2Sµƒ∆Ω∫‚◊™ªØ¬ »ÁÕºÀ˘ æ£∫
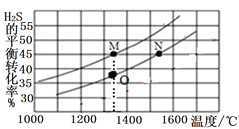
¢ŸMµ„∫ÕOµ„µƒƒÊ∑¥”¶ÀŸ¬ v(M)______v(O) (ÃÓ°∞>°±°∞<°±ªÚ°∞=°±£¨œ¬Õ¨)£ª
¢⁄M°¢N¡Ωµ„»ð∆˜ƒ⁄µƒ—π«ø2P(M)_____P(N)£¨∆Ω∫‚≥£ ˝K(M)_____K(N)°£
°æ¥∞∏°ø£´572kJ°§mol£≠1 S2 50% p Pa < < <
°æΩ‚Œˆ°ø
(1)¿˚”√∏«Àπ∂®¬…Ω¯––∑¥”¶2H2O(l) = 2H2(g)+O2(g) ¶§Hµƒº∆À„£ª
(2)¢Ò.”…∑¥”¶∑Ω≥à Ω2H2S(g)![]() S2(g)+2H2(g)ø…÷™£¨»Ù∆ º ±»ð∆˜÷–÷ª”–H2S£¨∆Ω∫‚ ±S2µƒŒÔ÷ µƒ¡øŒ™H2µƒ
S2(g)+2H2(g)ø…÷™£¨»Ù∆ º ±»ð∆˜÷–÷ª”–H2S£¨∆Ω∫‚ ±S2µƒŒÔ÷ µƒ¡øŒ™H2µƒ![]() £¨‘Ú«˙œþl±Ì 浃ŒÔ÷ «S2£¨«˙œþm±Ì 浃ŒÔ÷ «H2S£¨«˙œþn±Ì 浃ŒÔ÷ «H2£¨æð¥À∑÷ŒˆΩ‚¥£ª
£¨‘Ú«˙œþl±Ì 浃ŒÔ÷ «S2£¨«˙œþm±Ì 浃ŒÔ÷ «H2S£¨«˙œþn±Ì 浃ŒÔ÷ «H2£¨æð¥À∑÷ŒˆΩ‚¥£ª
¢Ú.∑¥”¶2H2S(g)![]() S2(g)+2H2(g)÷–£¨H2SµƒŒÔ÷ µƒ¡ø‘ˆº”£¨∆‰∆Ω∫‚◊™ªØ¬ ∑¥∂¯ºı–°£¨º¥Mµ„∫ÕOµ„∑÷±À˘‘⁄µƒ«˙œþ¥˙±ÌH2Sµƒ∆ º¡øŒ™0.1mol∫Õ0.2mol£¨æð¥ÀΩ‚¥£ª
S2(g)+2H2(g)÷–£¨H2SµƒŒÔ÷ µƒ¡ø‘ˆº”£¨∆‰∆Ω∫‚◊™ªØ¬ ∑¥∂¯ºı–°£¨º¥Mµ„∫ÕOµ„∑÷±À˘‘⁄µƒ«˙œþ¥˙±ÌH2Sµƒ∆ º¡øŒ™0.1mol∫Õ0.2mol£¨æð¥ÀΩ‚¥£ª
(1)∏˘æð∏«Àπ∂®¬…£¨∑¥”¶(¢Ò+¢Ú+¢Û)°¡2ø…µ√µΩ∑¥”¶2H2O(l) = 2H2(g)+O2(g)£¨∆‰¶§H=2(¶§H1+¶§H2+¶§H3)=2°¡(172+327-213)=+572kJ°§mol-1£¨π ¥∞∏Œ™£∫+572kJ°§mol-1£ª
(2)¢Ò.¢Ÿ”…∑¥”¶∑Ω≥à Ω2H2S(g)![]() S2(g)+2H2(g)ø…÷™£¨»Ù∆ º ±»ð∆˜÷–÷ª”–H2S£¨∆Ω∫‚ ±S2µƒŒÔ÷ µƒ¡øŒ™H2µƒ
S2(g)+2H2(g)ø…÷™£¨»Ù∆ º ±»ð∆˜÷–÷ª”–H2S£¨∆Ω∫‚ ±S2µƒŒÔ÷ µƒ¡øŒ™H2µƒ![]() £¨‘Ú«˙œþl±Ì 浃ŒÔ÷ «S2£¨π ¥∞∏Œ™£∫S2£ª
£¨‘Ú«˙œþl±Ì 浃ŒÔ÷ «S2£¨π ¥∞∏Œ™£∫S2£ª
¢⁄∏˘æðÕºœÒ£¨Aµ„ ±£¨¡ÚªØ«‚∫Õ«‚∆¯µƒŒÔ÷ µƒ¡øœýµ»£¨∏˘æð2H2S(g)![]() S2(g)+2H2(g)£¨Àµ√˜∑¥”¶µƒ¡ÚªØ«‚”Î £”ýµƒ¡ÚªØ«‚œýµ»£¨H2Sµƒ◊™ªØ¬ Œ™50%£¨π ¥∞∏Œ™£∫50%£ª
S2(g)+2H2(g)£¨Àµ√˜∑¥”¶µƒ¡ÚªØ«‚”Î £”ýµƒ¡ÚªØ«‚œýµ»£¨H2Sµƒ◊™ªØ¬ Œ™50%£¨π ¥∞∏Œ™£∫50%£ª
¢€∏˘æðAµ„ø…÷™£¨∆ º ±¡ÚªØ«‚Œ™20mol£¨Bµ„ ±£¨¡ÚªØ«‚”ÎS2µƒŒÔ÷ µƒ¡øœýµ»£¨…Ë∑÷Ω‚µƒ¡ÚªØ«‚Œ™x£¨‘Ú20-x=![]() £¨Ω‚µ√x=
£¨Ω‚µ√x=![]() mol£¨»ð∆˜÷–∫¨”–H2S
mol£¨»ð∆˜÷–∫¨”–H2S![]() mol£¨S2
mol£¨S2![]() mol£¨H2
mol£¨H2![]() mol£¨ŒÔ÷ µƒ¡ø∑÷ ˝∑÷±Œ™
mol£¨ŒÔ÷ µƒ¡ø∑÷ ˝∑÷±Œ™![]() £¨
£¨![]() £¨
£¨![]() £¨∆Ω∫‚≥£ ˝Kp=
£¨∆Ω∫‚≥£ ˝Kp=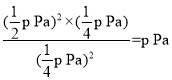 £¨π ¥∞∏Œ™£∫p Pa£ª
£¨π ¥∞∏Œ™£∫p Pa£ª
¢Ú.¢Ÿ∑¥”¶2H2S(g)![]() S2(g)+2H2(g)÷–£¨H2SµƒŒÔ÷ µƒ¡ø‘ˆº”£¨∆‰∆Ω∫‚◊™ªØ¬ ∑¥∂¯ºı–°£¨º¥Mµ„∫ÕOµ„∑÷±À˘‘⁄µƒ«˙œþ¥˙±ÌH2Sµƒ∆ º¡øŒ™0.1mol∫Õ0.2mol£¨∫„»ð»ð∆˜÷–£¨Mµ„µƒ≈®∂»–°”⁄Oµ„£¨‘ÚƒÊ∑¥”¶ÀŸ¬ v(M)< v(O)£¨π ¥∞∏Œ™£∫<£ª
S2(g)+2H2(g)÷–£¨H2SµƒŒÔ÷ µƒ¡ø‘ˆº”£¨∆‰∆Ω∫‚◊™ªØ¬ ∑¥∂¯ºı–°£¨º¥Mµ„∫ÕOµ„∑÷±À˘‘⁄µƒ«˙œþ¥˙±ÌH2Sµƒ∆ º¡øŒ™0.1mol∫Õ0.2mol£¨∫„»ð»ð∆˜÷–£¨Mµ„µƒ≈®∂»–°”⁄Oµ„£¨‘ÚƒÊ∑¥”¶ÀŸ¬ v(M)< v(O)£¨π ¥∞∏Œ™£∫<£ª
¢⁄”…ÕºœÒø…÷™£¨H2Sµƒ◊™ªØ¬ æ˘Œ™45%£¨ø…¡–»˝∂Œ Ω”–£∫

n(◊Ð)N=1.1+0.45+0.9=2.45mol
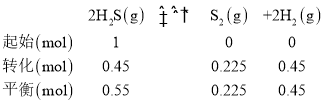
n(◊Ð)M=0.55+0.45+0.225=1.225mol
2n(◊Ð)M=n(◊Ð)M£¨”÷ÕºœÒø…÷™TM<TN£¨”…PV=nRTø…µ√£¨2P(M)<P(N)£¨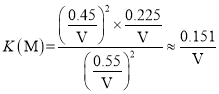 £¨
£¨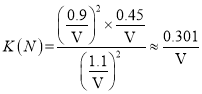 £¨‘ÚK(M)<K(N)£¨π ¥∞∏Œ™£∫<£ª<°£
£¨‘ÚK(M)<K(N)£¨π ¥∞∏Œ™£∫<£ª<°£


 –°ÃÏ≤≈øŒ ±◊˜“µœµ¡–¥∞∏
–°ÃÏ≤≈øŒ ±◊˜“µœµ¡–¥∞∏ “ªøŒÀƒ¡∑œµ¡–¥∞∏
“ªøŒÀƒ¡∑œµ¡–¥∞∏ ª∆∏‘–°◊¥‘™¬˙∑÷≥¥Ì¢≤‚—Èœµ¡–¥∞∏
ª∆∏‘–°◊¥‘™¬˙∑÷≥¥Ì¢≤‚—Èœµ¡–¥∞∏ –¬∏®Ωõº—ßœµ¡–¥∞∏
–¬∏®Ωõº—ßœµ¡–¥∞∏ —Ùπ‚Õ¨—ß“ªœþ√˚ ¶»´”≈∫√æÌœµ¡–¥∞∏
—Ùπ‚Õ¨—ß“ªœþ√˚ ¶»´”≈∫√æÌœµ¡–¥∞∏
| ƒÍº∂ | ∏þ÷–øŒ≥à | ƒÍº∂ | ≥ı÷–øŒ≥à |
| ∏þ“ª | ∏þ“ª√‚∑—øŒ≥ÃÕ∆ºˆ£° | ≥ı“ª | ≥ı“ª√‚∑—øŒ≥ÃÕ∆ºˆ£° |
| ∏þ∂˛ | ∏þ∂˛√‚∑—øŒ≥ÃÕ∆ºˆ£° | ≥ı∂˛ | ≥ı∂˛√‚∑—øŒ≥ÃÕ∆ºˆ£° |
| ∏þ»˝ | ∏þ»˝√‚∑—øŒ≥ÃÕ∆ºˆ£° | ≥ı»˝ | ≥ı»˝√‚∑—øŒ≥ÃÕ∆ºˆ£° |
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø“ª∂®¡øµƒFe°¢FeO°¢Fe2O3°¢Fe3O4µƒªÏ∫œŒÔ÷–º”»Î350mL 2molL©Å1µƒœ°œıÀ·«°∫√ πªÏ∫œŒÔÕÍ»´»ÐΩ‚£¨∑≈≥ˆ2.24L NO£®±Í◊º◊¥øˆ£©£¨Õ˘À˘µ√»Ð“∫÷–º”»ÎKSCN»Ð“∫£¨ŒÞ∫Ï…´≥ˆœ÷£Æ»Ù”√◊„¡øµƒH2‘⁄º”»»Ãıº˛œ¬ªπ‘≠œýÕ¨÷ ¡øµƒªÏ∫œŒÔ£¨À˘µ√µΩµƒÃ˙µƒŒÔ÷ µƒ¡øŒ™£® £©
A. 0.21 molB. 0.25 molC. 0.3 molD. 0.35 mol
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°øƒ≥ µ—È–°◊ÈŒ™¡ÀÃΩæøSO2µƒ–‘÷ £¨…˺∆¡À»Áœ¬◊∞÷√£¨

µ—È≤Ω÷Ë£∫
¢Ÿœ»¡¨Ω”∫√◊∞÷√£¨ºÏ≤È∆¯√Ж‘£¨‘Ÿº”»Î ‘º¡£ª
¢⁄º”»»A ‘πУª
¢€Ω´Õ≠ÀøœÚ…œ≥È∂Ø¿Îø™“∫√Ê°£
£®1£©A ‘πÐ÷–∑¢…˙∑¥”¶µƒªØ—ß∑Ω≥Ã Ω «______°£
£®2£©B ‘πÐ÷–µƒœ÷œÛ «______°£
£®3£© ‘πÐCŒÞ√˜œ‘œ÷œÛ£¨ƒ≥–°◊È»°“ª≤ø∑÷∑¥”¶∫Ûµƒ»Ð“∫£¨∑÷±µŒº”“‘œ¬ ‘º¡£¨«Îƒ„‘§≤‚ƒÐ∑Ò…˙≥…≥¡µÌ£¨»Ù…˙≥…≥¡µÌ£¨–¥≥ˆ…˙≥…≥¡µÌµƒªØ—ß Ω°£
º”»Î ‘º¡ | ƒÐ∑Ò…˙≥…≥¡µÌ | ≥¡µÌµƒªØ—ß Ω |
¬»ÀÆ | _____________ | __________ |
∞±ÀÆ | __________ | ___________ |
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø¿˚”√»ÁÕºÀ˘ æ◊∞÷√≤‚∂®÷–∫Õ»»µƒ µ—È≤Ω÷Ë»Áœ¬£∫
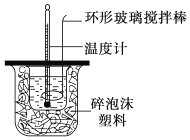
¢Ÿ”√¡øÕ≤¡ø»°50mL0.50mol/L—ŒÀ·µπ»Î–°…’±≠÷–£¨≤‚≥ˆ—ŒÀ·Œ¬∂»£ª
¢⁄”√¡Ì“ª¡øÕ≤¡ø»°50mL0.55mol/LNaOH»Ð“∫£¨≤¢”√¡Ì“ªŒ¬∂»º∆≤‚≥ˆ∆‰Œ¬∂»£ª
¢€Ω´NaOH»Ð“∫µπ»Î–°…’±≠÷–£¨…Ë∑® π÷ƪÏ∫œæ˘‘»£¨≤‚µ√ªÏ∫œ“∫◊Ó∏þŒ¬∂»°£
ªÿ¥œ¬¡–Œ £∫
(1)Œ™ ≤√¥À˘”√NaOH»Ð“∫“™…‘π˝¡ø____________________°£
(2)µπ»ÎNaOH»Ð“∫µƒ’˝»∑≤Ÿ◊˜ «________£®ÃÓ–Ú∫≈£©°£
A.—ÿ≤£¡ß∞Ùª∫¬˝µπ»Î B.∑÷»˝¥Œ…Ÿ¡øµπ»Î C.“ª¥Œ—∏ÀŸµπ»Î
(3) π—ŒÀ·”ÎNaOH»Ð“∫ªÏ∫œæ˘‘»µƒ’˝»∑≤Ÿ◊˜ «________£®ÃÓ–Ú∫≈£©°£
A.”√Œ¬∂»º∆–°–ƒΩ¡∞Ë B.Ω“ø™”≤÷Ω∆¨”√≤£¡ß∞ÙΩ¡∞Ë
C.«·«·µÿ’Òµ¥…’±≠ D.”√Ã◊‘⁄Œ¬∂»º∆…œµƒª∑–Œ≤£¡ßΩ¡∞Ë∞Ù«·«·µÿΩ¡∂Ø
(4)œ÷Ω´“ª∂®¡øµƒœ°«‚—ıªØƒ∆»Ð“∫°¢œ°«‚—ıªØ∏∆»Ð“∫°¢œ°∞±ÀÆ∑÷±∫Õ1L1mol°§L-1µƒœ°—ŒÀ·«°∫√ÕÍ»´∑¥”¶£¨∆‰∑¥”¶»»∑÷±Œ™°˜H1°¢°˜H2°¢°˜H3£¨‘Ú°˜H1°¢°˜H2°¢°˜H3µƒ¥Û–°πÿœµŒ™___________°£
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø298K ±£¨œÚ20 mL 0.1000 mol°§L-1 CH3COOH»Ð“∫÷–µŒ»Î0.1000 mol°§L-1NaOH»Ð“∫£¨µŒ∂®«˙œþ»ÁÕºÀ˘ æ(∫ˆ¬‘Œ¬∂»±‰ªØ)°£œ¬¡–Àµ∑®’˝»∑µƒ «
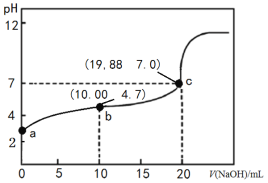
A.∏√µŒ∂®π˝≥Ô¶∏√—°‘Ò Ø»Ô»Ð“∫◊ˆ÷∏ 溡
B.”…cµ„ ˝÷µø…«Û¥◊À·µƒµÁ¿Î∆Ω∫‚≥£ ˝Œ™1.66°¡10-5 mol°§L-1
C.bµ„»Ð“∫÷–∏˜Œ¢¡£≈®∂»πÿœµŒ™2c(H£´)+c(CH3COOH) =c(CH3COO£≠)+2c(OH£≠)
D.÷–∫Õըê˝Õ¨pHµƒ¥◊À·∫Õ—ŒÀ·À˘”√«‚—ıªØƒ∆µƒŒÔ÷ µƒ¡ø£¨∫Û’þ∂ý
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°øœ¬¡–∏˜◊ÈŒÔ÷ ÷ƺ‰≤ªø…ƒÐ µœ÷»ÁÕºÀ˘ æ◊™ªØµƒ «£® £©
![]()
—°œÓ | X | Y | Z | M |
A | S | SO2 | SO3 | O2 |
B | HNO3 | Fe(NO3)3 | Fe(NO3)2 | Fe |
C | NaOH | Na2CO3 | Na2CO3 | CO2 |
D | HN3 | NO | NO2 | O2 |
A. A B. B C. C D. D
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°øº◊∞∑(CH3NH2) «“ª÷÷“ª‘™»ıºÓ£¨∆‰µÁ¿Î∑Ω≥Ã ΩŒ™£∫CH3NH2 + H2O ![]() CH3NH3+ + OH£≠°£≥£Œ¬œ¬£¨œÚ20.0 mL 0.10 mol/Lµƒº◊∞∑»Ð“∫÷–µŒº”VmL0.10mol/Lµƒœ°—ŒÀ·£¨ªÏ∫œ»Ð“∫µƒpH”ÎœýπÿŒ¢¡£≈®∂»µƒπÿœµ»ÁÕºÀ˘ æ°£œ¬¡–Àµ∑®÷–¥ÌŒÛµƒ «
CH3NH3+ + OH£≠°£≥£Œ¬œ¬£¨œÚ20.0 mL 0.10 mol/Lµƒº◊∞∑»Ð“∫÷–µŒº”VmL0.10mol/Lµƒœ°—ŒÀ·£¨ªÏ∫œ»Ð“∫µƒpH”ÎœýπÿŒ¢¡£≈®∂»µƒπÿœµ»ÁÕºÀ˘ æ°£œ¬¡–Àµ∑®÷–¥ÌŒÛµƒ «

A. bµ„∂‘”¶º”»Î—ŒÀ·µƒÃª˝V<20.00mL
B. ≥£Œ¬œ¬£¨∏˘æðaµ„ø…÷™º◊∞∑µƒµÁ¿Î∆Ω∫‚≥£ ˝Kb=10 -3£Æ4
C. bµ„ø…ƒÐ¥Ê‘⁄πÿœµ£∫c(Cl£≠) > c(CH3NH3+) > c(H+) = c(OH£≠)
D. V=20.00mL ±£¨»Ð“∫≥ »ıÀ·–‘
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø¿˚”√πÃ×ıªØŒÔµÁΩ‚≥ÿ£®SOEC)ø… µœ÷““ÕȵÁªØ—ßÕ—«‚÷∆““œ©£¨‘≠¿Ì æ“‚Õº»Áœ¬À˘ æ°£œ¬¡–Àµ∑®¥ÌŒÛµƒ «
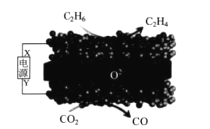
A.X «µÁ‘¥µƒ’˝º´
B.∏√◊∞÷√‘⁄π§◊˜π˝≥Ã÷–£¨O2-‘⁄πÃ×ıªØŒÔ÷–”…œ¬∑ΩœÚ…œ∑Ω«®“∆
C.“ıº´«¯∑¢…˙µƒ∑¥”¶Œ™£∫CO2+2e-+2H+=CO+H2O
D.∏√π˝≥õƒ◊Ð∑¥”¶∑Ω≥Ã ΩŒ™£∫C2H6+CO2=C2H4+CO+H2O
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
ø∆ƒø£∫∏þ÷–ªØ—ß ¿¥‘¥£∫ –գ∫
°æƒø°ø“ª∂®Œ¬∂»œ¬£¨ÃΩæøÕ≠”Îœ°HNO3µƒ∑¥”¶£¨∑¥”¶π˝≥ûÁœ¬£∫
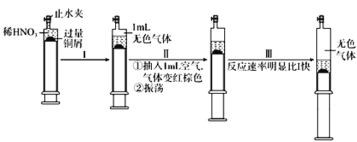
œ¬¡–Àµ∑®¥ÌŒÛµƒ «
A.π˝≥ÃI÷–…˙≥…ŒÞ…´∆¯Ãµƒ¿Î◊”∑Ω≥Ã Ω «3Cu+2NO3-+8H+ =3Cu2++2NO°¸+4H2O
B.≤Ω÷ËIII∑¥”¶ÀŸ¬ ±»I øϵƒ‘≠“Ú“ª∂® «NO2»Ð”⁄ÀÆ£¨ πc(HNO3)‘ˆ¥Û
C.π˝≥âÚ÷–∆¯Ã±‰≥…∫Ï◊ÿ…´µƒ∑¥”¶Œ™2NO+O2=2NO2
D.µ±ªÓ»˚≤ª‘Ÿ“∆∂Ø ±£¨‘Ÿ≥È»Îø’∆¯£¨Õ≠ø…“‘ºÃ–¯»ÐΩ‚
≤Èø¥¥∞∏∫ÕΩ‚Œˆ>>
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com