
【题目】医院处方药“复方电解质注射液”可作为水、电解质的补充源,注射液中含有NaCl、MgCl2和KCl三种无机盐,其中![]() 。
。
(1)若实验室药配制该电解质注射液500mL,所需的玻璃仪器有:玻璃板、烧杯和_______,需用托盘天平称量氯化钠固体___________g;
(2)已知该注射液中![]() ,
,![]() ,则
,则![]() ________
________![]() 。
。
【答案】胶头滴管、量筒、500 mL容量瓶 2.6 0.008
【解析】
(1)根据配制一定体积一定浓度溶液时操作步骤选择所需的仪器;依据m=cVM计算需要溶质的物质的量;
(2)依据溶液中存在电荷守恒规律解答。
(1)配制一定物质的量浓度溶液一般步骤:计算、称量、溶解、冷却、移液、定容、摇匀、装瓶等,用到的仪器:托盘天平、药匙、量筒、烧杯、玻璃棒、容量瓶、胶头滴管,配制该电解质注射液500mL,应选择500mL容量瓶,所以还缺少的玻璃仪器:500 mL容量瓶;需要称量氯化钠固体质量:0.089mol/L×0.5L×58.5g/mol=2.6g;
(2)溶液中存在电荷守恒规律:c(Cl-)×1=c(Na+)×1+c(K+)×1+c(Mg2+)×2,0.11molL-1=0.089molL-1+0.0050molL-1+2×c(Mg2+),解得c(Mg2+)=0.008mol/L。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. O2、O3 是氧元素的同素异形体,性质都相似
B. 35Cl与37Cl-互为同位素
C. 乙二醇( ![]() ) 和甘油(
) 和甘油( ![]() )互为同系物
)互为同系物
D. CH3CHO 与![]() 互为同分异构体
互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是
A.碳酸钠溶液中滴加少量醋酸溶液:![]()
B.氯化铁溶液中加入铁粉:![]()
C.碳酸氢钠溶液中滴加氢氧化钡溶液:![]()
D.氯化亚铁溶液中滴加H2O2溶液:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】LED产品的使用为城市增添色彩。下图是氢氧燃料电池驱动LED发光的一种装置示意图。下列有关叙述正确的是
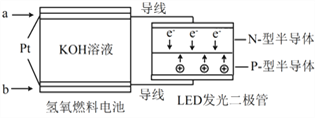
A. a处通入氧气, b处通氢气
B. 通入H2的电极发生反应:H2-2e- = 2H+
C. 通入O2的电极发生反应:O2 + 4e- + 2H2O = 4OH-
D. 该装置将化学能最终转化为电能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,无水硫酸铜粉末为受热分解生成CuO和气体A。气体A为SO2、SO3和O2中的一种或几种。请回答:
(1)只用一种试剂就能证明气体A中是否含有SO2,该试剂可以是__________;
a. 石蕊溶液 b. 品红溶液 c. 氯化钡溶液 d. 酸性高锰酸钾溶液
(2)对气体A的合理组成进行如下假设:
①只有SO3一种气体;②只有两种气体;③三种气体都有
若假设②成立,写出无水硫酸铜受热分解的反应方程式___________;
(3)若气体A中SO2、SO3和O2都有,用如图所示装置定量测定经NaOH溶液吸收后剩余气体体积(气体体积最后换算为标准状况)。
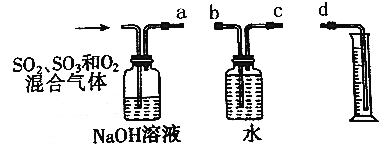
①装置的连接顺序为____________;(用字母表示);
②实验中测定的是_________气体的体积;
③实验发现测定结果比理论值明显偏低,其原因是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂离子电池应用很广。某种锂离子二次电池的电极材料主要是钴酸锂(LiCoO2)和石墨。钴是一种稀有的贵重金属,废旧锂离子电池电极材料的回收再生意义重大。
(1)锂离子电池(又称锂离子浓差电池)的工作原理:
ⅰ.充电过程:Li+从含LiCoO2的电极中脱出,正三价Co被氧化,此时该极处于贫锂态(Li1-xCoO2)。
ⅱ.放电过程原理示意图如图所示:
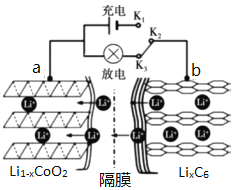
①放电时,电流从______(填“a”或“b”)极流出。
②充电时,a极的电极反应式为______。
(2)钴酸锂回收再生流程如下:
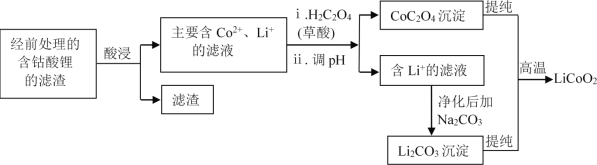
①用H2SO4酸浸时,通常添加30%的H2O2以提高浸出效率,其中H2O2的作用是______。
②用盐酸代替H2SO4和H2O2,浸出效率也很高,但工业上不使用盐酸,主要原因之一是:会产生有毒、有污染的气体。写出相应反应的化学方程式_______。
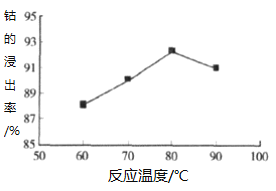
③其他条件不变时,相同反应时间,随着温度升高,含钴酸锂的固体滤渣在H2SO4和30% H2O2 混合液中的浸出率曲线如图,请解释温度高于80℃,钴的浸出率变化的原因:______。
④高温下,在O2存在时纯净的CoC2O4与Li2CO3再生为LiCoO2的化学方程式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据研究有机化合物的步骤和方法,填满下列空格:
实验步骤 | 解释或实验结论 |
(1)测得A的蒸气密度是同状况下甲烷的4.375倍,试通过计算填空: | (1)A的相对分子质量为_______。 |
(2)将此A 5.6g在足量纯O2中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重7.2g和17.6g | (2)A的实验式是________________。 (3)A的分子式为 _______________。 |
(3)将A通入溴水中,溴水褪色 | (4)说明A属于______________类(若溴水不褪色,则A属于 __________类) |
(4)A的核磁共振氢谱如图: | (5)综上所述,A的结构简式为 ______________。 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向一定量的Fe、FeO、Fe2O3、Fe3O4的混合物中加入100mL 1mol/L 的盐酸,恰好使混合物完全反应,放出 11.2mL(标准状况)气体,所得溶液加入 KSCN 溶液不变红色。用足量的CO 在高温下还原相同质量的此混合物,所得铁的质量为
A. 2.8g B. 11.2g C. 5.6g D. 无法计算
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法中正确的数目是
①12.0g熔融的NaHSO4中含有的阳离子数为0.2NA
②1mol Na2O 和Na2O2混合物中含有的阴、阴离子总数是3NA
③常温常压下,92g的NO2和N2O4混合气体含有的原子数为6NA
④7.8g![]() 中含有的碳碳双键数目为0.3NA
中含有的碳碳双键数目为0.3NA
⑤用1L1.0 mol/LFeCl3溶液制备氢氧化铁胶体,所得氢氧化铁胶粒的数目为NA
⑥1mol SO2与足量O2在一定条件下充分反应生成SO3,共转移2NA个电子
⑦在反应KIO3+6HI=KI+3I2 +3H2O 中,每生成3molI2转移的电子数为5NA
⑧常温常压下,17 g甲基(-14CH3)中所含的中子数为9NA
A. 3 B. 4 C. 5 D. 6
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com