
用
| A.质子数、 | B.中子数、 | C.最外层电子数、 | D.电子层数填写下列空格。 |
科目:高中化学 来源: 题型:填空题
Ⅰ.通常情况下,微粒A和B为分子,C和E为阳离子,D为阴离子,它们都含有10个电子;B溶于A后所得的物质可电离出C和D;A、B、E三种微粒反应后可得C和一种白色沉淀。请回答:
(1)用化学符号表示四种微粒:A________,B________,C________,D________。
(2)写出A、B、E三种微粒反应的离子方程式:____________________________________________________。
Ⅱ.(1)CH3+、CH3-、CH3-都是重要的有机反应中间体,它们的电子式分别是________、________、________;其中CH3+中四个原子是共平面的,三个键角相等,则键角应是________。
(2)叠氮化合物在化学工业上有重要应用。N3-叫做叠氮离子,请写出由三个原子构成的含有与N3-的电子数相同的粒子的化学式(3种)________、______、_______。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质)。
(1)把与下面元素有关性质相符的曲线标号填入相应的空格中: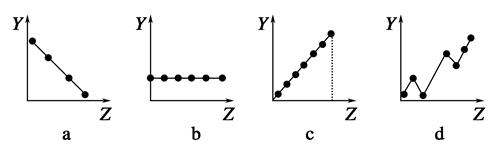
①第ⅡA族元素的价电子数________。
②第三周期元素的最高化合价________。
③F-、Na+、Mg2+、Al3+的离子半径________。
(2)元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。已知Y原子最外层电子数与核外电子总数之比为3∶4;M元素原子的最外层电子数与电子层数之比为4∶3;N-、Z+、X+的半径逐渐减小;化合物XN常温下为气体。据此回答:
①X为________(名称),Y为________(元素符号),Z原子结构示意图为________。
②N的最高价氧化物的水化物的化学式为__________。
③工业上制取单质M的化学方程式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
物质结构的多样性让人类使用的材料精彩纷呈。
(1)如图是原子序数相连的七种短周期元素第一电离能示意图。其中硼B元素是 (填图中元素代号)。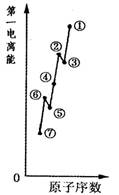
(2)乙二酸俗名草酸,是最简单的有机二元酸之一,结构简式为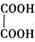 ,草酸钠晶体中存在 (填图中元素代号)。
,草酸钠晶体中存在 (填图中元素代号)。
A金属键;B非极性键;C键;D范德华力;E氢键;F离子键
(3)氧化锆(ZrO2)材料具有高硬度,高强度,高韧性,极高的耐磨性及耐化学腐蚀性,氧化锆陶瓷在许多领域获得广泛应用。锆石与钛同族的第五周期元素,锆原子的价电子排布式为 。
(4)含氧酸可电离的氢原子来自羟基,碳酸的结构式可表达为 ;若碳酸中的碳氧原子都在同一平面,则碳原子的杂化类型是 。
(5)PtCl4和氨水反应可获得PtCl4? 4NH3,PtCl4?4NH3 是一种配合物。100mL0.1mol?L-1PtCl4?4NH3 溶液中滴加足量AgNO3溶液可产生2.87g白色沉淀。该配合物溶于水的电离方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
元素周期表中前7周期的元素种类如下表所示:
| 周期数 | 一 | 二 | 三 | 四 | 五 | 六 | 七 |
| 元素种类 | 2 | 8 | 8 | 18 | 18 | 32 | 32 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
现有七种短周期主族元素,其原子序数按A、B、C、D、E、F、G的顺序递增。A元素的最高正化合价和最低负化合价的代数和等于0,且A是形成化合物种类最多的元素;C原子能形成分别含10电子、18电子的两种阴离子,且C与F位于同一主族;D单质投入冷水中反应缓慢,投入沸水中迅速产生气泡;E的简单阳离子是同周期元素所形成的简单离子中半径最小的。回答下列问题:
(1)B位于周期表第________周期第________族。
(2)A、B、C三种元素能形成等电子体,请写出其中一组等电子体:________________________________________________________________________。
(3)元素M位于E与F元素之间,且M单质是优良的半导体材料,广泛用于太阳能电池。M、F、G的气态氢化物的稳定性由强到弱的顺序为______________(用化学式表示)。
(4)若选择三种试剂设计实验能证明非金属性:B>A>M,用化学方程式表示实验原理:__________________________________________________。
(5)A、M、F、G的最高价氧化物对应水化物的酸性由强到弱的顺序为________________________(用化学式表示)。
(6)下列实验方法能证明D与E的金属性强弱关系的是________(填字母序号)。
A.比较D和E的单质分别与稀硫酸反应产生气泡的快慢
B.比较D和E的单质分别与同浓度的氢氧化钠溶液反应产生气泡的快慢
C.比较D和E的单质分别与氯气、氧气、硫等非金属单质反应的产物
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
X、Y、Z、M、N、Q为元素周期表前四周期的六种元素。其中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量(质量分数)最高的元素,M的内层电子数是最外层电子数的9倍,N的原子序数比M小1, Q在元素周期表的各元素中电负性最大。请回答下列问题:
(1)X元素在周期表中的位置是 ,属于 区元素,它的外围电子的电子排布图为 。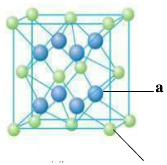
(2)XZ2分子的立体结构是 ,YZ2分子中Y的杂化轨道类型为 ,相同条件下两者在水中的溶解度较大的是 (写分子式),理由是 。
(3)含有元素N的盐的焰色反应为 色,许多金属盐都可以发生焰色反应,其原因是 。
(4)元素M与元素Q形成晶体结构如图所示,设其晶胞边长为a pm,则a位置与b位置之间的距离为_______pm(只要求列算式)。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
下面是元素周期表的一部分,参照元素①-⑧在表中的位置,请用化学用语回答下列问题:
| 族 周期 | IA | | 0 | |||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | | | | ② | ③ | ④ | | |
| 3 | ⑤ | | ⑥ | ⑦ | | | ⑧ | |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
A、B、C、D是原子序数均小于20的四种元素。A与B同主族,且能形成BA3型分子。B、C、D所形成的简单离子电子层结构相同,且B、C、D离子半径依次减小。据此回答下列问题:
(1)D元素在元素周期表中的位置是 。
(2)B与D所形成的化合物电子式为 。
(3)将C单质的水溶液滴加到B与D所形成化合物的水溶液中,产生淡黄色沉淀,其反应的化学方程式为 。
(4)实验室里除去BA2气体,可用下列试剂中的 (填字母)。
A.酸性高锰酸钾溶液 B.浓硫酸
C.NaOH溶液 D.品红溶液
(5)由A、B、D三种元素所组成的某种盐水溶液显碱性,其原因是 (用离子方程式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com