
A~J分别表示中学化学中常见的物质,它们之间的相互转化关系如图所示(部分反应物、生成物没有列出)。已知:G为金属元素的固态氧化物(常温下);A、B、C、D、E、F六种物质中均含有同一种元素。(已知F为红褐色沉淀)
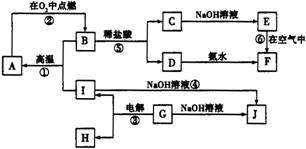
请填写下列空白:
(1)物质G的化学式是________。
(2)写出反应⑤的化学方程式________,写出反应④的离子方程式________。
(3)反应①~⑥中,不属于氧化还原反应的是________。(填序号)。
科目:高中化学 来源: 题型:
国际无机化学命名委员会在1989年作出决定,把长式周期表原先的主、副族及族号取消,由从左至右改为18列,碱金属族为第1列,稀有气体为第18列。按这个规定,下列说法不正确的是
A.第15列元素的最高价氧化物为R2O5 B.第2列元素中肯定没有非金属元素
C.第17列元素中的第一种元素的非金属性最强D.第16、17列元素都是非金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
下表是某地市场销售的一种“加碘食盐”包装袋上的部分文字说明。
| 配 料 | 氯化钠、碘酸钾 |
| 含碘量 | (20mg~40mg)/1kg |
| 保质期 | 18个月 |
| 食用方法 | 勿长时间炖炒 |
| 贮藏指南 | 避热、防潮 |
(1)已知碘在碘酸钾中的化合价为+5,1mol碘酸钾中共含5mol原子,则碘酸钾的化学式为 。
(2)碘酸钾与碘化钾在酸性条件下发生如下反应,配平化学方程式:
____ + KI+ H2SO4— K2SO4+ I2+ H2O
(3)上述反应生成的I2可用四氯化碳检验。向碘的四氯化碳溶液中加入Na2SO3稀溶液,将I2还原,以回收四氯化碳。某学生设计回收四氯化碳的操作步骤为:
a. 将碘的四氯化碳溶液置于分液漏斗中;
b. 加入适量Na2SO3稀溶液;
c. 分离出下层液体。
以上设计中遗漏的操作及在上述步骤中的位置是 。
(4)由食用方法和贮藏指南可推测碘酸钾的化学性质之一是 。
(5)用单质碘与氯酸钾发生置换反应可制得碘酸钾,该反应的化学方程式
为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
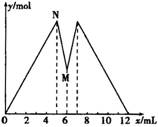
如图所示是向MgCl2和AlCl3的混合溶液中加入NaOH溶液和盐酸时沉淀的物质的量y mol与加入NaOH溶液和盐酸的体积x mL的关系图,根据图示判断,下列结论中不正确的是( )
A.N点时溶液中的溶质只有NaCl
B.原混合溶液中c (MgCl2)∶c (AlCl3)=1∶2
C.c (NaOH)=c (HCl)
D.M点之前加入的是NaOH溶液,M点之后加入的是盐酸
查看答案和解析>>
科目:高中化学 来源: 题型:
铝硅合金(含Si 13.5%)在凝固时的收缩率很小,因而这种合金适合铸造。①铝、②硅、③铝硅合金、④铝粉四种物质,其中熔点最低的是( )
A.① B.② C.③ D.④
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA 为阿伏加德罗常数的值。下列说法正确的是
A.1 L 0.1mol•L-1的氨水含有0.1NA个OH-
B.1 L 1 mol·L-1的NaClO溶液中含有ClO-的数目为NA
C.25℃时,pH =13的Ba(OH)2溶液中含有OH-的数目为0 .1 NA
D.在电解精炼粗铜的过程中,当阴极析出32 g铜时转移电子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
将6 mol A和5 mol B混合于4 L恒容密闭容器中,发生如下反应:3A(g)+B(g)  nC(g)+2D(g)
nC(g)+2D(g)
5 s后反应达到平衡状态,生成2 mol D,经测定以C表示的平均反应速率为0.1 mol·L-1·s-1。则下列结论中正确的是
A.5 s内以A表示的平均反应速率为0.15 mol·L-1·s-1
B.平衡时,B的浓度为1 mol·L-1
C.n值等于1
D.平衡时B的转化率为50%
查看答案和解析>>
科目:高中化学 来源: 题型:
向硫酸亚铁、硫酸铁、硫酸铜的混合溶液中加入铁粉,充分反应后过滤,滤渣中有铜粉和少量铁粉。那么此时的溶液中( )
A.肯定有Fe2+,可能有Fe3+ B.肯定有Fe3+,可能有Cu2+
C.肯定有Fe2+,可能有Fe3+和Cu2+ D.只有Fe2+,没有Fe3+和Cu2+
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA表示阿伏加德罗常数的数值,下列叙述中正确的是( )
A.1 mol NH3所含有的原子数为NA
B.常温常压下,22.4L氧气所含的原子数为2NA
C.常温常压下,48gO2和O3的混和物中所含氧原子数为3NA
D.1 L 0.1 mol/LNaCl溶液中所含的Na+为NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com