
【题目】(1)据科技日报网报道,南开大学科研团队借助镍和苯基硼酸共催化剂,首次实现烯丙醇高效、绿色合成。烯丙醇及其化合物可制成甘油、医药、农药、香料,合成维生素E和KI及天然抗癌药物紫杉醇中都含有关键的烯丙醇结构。丙烯醇的结构简式为CH2=CH-CH2OH。请回答下列问题:
①基态镍原子的价电子排布式为________。
②1 mol CH2=CH-CH2OH含___molσ键,烯丙醇分子中碳原子的杂化类型为___。
③Ni2+能形成多种配离子,如[Ni(NH3)6]2+、[Ni(CN)2]2- 和[Ni(SCN)2]- 等,与CN-互为等电子体的分子为_____。
(2)乙炔是有机合成工业的一种原料。工业上曾用CaC2与水反应生成乙炔。
①CaC2中C22-中碳与碳之间存在碳碳三键,C22-与O22+互为等电子体,O22+的电子式可表示为_______。
②乙炔与氢氰酸反应可得丙烯腈(H2C=CH-C≡N)。丙烯腈分子中碳原子轨道杂化类型是________。
【答案】3d84s2 9 sp2、sp3 N2(或CO等合理答案) ![]() sp、sp2杂化
sp、sp2杂化
【解析】
(1)①Ni是28号元素,原子核外电子排布式为:1s22s22p63s23p63d84s2,据此判断价电子的排布式;
②单键为σ键,双键含有1个σ键、1个π键,据此分析判断CH2=CH-CH2OH分子中含有的σ键数目;分子中碳原子均没有孤电子对,而碳碳双键中碳原子形成3个σ键,杂化轨道数目为3,另外碳原子形成4个σ键,杂化轨道数目为4;
③ 等电子体是指价电子数和原子数相同的分子、离子或原子团,据此书写与CN-互为等电子体的分子;
(2)①等电子体结构和性质相似,C22-与O22+和氮气互为等电子体,根据氮气分子电子式书写O22+电子式;
②根据价层电子对互斥理论判断C原子杂化类型。
(1)①Ni是28号元素,原子核外电子排布式为:1s22s22p63s23p63d84s2,属于过渡元素,价电子包括3d与4s能级电子,即价电子排布式为:3d84s2,故答案为:3d84s2;
②单键为σ键,双键含有1个σ键、1个π键,CH2=CH-CH2OH分子含有9个σ键,故1molCH2=CH-CH2OH含9molσ键;分子中碳原子均没有孤电子对,而碳碳双键中碳原子形成3个σ键,杂化轨道数目为3,C原子的杂化方式为sp2杂化,另外碳原子形成4个σ键,杂化轨道数目为4,碳原子采取sp3杂化,故答案为:9;sp2、sp3;
③ 等电子体是指价电子数和原子数相同的分子、离子或原子团,则与CN-互为等电子体的分子为N2或CO,故答案为: N2或CO;
(2)①等电子体结构和性质相似,C22-与O22+和氮气互为等电子体,根据氮气分子的电子式可知,O22+电子式为![]() ,故答案为:
,故答案为:![]() ;
;
②H2C=CH-C≡N分子中连接双键的C原子价层电子对个数是3且不含孤电子对,所以为sp2杂化,连接三键的碳原子价层电子对个数是2且不含孤电子对,所以C原子采用sp杂化,故答案为:sp、sp2。


科目:高中化学 来源: 题型:
【题目】X、Y、Z、U、W是原子序数依次增大的前四周期元素.其中Y的原子核外有7种运动状态不同的电子;X、Z中未成对电子数均为2; U的氧化物是第三周期元素形成的常见两性氧化物;W的内层电子全充满,最外层只有1个电子。请回答下列问题:
(1)X、Y、Z的电负性从大到小的顺序是_______ (用元素符号表示,下同)。三种元素的第一电离能由大到小的顺序为__________。
(2)写出Y的价电子排布式____,W同周期的元素中,与W原子最外层电子数相等的元素还有________。
(3)根据等电子体原理,可知化合物XZ的结构式是________, YZ2-的VSEPR模型是________。
(4)X、Y、Z的简单氢化物的键角从大到小的顺序是________ (用化学式表示),原因是_____________。
(5)Y的氢化物易液化的原因是___________。
(6)XZ32-的立体构型是________,其中X原子的杂化轨道类型是________,互为等电子体的离子________。
(7)用氢键表示式写出Z的氢化物中存在的氢键________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. NH3和CH4的中心原子都是sp3杂化
B. 基态原子的核外电子排布为[Kr]4d105s1的元素属于d区
C. SO2和CO2都是直线形分子,其中心原子都是sp杂化
D. 电子由低能级跃迁至较高能级时,可通过光谱仪直接摄取原子的发射光谱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碱式硫酸铝溶液可用于烟气脱硫。室温下向一定浓度的硫酸铝溶液中加入一定量的碳酸钙粉末,反应后经过滤得到碱式硫酸铝溶液,反应方程式为(2x)Al2(SO4)3+3xCaCO3+3xH2O=2[(1x)Al2(SO4)3·xAl(OH)3]+3xCaSO4↓+3xCO2↑。生成物(1x)Al2(SO4)3·xAl(OH)3中x值的大小影响碱式硫酸铝溶液的脱硫效率。
通过测定碱式硫酸铝溶液中相关离子的浓度确定x的值,测定方法如下:
①取碱式硫酸铝溶液25.00 mL,加入盐酸酸化的过量BaCl2溶液充分反应,静置后过滤、洗涤,干燥至恒重,得固体2.3300 g。
②取碱式硫酸铝溶液2.50 mL,稀释至25 mL,加入0.1000 mol·L1EDTA标准溶液25.00 mL,调节溶液pH约为4.2,煮沸,冷却后用0.08000 mol·L1CuSO4标准溶液滴定过量的EDTA至终点,消耗CuSO4标准溶液20.00 mL(已知Al3+、Cu2+与EDTA反应的化学计量比均为1∶1)。
计算(1x)Al2(SO4)3·xAl(OH)3中的x值(写出计算过程)___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
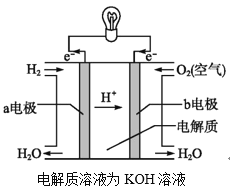
【题目】液体燃料电池相比于气体燃料电池具有体积小等优点.一种以液态肼(N2H4)为燃料的电池装置如图所示,该电池用空气中的氧气作为氧化剂,KOH溶液作为电解质溶液.关于该电池的叙述正确的是( )

A. b极发生氧化反应
B. a极为该电池的正极
C. 放电时,电流从a极经过负载流向b极
D. a极的反应式:N2H4+4OH﹣﹣4e﹣═N2↑+4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源是现代文明的原动力,通过化学方法可以使能量按人们所期望的形式转化,从而开辟新能源和提高能源的利用率。
(1)氢气燃烧,该反应是___反应(填“吸热”或“放热”),这是由于反应物的总能量___(填“大于”“小于”或“等于”)生成物的总能量;从化学反应的本质来看,是由于断裂反应物中的化学键吸收的总能量___(填“大于”“小于”或“等于”)形成产物的化学键放出的总能量。
(2)通过氢气的燃烧反应,可以把氢气中储存的化学能转化为热能,如果将该氧化还原反应设计成原电池装置,就可以把氢气中储存的化学能转化为电能,如图就是能够实现该转化的装置,被称为氢氧燃料电池。
该电池的正极是___(填“a电极”或“b电极”),电极反应式为___,该电极上的物质发生反应的反应类型是___(填“氧化反应”或“还原反应”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】肉桂酸甲酯(![]() )常用于调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精。
)常用于调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精。
(1)肉桂酸甲酯中含氧官能团的名称是_________
(2)下列有关肉桂酸甲酯的叙述中,正确的是_________(填字母);
A.不能与溴的四氯化碳溶液发生加成反应
B.可以使酸性高锰酸钾溶液褪色
C.在碱性条件下能发生水解反应
D.难以发生加聚反应
(3)G为肉桂酸甲酯的一种同分异构体,其分子结构模型如下图所示(图中球与球之间连线表示单键或双键)。则G的结构简式为_________

(4)用芳香烃A为原料合成G的路线如下:
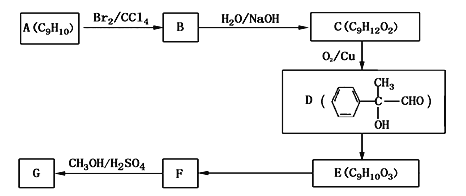
①A的结构简式________
②E→F的反应类型是_______
③C→D的化学方程式为__________________
④写出符合下列条件的F的同分异构体的结构简式__________
ⅰ.分子内含苯环,且苯环上只有一个支链;
ⅱ.一定条件下,1mol该物质与足量银氨溶液充分反应,生成4mol银单质。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通过海水晾晒可得粗盐,粗盐除NaCl外,还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质。以下是制备精盐的实验方案,各步操作流程如图:

(1)在第①步粗盐溶解操作中要用玻璃棒搅拌,作用是______。
(2)第②步操作的目的是除去粗盐中的______(填化学式,下同),第⑥步操作的目的是除去滤液中______。
(3)第⑤步“过滤”操作中得到沉淀的成分有:泥沙、BaSO4、Mg(OH)2、______(填化学式)。
(4)在第③步操作中,选择的除杂的试剂不能用KOH代替NaOH,理由是______。
(5)实验所得精盐的质量大于粗盐中NaCl的质量,原因是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示装置,电流表指针发生偏转,同时A极逐渐变粗,B极逐渐变细,C为电解质溶液,则A、B、C应是下列各组中的( )
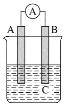
A.A是Zn,B是Cu,C为稀硫酸
B.A是Cu,B是Zn,C为稀硫酸
C.A是Ag,B是Fe,C为稀AgNO3溶液
D.A是Fe,B是Ag,C为稀AgNO3溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com