
(15分)某校化学兴趣小组为探究SO2气体的还原性设计了如下装置图:

(1)SO2气体还原Fe3+的离子反应方程式为 ;
(2)实验中所需的SO2气体可以用浓硫酸和铜反应来制取,该反应的化学方程式为
,在反应表现了H2SO4的哪些性质 。
(3)装置C的作用是 。
(4)若要从A中得到溶液提取晶体,必须进行的实验操作步骤:蒸发、冷却结晶、过滤、自然干燥,在这一系列操作中没有用到的仪器有 (填字母序号)。
A.蒸发皿 B.石棉网 C.漏斗 D.烧杯
E.玻璃棒 F.坩埚
(5)在上述装置中通入过量的SO2,为了验证A中SO2与Fe3+发生了氧化还原反应他们取A中的溶液,分成三份,并设计了如下实验:
方案①:往第一份试液中加入KMnO4溶液,不变红,紫色褪去。
方案②:往第二份试液加入KSCN溶液,不变红,再加入新制的氯水,溶液变红。
方案③:往第三份试液加入用稀盐酸酸化的BaCl2,产生白色沉淀
上述方案不合理的一个方案 (填数字序号),原因是 。
(6)上述装置中能表明I-的还原性弱于SO2的现象是 。
 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

| 钠块质量 | 实验现象 |
| 0.2g | 钠块剧烈燃烧,发出爆炸声,少量的钠溅出 |
| 0.1g | 钠块燃烧,发出爆炸声 |
| 0.05g | 钠块四处游动,偶有轻微的爆炸声,未见钠块燃烧 |
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
(15分)某校化学兴趣小组为探究SO2气体的还原性设计了如下装置图:
(1)SO2气体还原Fe3+的离子反应方程式为 ;
(2)实验中所需的SO2气体可以用浓硫酸和铜反应来制取,该反应的化学方程式为
,在反应表现了H2SO4的哪些性质 。
(3)装置C的作用是 。
(4)若要从A中得到溶液提取晶体,必须进行的实验操作步骤:蒸发、冷却结晶、过滤、自然干燥,在这一系列操作中没有用到的仪器有 (填字母序号)。
A.蒸发皿 B.石棉网 C.漏斗 D.烧杯
E.玻璃棒 F.坩埚
(5)在上述装置中通入过量的SO2,为了验证A中SO2与Fe3+发生了氧化还原反应他们取A中的溶液,分成三份,并设计了如下实验:
方案①:往第一份试液中加入KMnO4溶液,不变红,紫色褪去。
方案②:往第二份试液加入KSCN溶液,不变红,再加入新制的氯水,溶液变红。
方案③:往第三份试液加入用稀盐酸酸化的BaCl2,产生白色沉淀
上述方案不合理的一个方案 (填数字序号),原因是 。
(6)上述装置中能表明I-的还原性弱于SO2的现象是 。
查看答案和解析>>
科目:高中化学 来源:2012届山东省临沂市苍山县高三上学期期末检测化学试卷 题型:填空题
(15分)某校化学兴趣小组为探究SO2气体的还原性设计了如下装置图: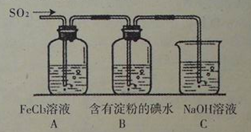
(1)SO2气体还原Fe3+的离子反应方程式为 ;
(2)实验中所需的SO2气体可以用浓硫酸和铜反应来制取,该反应的化学方程式为
,在反应表现了H2SO4的哪些性质 。
(3)装置C的作用是 。
(4)若要从A中得到溶液提取晶体,必须进行的实验操作步骤:蒸发、冷却结晶、过滤、自然干燥,在这一系列操作中没有用到的仪器有 (填字母序号)。
| A.蒸发皿 | B.石棉网 | C.漏斗 | D.烧杯 |
查看答案和解析>>
科目:高中化学 来源:2012-2013学年河北省高三9月月考化学化学试卷(解析版) 题型:实验题
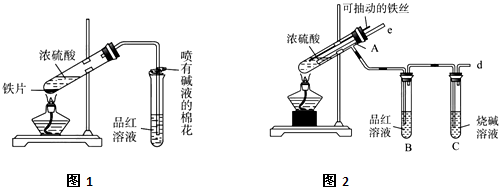
(13分)某校化学兴趣小组为探究铁与浓硫酸的反应,设计了图1、图2所示装置进行实验。

(1)比较两个实验装置,图2装置的优点是:
①能更好的吸收有毒气体SO2防止其污染环境;
② 。
(2)导气管e有两个主要作用:一是在反应过程中,因导管插入液面下,可起到”液封”作用阻止SO2气体逸出而防止污染环境;二是 。
(3)能说明有SO2气体产生的实验现象是 。
(4)反应一段时间后,用滴管吸取A试管中的溶液滴入到适量水中作为试样,试样中所含金属离子的成分有以下三种可能:
Ⅰ:只含有Fe3+;Ⅱ:只含有Fe2+;Ⅲ:既有Fe3+又有Fe2+。
为验证Ⅱ、Ⅲ的可能性,选用如下试剂,填写下列空格:
A.稀HCl溶液 B.稀硫酸 C.KSCN溶液 D.酸性KMnO4溶液
E.NaOH溶液 F.淀粉KI溶液 G. H2O2溶液
验证Ⅱ:取试样,先滴加少量的 (填试剂序号,下同),振荡,再滴加少量的 ,根据溶液颜色的变化可确定假设Ⅱ是否正确。
验证Ⅲ:步骤1.取试样,滴加少量的 (填试剂序号),溶液的颜色变 色,则试样中含有Fe3+发生反应的离子方程式为 。
步骤2.再取适量的试样滴加少量的 (填试剂序号),溶液颜色的变化为 ,则试样中含有Fe2+。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com