
A、 |
B、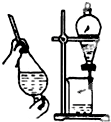 |
C、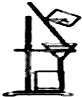 |
D、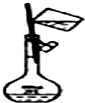 |
科目:高中化学 来源: 题型:
| A、正反应活化能小于100kJ?mol-1 |
| B、逆反应活化能一定小于100kJ?mol-1 |
| C、逆反应反应活化能大于100kJ?mol-1 |
| D、正反应活化能比逆反应活化能大100kJ?mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 35 | 50 | 60 | 70 | 80 |
| 温度/℃ | 25 | 26 | 26 | 26 | 26 | 26 | 26.5 | 27 | 27 | 27 | 27 |
| 实验 编号 | 铜片 质量/g | 0.1mol?L-1的 硝酸体积/mL | 硝酸铜 晶体/g | 亚硝酸钠 晶体/g | 实验目的 |
| ① | 5 | 20 | 0 | 0 | 实验①和②探究 |
| ② | 5 | 0.5 | |||
| ③ | 5 | 20 | 0.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:
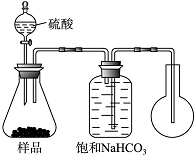 碳酸氢钠是一种在生产、生活实际中有着重要用途的化合物.某课外兴趣活动小组的同学进行了以下的实验活动.
碳酸氢钠是一种在生产、生活实际中有着重要用途的化合物.某课外兴趣活动小组的同学进行了以下的实验活动.| 温度/℃ | 10 | 20 | 30 | 加热煮沸后,冷却至50℃ |
| pH | 8.3 | 8.4 | 8.5 | 8.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③ | B、①③④ |
| C、④⑤⑥ | D、①②⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| △ |
| t/min | 0 | 5 | 10 |
| AO/mol?Lˉ1 | 1.00 | 0.65 | 0.50 |
| H2/mol?Lˉ1 | 2.00 | 1.00 | |
| AH3OH/mol?Lˉ1 | 0.00 | 0.35 | 0.50 |
查看答案和解析>>
科目:高中化学 来源: 题型:
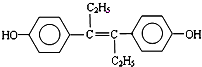
| A、M属于芳香族化合物 |
| B、M可与NaOH溶液或NaHCO3溶液发生反应 |
| C、1molM最多能与7molH2发生加成反应 |
| D、1molM与饱和溴水混合,最多消耗5molBr2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com