
A、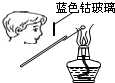 检验K2CO3中的K+ |
B、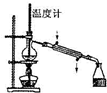 制蒸馏水 |
C、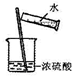 稀释浓硫酸 |
D、 除去CO的CO2 |


科目:高中化学 来源: 题型:
| CH3COOH | H2CO3 | H2S | H3PO4 |
| 1.8×10-5 mol?L-1 | K1=4.3×10-7 mol?L-1 K2=5.6×10-11 mol?L-1 | K1=9.1×10-8 mol?L-1 K2=1.1×10-12 mol?L-1 | K1=7.5×10-3 mol?L-1 K2=6.2×10-8 mol?L-1 K3=2.2×10-13 mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | CH3CH3+Cl2
CH2=CH2+HCl→CH3CH2Cl | 均为取代反应 | ||
| B | 明矾用于净水 碳酸钠溶液显碱性 | 均发生了水解反应 | ||
| C | Cl2+2Br?=2Cl?+Br2 Zn+Cu2+=Zn2++Cu | 均为单质被还原的置换反应 | ||
| D | 2Na2O2+2H2O=4NaOH+O2↑ Cl2+H2O=HCl+HClO | 均为水作还原剂的氧化还原反应 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cu2++2OH-=Cu(OH)2 CuCO3+2NaOH=Cu(OH)2+Na2CO3 |
| B、CO32-+2H+=CO2+H2O BaCO3+2HCl=BaCl2+CO2+H2O |
| C、Ca2++CO32-=CaCO3 Ca(NO3)2+Na2CO3=CaCO3+NaNO3 |
| D、H++OH-=H2O 2KOH+H2SO4=K2SO4+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 2 |
| 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
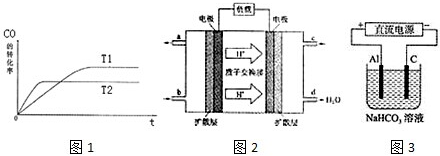
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com