
| 2 |
| 3 |
| 2 |
| 3 |


 �����Ƹ���ʦ����ϵ�д�
�����Ƹ���ʦ����ϵ�д� ��ͨ����ͬ����ϰ��ϵ�д�
��ͨ����ͬ����ϰ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����������Է���������ͬ�����ṹ��ͬ��������һ����ͬ���칹�� |
| B���л��������֮�䲻���ܳ���ͬ���칹�� |
| C���л�������Ϊͬ���칹�壬������һ������Ϊͬϵ�� |
| D�������л�������̼Ԫ�ص�����������ͬ��������һ��Ϊͬ���칹�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��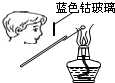 ����K2CO3�е�K+ |
B��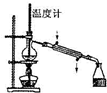 ������ˮ |
C��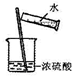 ϡ��Ũ���� |
D�� ��ȥCO��CO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
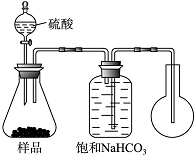 ̼��������һ��������������ʵ����������Ҫ��;�Ļ����ij������Ȥ�С���ͬѧ���������µ�ʵ����
̼��������һ��������������ʵ����������Ҫ��;�Ļ����ij������Ȥ�С���ͬѧ���������µ�ʵ����| �¶�/�� | 10 | 20 | 30 | ������к���ȴ��50�� |
| pH | 8.3 | 8.4 | 8.5 | 8.8 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���٢ڢ� | B���٢ۢ� |
| C���ܢݢ� | D���٢ڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
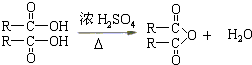
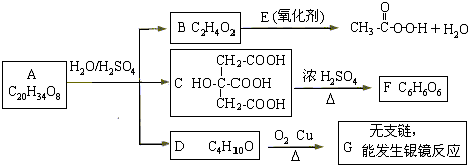
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �� |
| t/min | 0 | 5 | 10 |
| AO/mol?L��1 | 1.00 | 0.65 | 0.50 |
| H2/mol?L��1 | 2.00 | 1.00 | |
| AH3OH/mol?L��1 | 0.00 | 0.35 | 0.50 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A�� |
B�� |
C��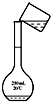 |
D�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��0.01mol/L��CH3COOH |
| B��0.01mol/LHCl0 |
| C��0.01mol/LHF |
| D��0.005mol/LH2SO4 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com