
【题目】铁是人类应用较早,当前应用量最大的金属元素。下列有关说法中正确的是( )
A.人类使用铁制品在铝之后
B.常温下,铁不能与浓硝酸反应
C.铁与水蒸气在高温下的反应产物为Fe2O3和H2
D.除去FeCl3溶液中的FeCl2杂质可以向溶液中加入适量氯水
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】硼酸(H3BO3)是一种重要的化工原料,广泛应用于玻璃、医药、肥料等工艺。一种以硼镁矿(含Mg2B2O5·H2O、SiO2及少量Fe2O3、Al2O3)为原料生产硼酸及轻质氧化镁的工艺流程如下:
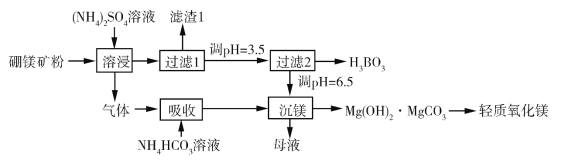
回答下列问题:
(1)在95 ℃“溶侵”硼镁矿粉,产生的气体在“吸收”中反应的化学方程式为_________。
(2)“滤渣1”的主要成分有_________。为检验“过滤1”后的滤液中是否含有Fe3+离子,可选用的化学试剂是_________。
(3)根据H3BO3的解离反应:H3BO3+H2O![]() H++B(OH)4,Ka=5.81×1010,可判断H3BO3是_______酸;在“过滤2”前,将溶液pH调节至3.5,目的是_______________。
H++B(OH)4,Ka=5.81×1010,可判断H3BO3是_______酸;在“过滤2”前,将溶液pH调节至3.5,目的是_______________。
(4)在“沉镁”中生成Mg(OH)2·MgCO3沉淀的离子方程式为__________,母液经加热后可返回___________工序循环使用。由碱式碳酸镁制备轻质氧化镁的方法是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一固定容积的密闭容器中,进行如下反应:C(s)+ H2O(g)CO(g)+ H2(g)
(1)若容器容积为2L,反应10s氢气质量增加0.4g,则该时间内一氧化碳的反应速率为___mol/(L·s)。
(2)若增加碳的量,则正反应速率_____。(选填“增大”、“减小”、“不变”)
(3)该反应达到平衡状态的标志是______。
a.压强不变 b.v正(H2)= v正(H2O) c.c(CO)不变 d.c(H2O)= c(CO)
(4)若升高温度,平衡向右移动,则正反应是___________反应。(选填“吸热”或“放热”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮是生命物质中重要的组成元素之一。含氮物质的使用既给人类带来福音,又给人们带来一些负面影响。
(1)肥料的三要素,除了氮还有____。
(2)NH3是氮的氢化物,它的空间构型是_____,属于____分子(填写“极性”或“非极性”),N原子的结构示意图是____。
(3)氨的水溶液叫做氨水,它可作为化学肥料。实际使用时,因为有很多不便,所以往往制成铵盐。NH4Cl就是常见的铵盐,NH4Cl属于___晶体,长期使用含NH4Cl的氮肥会使土壤___(填写“酸”或“碱”)化,请结合有关方程式说明原因____。
(4)工业上通常以铁触媒为催化剂,在500℃左右,20~50MPa下合成氨气。采用该压强的原因是____。
(5)含氮废水进入水体会对环境造成污染,某课题小组利用废铝将NO3-还原为N2,从而消除污染。其反应如下:6NO3-+10Al+18H2O→3N2↑+10Al(OH)3+6OH-,该反应中,还原剂是____,被还原的元素是____;每生成2molN2,转移的电子数是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】今年是俄罗斯化学家门捷列夫提出“元素周期律”150周年。门捷列夫为好几种当时尚未发现的元素(如“类铝”“类硅”和“类硼”)留下了空位。而法国科学家在1875年研究闪锌矿(ZnS)时发现的“镓”,正是门捷列夫预言的“类铝”,其性质也是和预言中的惊人相似。请回答下列问题:
(1)①基态镓原子中,核外存在__________对自旋相反的电子,核外电子占据的最高能级的电子云轮廓图为__________形;门捷列夫预言的“类硼”就是现在的钪,“类硅”即是现在的锗。在镓、钪、锗三种元素的原子中,未成对电子数最多的是_________ (填元素符号)。
②下列说法中,最有可能正确的一项是_________(填字母代号)。
A 类铝在100℃时蒸气压很高 B 类铝的氧化物一定不能溶于强碱溶液
C 类铝一定不能与沸水反应 D 类铝能生成类似明矾的矾类
(2)氯化镓晶体熔点为77.9℃。氯化镓分子中镓的杂化方式为_______,空间构型为_______;写出与氯化镓互为等电子的的分子、离子各一种:_______、_______。
(3)GaN、GaP、GaAs都是很好的半导体材料,晶体类型与晶体硅类似,GaN、GaP、GaAs晶体的熔点如下表所示,分析其变化原因:__________________。
GaN | GaP | GaAs | |
熔点 | 1700℃ | 1480℃ | 1238℃ |
(4)2011年,我国将镓列为战略储备金属,我国的镓储量约占世界储量的80%以上。砷化镓也是半导体材料,其结构与硫化锌类似,其晶胞结构如下图所示:

①原子坐标参数是晶胞的基本要素之一,表示晶胞内部各原子的相对位置。图中A(0,0,0)、B(![]() )、C(1,
)、C(1,![]() ,
,![]() ),则此晶胞中,距离A球最远的黑球的坐标参数为______________。
),则此晶胞中,距离A球最远的黑球的坐标参数为______________。
②若砷和镓的原子半径分别为a cm和b cm,砷化镓的摩尔质量为M g/mol,密度为![]() g/cm3,晶胞中原子体积占空间体积百分率(即原子体积的空间占有率)为_________ (用含a、b、M、
g/cm3,晶胞中原子体积占空间体积百分率(即原子体积的空间占有率)为_________ (用含a、b、M、![]() 、NA的代数式表示,NA表示阿伏加德罗常数的值)。
、NA的代数式表示,NA表示阿伏加德罗常数的值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L密闭容器内,t℃时发生反应:N2(g)+3H2(g)![]() 2NH3(g),在体系中,n(N2)随时间的变化如下表:
2NH3(g),在体系中,n(N2)随时间的变化如下表:
时间(min) | 0 | 1 | 2 | 3 | 4 | 5 |
N2的物质的量(mol) | 0.20 | 0.10 | 0.08 | 0.06 | 0.06 | 0.06 |
(1)上述反应在第5min时,N2的转化率为___;
(2)用H2表示从0~2min内该反应的平均速率v(H2)=___;
(3)t℃时,在4个均为2L密闭容器中不同投料下进行合成氨反应。根据在相同时间内测定的结果,判断该反应进行快慢的顺序为___。(用字母填空,下同);
a.v(NH3)=0.05mol·L-1·min-1
b.v(H2)=0.03mol·L-1·min-1
c.v(N2)=0.02mol·L-1·min-1
d.v(H2)=0.00lmol·L-1·s-1
(4)下列表述能作为反应达到化学平衡状态的标志是___。
a.反应速率v(N2)∶v(H2) ∶v(NH3)=1∶3∶2
b.各组分的物质的量浓度不再改变
c.混合气体的平均相对分子质量不再改变
d.混合气体的密度不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作能达到实验目的的是
A.将pH试纸放在实验台上测量溶液的pH
B.通过蒸干FeCl3溶液制取无水FeCl3固体
C.可用热的烧碱溶液区分植物油和矿物油
D.将8 g NaOH固体置于100 mL容量瓶中,加水至刻度线,配制2 mol·L-1 NaOH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨对人类生存具有重大意义,反应为:N2(g)+3H2(g)![]() 2NH3(g) H
2NH3(g) H
(1)科学家研究在催化剂表面合成氨的反应机理,反应步骤与能量的关系如图所示(吸附在催化剂表面的微粒用*标注,省略了反应过程中部分微粒)。
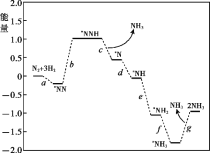
① NH3的电子式是_______。
② 写出步骤c的化学方程式_______。
③ 由图像可知合成氨反应的H______0(填“>”、“<”或“=”)。
(2)传统合成氨工艺是将N2和H2在高温、高压条件下发生反应。若向容积为1.0 L的反应容器中投入5 mol N2、15 mol H2,在不同温度下分别达平衡时,混合气中NH3的质量分数随压强变化的曲线如图所示:

① 温度T1、T2、T3大小关系是_______。
② M点的平衡常数 K = _______(可用分数表示)。
(3)目前科学家利用生物燃料电池原理(电池工作时MV2+/MV+在电极与酶之间传递电子),研究室温下合成氨并取得初步成果,示意图如下:
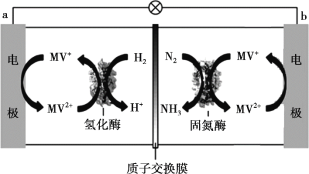
① 导线中电子移动方向是_______。
② 固氮酶区域发生反应的离子方程式是_______。
③ 相比传统工业合成氨,该方法的优点有_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂用含淀粉质量分数为76%的陈化粮10.0t来制取乙醇。如果在发酵过程中有81%的淀粉转化为乙醇,制得的乙醇溶液中含乙醇质量分数为40%,则可制得这样的乙醇溶液质量是
A. 8.74 tB. 9.45tC. 9.88tD. 10.25t
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com