
����Ŀ��̼����Ԫ�صĵ��ʼ��仯�����ǹ�����Ȼ�����Ҫ���ʡ�
��1������������л��ʵ���ҿ�ͨ�����з�Ӧ��ȡ��
CH3COONa��NaOH![]() CH4����X(����ƽ)
CH4����X(����ƽ)
��X���� ���壨������ͣ���
��MgO������۵��CaO�ߣ���Ҫԭ���� ��
��2��C60�����ʯ��ʯī��������Ҫ��̼���ʣ��ṹģ�ͷֱ�����ͼ��ʾ������ʯī����ʾ�����е�һ��ṹ����
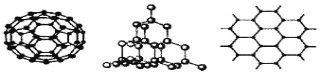
�����ʯ��̼ԭ�ӵ��ӻ���ʽΪ ��
��ʯī��״�ṹ�У�ƽ��ÿ����������ռ�е�C��C������ ����
���𰸡���1�������ӣ���Mg2���뾶��Ca2��С�����MgO����ľ����ܽϴ��۵�ϸߣ���2����sp3����3��
��������
�����������1�����ݷ�Ӧǰ��Ԫ���غ㡢ԭ�Ӹ����غ㣬XΪN2CO3�������Σ��������ӻ�����������������ӻ����������Խ���۷е�Խ�ߣ�����������������������Ӱ뾶�йأ��뾶ԽС�����������Խ�࣬������Խ���۷е�Խ�ߣ�Mg2���İ뾶С��Ca2����(2)�����ݽ��ʯ�Ľṹ��C��4���������µ��Ӷԣ�����ӻ�����Ϊsp3��������ʯī�Ľṹ��ÿ��C��C��2��ƽ�������ι��ã��������һ�������ε�C-C�ĸ���Ϊ6��1/2=3��


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�˼���ij����NaHCO3���ʵ�Na2CO3��Ʒ�Ĵ��ȣ��ֽ�w1 g��Ʒ���ȣ���������Ϊw2 g�������Ʒ��Na2CO3�Ĵ���(��������)��
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪N2+O2=2NOΪ���ȷ�Ӧ����H=+180 kJ��mol��1������N��N��O=O���ļ��ֱܷ�Ϊ946 kJ��mol��1��498 kJ��mol��1����N-O���ļ���Ϊ�� ��
A��1264 kJ��mol��1 B��632 kJ��mol��1 C��316 kJ��mol��1 D��1624 kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��д�����������ӷ���ʽ���Ӧ�Ļ�ѧ����ʽ��
(1)H+ + OH�� == H2O ��______________________________________���𰸲�Ψһ����
(2)2H+ + CO32�� == H2O + CO2�� ��____________________________���𰸲�Ψһ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��1mol MgSO4��7H2O���нᾧˮ������Ϊ( )
A.16 g
B.18 g
C.112 g
D.126 g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ģ�ͷֱ��ʾC2H2��S8��SF6�Ľṹ������˵���������ǣ� ��
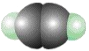

A��32 g S8�������0.125 mol ����
B��SF6���ɼ��Լ����ɵķǼ��Է���
C��1 mol C2H2��������3 mol ������2 mol ����
D��1 mol S8���8 mol S��S��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������мȺ��й��ۼ��ֺ������Ӽ����ǣ� ��
A.NaI
B.CaCl2
C.NO2
D.KNO3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ��������NaHCO3��Ϊ���ȷݣ���һ��ֱ�Ӽ��������У������������ʵ���Ϊn1���ڶ������ȼ��ȣ�ʹ�䲿�ַֽ���ټ��������У������������ʵ���Ϊn2�����������ȼ��ȣ�ʹ����ȫ�ֽ���ټ��������У������������ʵ���Ϊn3�����������ᶼ��ȫ��Ӧ����n1��n2��n3�Ĵ�С��ϵ��ȷ����(����)
A. n1>n2>n3 B. n2>n1>n3 C. n1��n2��n3 D. n1>n3>n2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����й�����ϩ�������˵���У�����ȷ����( )
A. ��ϩ���ڲ������������������ڱ�������
B. ��ϩ����������ԭ�Ӵ���ͬһƽ���ϣ����������Ϊ����ṹ������ԭ�Ӳ���ͬһƽ����
C. ��ϩ���ӵ�C=C������һ����������
D. ��ϩ���ӵ�C=C����������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com