
【题目】在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图所示,下列表述正确的是( )

A. 此反应的化学方程式为2M = N
B. t2时,正逆反应速率相等,达到平衡
C. t3时,正反应速率大于逆反应速率
D. t1时,N的浓度是M浓度的2倍
 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】方铅矿(主要成分是PbS,含少量ZnS、Fe、Ag)是提炼铅及其化合物的重要矿物,其工艺流程如下:

回答下列问题:
(1)流程中“趁热”过滤的原因是_____________,滤渣的主要成分是_________________。
(2)该工艺流程中可循环利用的物质是__________________。
(3)PbSO4与PbS在加热条件下发生反应的化学方程式为_____________________。
(4)《药性论》中有关铅丹(Pb3O4)的描述是:“治惊悸狂走,呕逆,消渴。”将PbO高温焙烧可制得铅丹,铅丹中含有的PbO与Al2O3性质相似,可用氢氧化钠溶液提纯铅丹,提纯时发生反应的离子方程是_______________。
(5)以石墨为电极,电解Pb(NO3)2溶液制备PbO2,电解过程中阳极的电极反应式为____________;若电解过程中以铅蓄电池为电源,当电解装置中阳极增重23.9g时(忽略副反应),理论上蓄电池负极增重_____g。
(6)取一定量含有Pb2+、Cu2+的工业废水,向其中滴加Na2S溶液,当PbS开始沉淀时,溶液中 =__________。(已知KSP(PbS)=3.4×10-28,Ksp(CuS)=1.3×10-36)
=__________。(已知KSP(PbS)=3.4×10-28,Ksp(CuS)=1.3×10-36)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙三瓶溶液分别为NaCl、NaBr、KI,向甲中加入淀粉溶液和氯水,则溶液变为橙色,再加入丙溶液,颜色无明显变化,则甲、乙、丙依次含有
A. NaBr NaCl KI B. NaBr KI NaCl
C. KI NaBr NaCl D. NaCl KI NaBr
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物G是一种医药中间体,常用于制备抗凝血药。可以通过下图所示的路线合成:

已知:RCOOH![]() RCOCl;D与FeCl3溶液能发生显色。
RCOCl;D与FeCl3溶液能发生显色。
请回答下列问题:
⑴B→C的转化所加的试剂可能是__________,C+E→F的反应类型是_______。
⑵有关G的下列说法正确的是_________。
A.属于芳香烃 B.能与FeCl3溶液发生显色反应
C.可以发生水解、加成、氧化、酯化等反应 D.1mol G最多可以跟4mol H2反应
⑶E的结构简式为_________。
⑷F与足量NaOH溶液充分反应的化学方程式为__________________________________。
⑸写出同时满足下列条件的E的同分异构体的结构简式_______________。
①发生水解反应②与FeCl3溶液能发生显色反应③苯环上有两种不同化学环境的氢原子
⑹已知:酚羟基一般不易直接与羧酸酯化。而苯甲酸苯酚酯(![]() )是一种重要的有机合成中间体。试写出以苯酚、甲苯为原料制取该化合物的合成路线流程图(无机原料任用)。注:合成路线的书写格式参照如下示例流程图:_________________
)是一种重要的有机合成中间体。试写出以苯酚、甲苯为原料制取该化合物的合成路线流程图(无机原料任用)。注:合成路线的书写格式参照如下示例流程图:_________________
CH3CHO![]() CH3COOH
CH3COOH![]() CH3COOCH2CH3
CH3COOCH2CH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯是石油裂解气的主要成分,其产量通常用来衡量一个国家的石油化工水平。在一定条件下,有如下转化:

(1)乙烯的电子式是___________________。
(2)由重油生产乙烯的裂解反应属于_________________(填“化学”或“物理”)变化。
(3)乙烯转化为乙醇的反应类型是__________________。
(4)乙醇转化为A的化学方程式是____________________________________________。
(5)工业上乙烯通过聚合反应可得到高分子化合物B,反应的化学方程式是_____________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组在实验室利用质子酸甲醇燃料电池作电源,电解硫酸铜溶液。

请回答下列问题:
(1)通入氧气的电极为______(填“正极”或“负极”),通入甲醇一极的电极反应式为_________。
(2)b电极上的现象为________________。
(3)假设硫酸铜溶液的体积为600 mL(电解前后溶液的体积变化忽略不计),若消耗336 mL(标准状况)O2,则电解后硫酸铜溶液的pH为________。
(4)若a、b均换成铜电极,则电解一段时间后硫酸铜溶液的浓度________(填“增大”“减小”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国规定食盐的含碘量(按每千克食盐含碘元素计)为20mgkg﹣1~40mgkg﹣1 , 则每千克食盐加入碘酸钾(KIO3)的物质的量应不少于 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿魏酸乙酯是生产用于治疗心脑血管疾病及白细胞减少等症药品的基本原料,如心血康、利脉胶囊、太太口服液等。现根据如下流程合成阿魏酸乙酯:
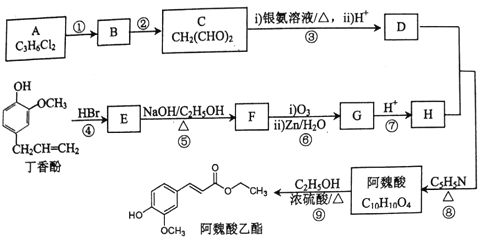
已知:
① E中有两个甲基,F中没有亚甲基(一CH2一)
②![]()
③![]()
回答下列问题:
(1)反应①的条件为______;反应⑨的类型为________;A的名称为_____(系统命名法)。
(2)由C生成D的过程中,步骤i)的化学方程式为:_________。
(3) B和D反应生成的某种有机物核磁共振氢谱显示有3 组吸收峰,该反应的化学方程式
为:__________
(4)G的分子式为_____。
(5)有同学提出:可用酸性高锰酸钾溶液检测反应⑧中是否有阿魏酸生成,该说法是否
正确____ (填“是”或“否”)理由是________。
(6)H 有多种同分异构体,写出同时符合下列要求的所有H 的同分异构体结构简式____。
① 既能发生银镜反应,又能与FeCl3溶液发生显色反应;② 苯环上的一氯代物只有一种。
(7)参照上述流程,请写出由环戊烯(![]() )制备l,9-壬二酸[HOOC(CH2)7COOH]的合成路线流程图(其他原料任选)___________。
)制备l,9-壬二酸[HOOC(CH2)7COOH]的合成路线流程图(其他原料任选)___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学——选修3:物质结构与性质]
黄铜专指铜锌合金,始于明代《明会典》,古代黄铜主要用于铸币和铸造雕塑。回答下列问题:
(1)Zn元素在周期表中的位置为_____________,基态Zn2+外围电子排布式为_____________。
(2)硝酸铜溶液可与乙二胺(![]() )形成配位化合物[Cu(en)2](NO3)2(“en”表示乙二胺)。
)形成配位化合物[Cu(en)2](NO3)2(“en”表示乙二胺)。
①NO3-的空间构型为_____________。
②Cu2+与乙二胺分子之间存在的化学键类型为______________,在乙二胺分子中提供孤电子对的原子是_____________。
③在乙二胺分子中C的杂化轨道类型是_____________。
④乙二胺的沸点116℃,而相对分子质量比乙二胺大1的三甲胺(![]() )的沸点只有2.87℃,其原因是___________________________________。
)的沸点只有2.87℃,其原因是___________________________________。
(3)铜的晶胞实物堆积模型如图所示,设铜的密度为ρg·cm-3。

①铜的晶体堆积方式为_____________。
②铜晶胞参数a=_____________cm(列出式子即可,设铜的摩尔质量为Mg·mol-1,阿伏伽德罗常数值为NA)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com