
����Ŀ���ɶ�����Ԫ����ɵ���ѧ��������A��B��C��D��E��X������ͼת����ϵ������������ͷ�Ӧ������ȥ����X��һ������̼Ԫ�ء�

��1����AΪ�������ʣ�B����ɫ��ӦΪ��ɫ����д��A��ˮ��Ӧ�����ӷ���ʽ_____��B��D��Ӧ�����ӷ���ʽ_______________________________��
��2����AΪ�ǽ������ʣ�A��ˮ��Ӧʱ��H2O�Ȳ���������Ҳ���ǻ�ԭ������E�ĽṹʽΪ__________��д��B��D��Ӧ�����ӷ���ʽ_________________________��
��3����AΪ�����EΪ���ӻ������д��E�ĵ���ʽ__________________��д��B��D��Ӧ�Ļ�ѧ����ʽ______________________________________��
���𰸡�2Na+2H2O��2Na++2OH-+H2��OH-+HCO3-��CO32-+H2OH-O-ClH++HCO3-��CO2��+H2O![]() 2CO+O2
2CO+O2![]() 2CO2
2CO2
��������
��1����AΪ�������ʣ�B����ɫ��ӦΪ��ɫ��˵��A���ƣ�B���������ƣ�E��������X�Ƕ�����̼��C��̼���ƣ�D��̼�����ƣ���A��ˮ��Ӧ�����ӷ���ʽΪ2Na+2H2O��2Na++2OH-+H2����B��D��Ӧ�����ӷ���ʽΪOH-+HCO3-��CO32-+H2O��
��2����AΪ�ǽ������ʣ�A��ˮ��Ӧʱ��H2O�Ȳ���������Ҳ���ǻ�ԭ������A��������B���Ȼ��⣬E�Ǵ����ᣬX��̼���ƣ�C�Ƕ�����̼��D��̼�����ƣ���E�ĽṹʽΪH-O-Cl��B��D��Ӧ�����ӷ���ʽΪH++HCO3-��CO2��+H2O��
��3����AΪ�����EΪ���ӻ������A�ǹ������ƣ�E���������ƣ�B��������X��̼��C�Ƕ�����̼��D��һ����̼����E�ĵ���ʽΪ![]() ��B��D��Ӧ�Ļ�ѧ����ʽΪ2CO+O2
��B��D��Ӧ�Ļ�ѧ����ʽΪ2CO+O2![]() 2CO2��
2CO2��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ʴ�йص�˵����ȷ����(����)

A. ͼa�������뺣ˮ�е�������Խ�����˸�ʴԽ����
B. ͼb����������M������Nʱ��Cu-Zn�Ͻ�ĸ�ʴ���ʼ�С
C. ͼc������ͨ����ʱZn��ʴ����������Zn�Ϸų����������Ҳ����
D. ͼd����Zn-MnO2�ɵ���Էŵ縯ʴ��Ҫ����MnO2���������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ף�P4S3���ǻ���ɫ��״���壬��ȼ���ж������ӽṹ֮һ��ͼ��ʾ����֪��ȼ��ʱP������ΪP4010�������й�P4S3��˵���в���ȷ����

A. P4S3���ڹ��ۻ�����
B. 1mol P4S3�����к���9mol���ۼ�
C. P4S3���ȼ�յĻ�ѧ����ʽΪP4S3+8O2=P4O10+3SO2
D. P4S3����Ԫ��Ϊ+3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��EΪ������Ԫ�أ���ԭ��������������������֮��Ϊ39��B��Cͬ���ڣ�A��Dͬ���壬A��C���������γ�����Һ̬������A2C��A2C2��EԪ�ص�������������������ȡ����û�ѧ����ش��������⣺
��1��EԪ�������ڱ��е�λ��Ϊ____________����д��E����������Ӧˮ����ĵ��뷽��ʽ��_________________________________��
��2��C��D��E����Ԫ�ض�Ӧ�����Ӱ뾶�Ӵ�С��˳��Ϊ(�����ӷ��ű�ʾ)_____>_____>_____����A��B��C����Ԫ����ɵ�18�������ķ���ʽΪ______________________��
��3���õ���ʽ��ʾBC2���γɹ��̣�_________________________________��
��4��ԭ��������CС1��Ԫ��F��Ҳ����A�γ�18���ӵķ��ӣ���֪1 mol�÷�����һ�������¿��Ի�ԭ4 mol����ͭ��ͬʱ����һ������Ⱦ�����嵥�ʺͺ�ɫ���廹��ˮ����д����ѧ����ʽ_____________��
��5����ӡˢ��·���Ϻ���ͭ�������Ļ��շ����ǽ�������ʹͭת��Ϊ����ͭ�����������ܽ⡣�ָ���A2C2��ϡ������ݷ�ӡˢ��·��ȴﵽ����Ŀ�ģ��ֱ����˻�������д����Ӧ�����ӷ���ʽ��___________��
��6��Ԫ��D�ĵ�����һ�������£�����A���ʻ�������һ�ֻ�����DA�� DA����ˮ��Ӧ�ų�����������1 mol DA��1 mol E���ʻ�ϼ���������ˮ����ַ�Ӧ�����ɵ������ڱ�״���µ������_________L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й�ͬ���칹����Ŀ�������У���ȷ����
A. C3H8O��2��ͬ���칹��
B. C8H10��ֻ��3�����ڷ�������ͬ���칹��
C. �ױ������ϵ�һ����ԭ�ӱ���3��̼ԭ�ӵ����ȡ�������ò�����6��
D. CH3CH2CH2CH3��������������Ӧ��ֻ����1��һ�ȴ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�л���Ľṹ��ʽ��ͼ��ʾ�������й��������ʵ������У���ȷ����
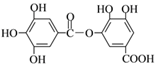
A. �������ԣ�1 mol���л�������ˮ��Ӧ�����������4 mol Br2
B. ���ܷ���ˮ�ⷴӦ��ˮ������������ֲ���
C. ��Ni���£�1 mol�����ʿ��Ժ�7 mol H2�����ӳɷ�Ӧ
D. ��һ�������£�1 mol�������������6 mol NaOH��ȫ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij100mL��Һ���ܺ���Na+��NH4+��Fe3+��CO32����SO42����Cl���е������֣�ȡ����Һ��������ʵ�飬ʵ�������ͼ���������Լ�������������ȫ���ݳ�������˵������ȷ���ǣ�������

A. ԭ��Һһ������CO32����SO42����һ��������Fe3+
B. ԭ��Һһ������Cl�������ܴ���Na+
C. ԭ��Һ��c��Cl������0.1molL��1
D. ��ԭ��Һ�в�����Na+����c��Cl������0.1molL��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ��a��b��c��d��e ��ԭ���������������������γɵĻ�����X��Y��Z��W ��һ�������µ��ת����ϵ��ͼ��ʾ����֪X��Y��Z������dԪ�أ�X����ɫ��Ӧ�ʻ�ɫ��Y�������������0.1mol��L-1W��Һ��pHΪ1������˵����ȷ����

A. eԪ�صĺ������������ͬ��������ǿ
B. bԪ�صĵ��ʺ��⻯����ܾ��������Ժ�Ư����
C. c��e��a��eԪ���γɵĻ���������ڵ�����һ�ѧ��������ͬ
D. b��c��dԪ�ص����Ӱ뾶��С˳���� c��d��b
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������Ϊһ����Ҫ�����м��壬��ϳɷ������£�

��1��������III�ķ���ʽΪ_______________
��2��д��������I��NaOH����Һ�з�Ӧ�Ļ�ѧ����ʽ��ע��:�������ɻ�Ϊͬ���칹��������л��д������һ����Ϊ�����T�ɣ�____________________________________________
��3��д��������������Ƶ�������ͭ��Ӧ�Ļ�ѧ����ʽ___________________________��
��4��������IV��Ũ������·�Ӧ������Ԫ��״������д�������ʵĽṹ��ʽ_________��
��5���������������ת����ϵ����������������Ƴ�![]() ��2-��-1,3-����ϩ���������Ƣٵķ�Ӧ���õ��л���VI��VII���ṹ��ʽ�ֱ���Ϊ_______��_______���������ʵ���֮����_________��
��2-��-1,3-����ϩ���������Ƣٵķ�Ӧ���õ��л���VI��VII���ṹ��ʽ�ֱ���Ϊ_______��_______���������ʵ���֮����_________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com