
����Ŀ������(�Ҷ���)������ԭ���ͳ����������ڽ������⡢֯��Ư��ϡ��������һ���Ʊ�����(��2���ᾧˮ)�Ĺ����������ң�

�ش��������⣺
��1��CO��NaOH��һ�������ºϳɼ����ơ������Ƽ�������Ļ�ѧ��Ӧ����ʽ�ֱ�Ϊ��__________________��_______________��
��2�����Ʊ������������ι��˲��������˲���������Һ��___________��������________�����˲���������Һ��____________��____________��������_______��
��3�����չ�������������Ŀ����______________��
��4�����˽�������������ֱ���������ữ�Ʊ����ᡣ�÷�����ȱ���Dz�Ʒ���������к��е�������Ҫ��____________________��
��5���ᾧˮ�ϲ����Ʒ�Ĵ����ø�����ط��ⶨ��
���������Ʒ0.250 g����ˮ����0.0500 mol��L-1������KMnO4��Һ�ζ�����dz�ۺ�ɫ�����ʣ�����KMnO4��Һ15.00 mL����Ӧ�����ӷ���ʽΪ__________________��
��ʽ����ó�Ʒ�Ĵ���____________________________��
���𰸡�CO��NaOH![]() HCOONa 2HCOONa
HCOONa 2HCOONa![]() Na2C2O4��H2�� NaOH��Һ CaC2O4 H2C2O4��Һ H2SO4��Һ CaSO4 �ֱ�ѭ�������������ƺ�����(���ͳɱ�)����С��Ⱦ Na2SO4 5C2O42��+2MnO4��+16H��==2Mn2��+8H2O+10CO2��
Na2C2O4��H2�� NaOH��Һ CaC2O4 H2C2O4��Һ H2SO4��Һ CaSO4 �ֱ�ѭ�������������ƺ�����(���ͳɱ�)����С��Ⱦ Na2SO4 5C2O42��+2MnO4��+16H��==2Mn2��+8H2O+10CO2�� 
��������
��������ͼ֪��һ�������£�һ����̼���������Ʒ�Ӧ���ɼ����ƣ���Ӧ����ʽΪ��CO��NaOH![]() HCOONa�����������£��������������ɲ����ƣ���ԭ���غ��֪���������ɣ���Ӧ����ʽΪ2HCOONa
HCOONa�����������£��������������ɲ����ƣ���ԭ���غ��֪���������ɣ���Ӧ����ʽΪ2HCOONa![]() Na2C2O4��H2�������������������Ʒ�Ӧ�õ���������������ƣ���Һ��NaOH��Һ��Ũ����ѭ�����ã�����ΪCa C2O4������������ᷴӦ�õ������������ƣ�������ΪCaSO4����ҺBΪ��������Һ���پ����ᾧ������õ������ƾ��壬ĸҺ�к�������Ͳ��ᣬ��ѭ�����á�
Na2C2O4��H2�������������������Ʒ�Ӧ�õ���������������ƣ���Һ��NaOH��Һ��Ũ����ѭ�����ã�����ΪCa C2O4������������ᷴӦ�õ������������ƣ�������ΪCaSO4����ҺBΪ��������Һ���پ����ᾧ������õ������ƾ��壬ĸҺ�к�������Ͳ��ᣬ��ѭ�����á�
��1�����ݹ�������ͼ��֪��CO��NaOH��һ�������ºϳɼ����Ʒ���ʽΪCO��NaOH![]() HCOONa�������Ƽ��������ͬʱ���в��������ɣ���˷�Ӧ�Ļ�ѧ��Ӧ����ʽΪ2HCOONa
HCOONa�������Ƽ��������ͬʱ���в��������ɣ���˷�Ӧ�Ļ�ѧ��Ӧ����ʽΪ2HCOONa![]() Na2C2O4��H2����
Na2C2O4��H2����
��2�����ݷ�Ӧԭ�����ܽ����Լ�ʾ��ͼ��֪�����˲���������Һ��NaOH��Һ��������CaC2O4�����˲���������Һ��H2C2O4��Һ��H2SO4��Һ��������CaSO4��
��3�����ݹ��չ��̿�֪������������ѭ�������������ƣ�����������ѭ���������ᣬ�������ԭ�ϵ������ʣ��ֽ����˳ɱ�����С��Ⱦ��
��4�������������IJ���Ϊ�����ƣ�ֱ���������ữ�����ɲ���������ƣ����к��е�������Ҫ��Na2SO4��
��5���ڲⶨ�����У��������Ϊ������������Ϊ��ԭ������Ӧ�����ӷ���ʽ5C2O42- + 2MnO4- + 16H+= 2Mn2++ 8H2O + 10CO2�������ݷ���ʽ�ɵù�ϵʽ��
5H2C2O4��2H2O ~ 2KMnO4
5 2
n 0.05mol/L��15.0��10-3L
���n��H2C2O4��2H2O��=1.875��10-3mol
��m��H2C2O4��2H2O��=1.875��10-3mol��126g/mol=0.236g
���Գ�Ʒ�Ĵ�����=![]() ��100%=94.5%��
��100%=94.5%��


 Ӣ��СӢ������Ĭдϵ�д�
Ӣ��СӢ������Ĭдϵ�д� �����ҵ���������ͯ������ϵ�д�
�����ҵ���������ͯ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������Ի�����Ϊԭ���Ʊ������ϩ�ĺϳ�·�ߣ�����˵����ȷ����( )
![]()
A. ![]() �Ľṹ��ʽΪ
�Ľṹ��ʽΪ![]()
B. ��Ӧ�ܵķ�Ӧ�Լ��ͷ�Ӧ������Ũ![]() ����
����
C. �٢ڢ۵ķ�Ӧ���ͷֱ�Ϊ±����ˮ�⡢��ȥ
D. �����ϩ��![]() ��1��1�����ʵ���֮�ȼӳɿ�����
��1��1�����ʵ���֮�ȼӳɿ�����![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ŧ�۵�����ִ��������й㷺Ӧ�ã���һ����п��أ���缫�ֱ���Ag2O��Zn���������ҺΪKOH��Һ���ܷ�ӦΪAg2O+Zn=ZnO+2Ag������һ���缫��ӦΪAg2O+H2O+2e-=2Ag+2OH-��

��1����������Ϊ___________��
��2��д����һ�缫�ĵ缫��Ӧʽ__________��
��3���ڵ��ʹ�õĹ����У��������Һ��KOH�����ʵ��������仯��________������С�����䣩��
��4������ع���ʱͨ����·�����ṩ��1mol���ӣ��������ĵĸ���������_______��
��5���������з�Ӧ��Fe+2Fe3+=3Fe2+���һ��ԭ��أ���ѡ���ʵ��IJ��Ϻ��Լ���
�ٵ������ҺΪ_____________��
�ڸ�����Ӧʽ��____________________��
����Һ��Fe3+��__________���ƶ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ԭ��Ӧ�������������о��й㷺����;���ᴩ�Ž�
��1�����������������е�������û�з���������ԭ��Ӧ����____(��д��ĸ����)
��2��ˮ���������Ҫ��ɲ��֣��������к�������һ�����ʡ��������ֻ�����Ӧ������������ԭ��Ӧ�Ĺ�ϵ��������ͼ���
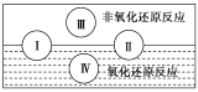
��д����ˮ�μӵķ��Ϸ�Ӧ���͢���һ����ѧ����ʽ��_____������ˮΪ______����
��3��������������˫��ˮ��ҽ������������ɱ��������������ϴ�˿ڡ�H2O2��ʱ����Ϊ��ҵ��Һ��������������ɫ�������������ƣ��������ɿ�ҵ��Һ�е��軯��(��KCN)�������·�Ӧʵ�֣�KCN��H2O2��H2O=A��NH3������ָ��������A�Ļ�ѧʽΪ___��������H2O2����Ϊ��ɫ��������������_______��
��4���Ȼ�麟��������ӡ��磺�ں���ͭ��ʱ���Ȼ�麟�ȥͭ�����������ͭ�Ա㺸�ӣ��䷴ӦΪ��____CuO��___NH4Cl![]() ____Cu��___CuCl2��___N2����___H2O��
____Cu��___CuCl2��___N2����___H2O��
����ƽ��������ԭ��Ӧ����ʽ��
�ڸ÷�Ӧ�У���������Ԫ����______(��Ԫ������)����������____(�ѧʽ)��
�۷�Ӧ��������0.2mol�����壬����_____mol�ĵ���ת�ơ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧ��ȤС����ʵ���ҴӺ���������ȡ�Ⲣ�Ʊ�KI���塣��ش���������
(1)��ˮ��Һ����ȡ�����ѡ�õ��Լ���____________��(�����)
A���ƾ� B��CCl4 C����ϩ D��ֱ������
(2)KI������Ʊ���ʵ��װ����ͼ��

ʵ�鲽������
i������0.5mol��L1��KOH��Һ��
i��������ƿ�м���12.7g����I2��250mL 0.5mol��L1��KOH��Һ������������ȫ�ܽ⡣
����ͨ����Һ©����Ӧ�����Һ�еμ��������ᣬ��ַ�Ӧ��HCOOH������ΪCO2������KOH��Һ��pH��9~10����������Һ����Ũ������ȴ�ᾧ�����ˡ�ϴ�ӡ������KI��Ʒ8.3g����ش��������⣺
������0.5mol��L1 KOH��Һʱ�����в���������õ���ҺŨ��ƫ�ߵ���_____(�����)��
A�������Ϸֱ����������ȵ�ֽƬ�����KOH����
B��KOH������Ʒ�л���K2O2
C�������õĹ�������ձ����ܽ�δ����ȴֱ��ת��������ƿ
D��δϴ���ձ���������ֱ��������ƿ�м�ˮ����
E������ʱ���ӿ̶���
�ڲ��袢��I2��KOH��Һ��Ӧ���ɵ���������ͻ�ԭ��������ʵ���֮��Ϊ1��5����д����������Ļ�ѧʽ��____________��
�۲��袣������Һ�еμ���������ʱ�������___________��(�a����b����a��b��)
��ʵ���У�����HCOOH����������ԭ��Ӧ�����ӷ���ʽΪ____________________��
��ʵ����KI�IJ���Ϊ________________%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڳ��������еĻ�ѧ��Ӧ��Zn(s)+H2SO4(aq)=ZnSO4(aq)+H2(g)�����������в���ȷ����(����)

A. Zn��H2SO4������������ZnSO4��H2��������
B. ��Ӧ������������ϵ������ͼ��ʾ
C. �����÷�Ӧ��Ƴ�ԭ��أ���ZnΪ����
D. �����÷�Ӧ��Ƴ�ԭ��أ�����32.5gп�ܽ�ʱ�����ų�22.4 L����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����淴ӦmA(g)��nB(s)![]() pC(g)��qD(g)���ڷ�Ӧ�����У���������������ʱ��D�İٷֺ������¶�(T)��ѹǿ(P)�Ĺ�ϵ��ͼ��ʾ���ж����������в���ȷ������
pC(g)��qD(g)���ڷ�Ӧ�����У���������������ʱ��D�İٷֺ������¶�(T)��ѹǿ(P)�Ĺ�ϵ��ͼ��ʾ���ж����������в���ȷ������
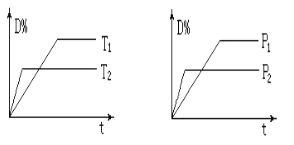
A. �ﵽƽ��������¶ȣ�ƽ�����淴Ӧ�����ƶ�
B. �ﵽƽ�����ʹ�ô�����D�����ʵ�����������
C. ��ѧ����ʽ��һ����m��p��q
D. ƽ�������B������������ƽ��������Ӧ�����ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪25��ʱ����(H2C2O4)�ĵ��볣��ΪK1=5.0��10-2��K2=5.4��10-5������Ƶ�Ksp=4.0��10-8��̼��Ƶ�Ksp=2.5��10-9����ͬ�¶���ˮ�����ӻ��������±���
t/�� | 0 | 10 | 20 | 25 | 40 | 50 | 90 | 100 |
Kw/10-14 | 0.134 | 0.292 | 0.681 | 1.00 | 2.92 | 5.57 | 38.0 | 55.0 |
(1)�����½�0.2 mol/L��KOH��Һ20 mL��0.2 mol/L�IJ�����Һ20 mL��Ϻ���Һ�����ԣ����Ϻ���Һ�и�����Ũ�ȵĴ�С˳��Ϊ__________________________________��
(2)��֪������ʹ���Ը��������Һ(ϡ�����ữ)��ɫ��������ƿ�з���20.00mLδ֪Ũ�ȵIJ��ᣬ��0.1mol/L���������Һ�ζ���������ζ��յ�ʱ����������VmL���������Һ�����������ʵ���Ũ��Ϊ__________mol/L��
(3)90��ʱ����0.005 mol/L������������Һ20 mL��0.0012 mol/L�IJ�����Һ20 mL��ϣ���Ϻ���Һ��pH=___________��
(4)25��ʱ����20 mL����Ƶı�����Һ����μ���8.0��10-4 mol/L��̼�����Һ10 mL���ܷ����������___________(����������������)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ҹ�������Ա���Ƴ�һ������Na-CO2��ء��õ������CO2�Ĺ���ԭ����ͼ��ʾ�����յ�ȫ��CO2�У���![]() ת��ΪNa2CO3��������ڶ��̼����(MWCNT)�缫���档����˵������ȷ����
ת��ΪNa2CO3��������ڶ��̼����(MWCNT)�缫���档����˵������ȷ����
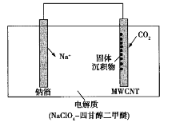
A. �Ʋ�Ϊ����������������Ӧ
B. ÿ����22.4 LCO2��ת�Ƶ�����Ϊ![]() mol
mol
C. ������Ӧʽ��4Na++3CO2+4e-=2Na2CO3+C
D. Na+ͨ�����������MWCNT��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com