
【题目】某温度下,在2L密闭容器中投入一定量的A、B发生反应:3A(g)+bB(g)![]() cC(g) △H= -Q kJmol-1(Q>0),12s 时达到平衡,生成C的物质的量为0.8mol,反应过程如图所示。试计算:
cC(g) △H= -Q kJmol-1(Q>0),12s 时达到平衡,生成C的物质的量为0.8mol,反应过程如图所示。试计算:
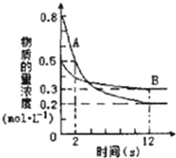
(1)前12s内,A的平均反应速率为______________。
(2)化学计量数之比b:c=______________。
(3)12s内,A和B反应放出的热量为__________(用Q表示)。
【答案】0.05mol/(L·s) 1:2 0.4Q kJ
【解析】
(1)据图象分析可以知道A的浓度变化量,根据v=c/t计算出A的平均反应速率;
(2)根据速率之比和系数成正比,计算出B、C物质的反应速率,进而计算出化学计量数之比b:c的数值;
(3)12s内,反应3molA放热QkJ,反应A的物质的量=(0.8mol/L-0.2mol/L)×2L=1.2mol,结合化学方程式定量关系计算分析。
(1)某温度下,在2L密闭容器中投入一定量的A、B发生反应: 3A(g)+bB(g)![]() cC(g) △H= -Q kJmol-1(Q>0), 12s时达到平衡,生成C的物质的量为0.8mol ,据图象分析可以知道A的浓度变化=0.8mol/L-0.2mol/L=0.6mol/L,反应速率v=c/t=0.6mol/L÷12s= 0.05mol/(L·s) ;
cC(g) △H= -Q kJmol-1(Q>0), 12s时达到平衡,生成C的物质的量为0.8mol ,据图象分析可以知道A的浓度变化=0.8mol/L-0.2mol/L=0.6mol/L,反应速率v=c/t=0.6mol/L÷12s= 0.05mol/(L·s) ;
答案是:0.05mol/(L·s);
(2)图象分析B的浓度变化=0.5mol/L-0.3mol/L=0.2mol/L,计算B的反应速率=0.2mol/L÷12s= 1/60 mol/(L·s),速率之比等于化学方程式计量数之比,3:b=0.05: 1/60,b=1,3:c=0.05:0.8mol/(2L×12s),c=2;化学计量数之比b:c=1:2;
故答案是:1:2;
(3)12s内,反应3molA放热QkJ,反应A的物质的量=(0.8mol/L-0.2mol/L)×2L=1.2mol,结合化学方程式定量关系计算:3A(g)+bB(g)![]() cC(g) △H= -Q kJmol-1(Q>0),1.2molA反应放出热量0.4QkJ;
cC(g) △H= -Q kJmol-1(Q>0),1.2molA反应放出热量0.4QkJ;
故答案是:0.4Q kJ。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】按如图所示装置进行实验,填写有关现象及化学方程式。
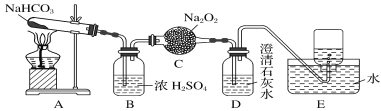
(1) D装置的作用是________,E中收集的气体是___________ (填名称)。
(2) 浓硫酸的作用是 _____________。
(3) A中发生反应的化学方程式为____________。
(4) C中发生反应的化学方程式为_________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】信息时代产生的大量电子垃圾对环境构成了极大的威胁。某“变废为宝”学生探究小组将一批废弃的线路板简单处理后,得到含70%Cu,25%Al、4%Fe及少量Au、Pt等金属的混合物,并设计出如下制备硫酸铜和硫酸铝晶体的路线:(友情提示:要将溶液中的![]() 、
、![]() 、
、![]() 、
、![]() 沉淀为氢氧化物,需溶液的pH分别为:6.4、6.4、3.7、4.7)
沉淀为氢氧化物,需溶液的pH分别为:6.4、6.4、3.7、4.7)
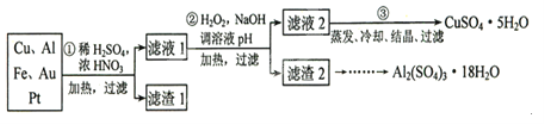
请回答下列问题:
(1)如何检验滤液1中是否含有![]() ?_______________;得到滤渣1的主要成分为____________。
?_______________;得到滤渣1的主要成分为____________。
(2)第2步加![]() 的作用是____________,使用
的作用是____________,使用![]() 的优点是____________;调溶液pH的目的是使____________生成沉淀。
的优点是____________;调溶液pH的目的是使____________生成沉淀。
(3)用第③步所得![]() 制备无水
制备无水![]() 的方法是____________。
的方法是____________。
(4)由滤渣2制取![]() ,探究小组设计了三种方案:
,探究小组设计了三种方案:
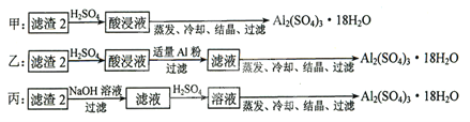
上述三种方案中,______方案不可行,原因是_________;从原子利用率角度考虑,______方案更合理。
(5)结晶水的测定:将坩埚洗净,烘干至恒重,记录质量;在坩埚中加入研细的三草酸合铁酸钾晶体,称量并记录质量;加热至250℃,恒温一段时间,置于空气中冷却,称量并记录质量;计算结晶水含量。请纠正实验过程中的两处错误:______________、______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】德国化学家凯库勒认为苯分子的结构中,碳碳间以单、双键交替结合而成环状。为了评价凯库勒的观点,某学生设计了以下实验方案:
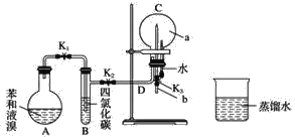
实验操作:
①按如图所示的装置图连接好各仪器;
②检验装置的气密性;
③在A中加入适量的苯和液溴的混合液体,再加入少量铁粉,塞上橡皮塞,打开K1、K2止水夹,关闭K3止水夹;
④待烧瓶C中气体收集满后,将导管b的下端插入烧杯里的水中,关闭K2,打开K3,挤压预先装有水的胶头滴管的胶头,观察实验现象。
请回答下列问题:
(1)能证明凯库勒观点错误的实验现象是_________。
(2)A中所发生的反应的反应类型为__________。
(3)A中发生反应的化学方程式__________。
(4)装置B的作用是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在常温下的一密闭容器中事先放入1.56g过氧化钠,然后再通入乙烷与氧气的混合气体,用电火花引爆,直至反应完全为止,恢复到原温度,容器内压强近似为零。
(1)相同条件下,通入的气体氧气和乙烷的体积比是多少?_____
(2)通入氧气的质量最大应是多少?_____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“84”消毒液(主要成分为![]() )广泛应用于杀菌消毒。某化学学习小组用甲烷燃料电池电解饱和食盐水制备“84”消毒液,装置如图所示,
)广泛应用于杀菌消毒。某化学学习小组用甲烷燃料电池电解饱和食盐水制备“84”消毒液,装置如图所示,![]() ,
,![]() ,
,![]() ,
,![]() 均为惰性电极,下列说法正确的是( )
均为惰性电极,下列说法正确的是( )
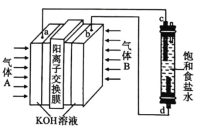
A.气体B为甲烷
B.电解装置中的总反应为NaCl+H2O![]() NaClO+H2↑
NaClO+H2↑
C.消耗2.24L(标准状况)甲烷,K+通过交换膜向左室移动0.8mol
D.甲烷发生的电极反应方程式为CH4-8e-+8OH—=CO2↑+6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)2019年诺贝尔化学奖颁给了三位在锂电池领域做出突出贡献的科学家。
①基态锂原子核外有________种不同空间运动状态的电子。
②![]() 状态的锂到
状态的锂到![]() 状态的锂所得的原子光谱是________光谱。
状态的锂所得的原子光谱是________光谱。
③锂和铍相比,锂的第Ⅱ电离能________(填“>”“<”或“=”)铍的第Ⅱ电离能。
(2)某锂离子电池的正极材料为![]() 。
。
①基态![]() 原子价层电子的电子排布图(轨道表达式)是________。
原子价层电子的电子排布图(轨道表达式)是________。
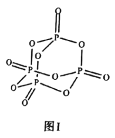
②磷元素是生物体不可缺少的元素之一,把一种填有![]() 的苏打石灰玻璃移植到体内,钙离子和磷酸根离子在玻璃和骨头的间隙中溶出,有助于诱导新的骨骼生成。
的苏打石灰玻璃移植到体内,钙离子和磷酸根离子在玻璃和骨头的间隙中溶出,有助于诱导新的骨骼生成。![]() 的结构如图I所示,其中
的结构如图I所示,其中![]() 原子的杂化方式是________,
原子的杂化方式是________,![]() 是________(填“极性”或“非极性”)分子。
是________(填“极性”或“非极性”)分子。
③![]() 原子形成的含氧酸有很多种结构,图Ⅱ是某种多聚磷酸根的结构示意图。这种多聚磷酸的化学式为________(用
原子形成的含氧酸有很多种结构,图Ⅱ是某种多聚磷酸根的结构示意图。这种多聚磷酸的化学式为________(用![]() 表示磷原子的个数)。
表示磷原子的个数)。

(3)某锂电池负极材料晶体中![]() 嵌入两层石墨层中导致石墨堆积方式发生改变,形成如图Ⅲ所示的晶体结构。
嵌入两层石墨层中导致石墨堆积方式发生改变,形成如图Ⅲ所示的晶体结构。
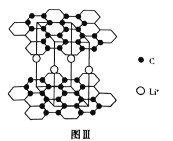
①石墨是一种导体,但石墨的导电性只能沿石墨平面的方向,原因是________。
②已知最近碳一碳原子间的距离是![]() ,则最近锂一锂离子间的距离是________
,则最近锂一锂离子间的距离是________![]() ;石墨层之间的距离是
;石墨层之间的距离是![]() (其中
(其中![]() ),
),![]() 表示阿伏加德罗常数的值,该晶体的密度是________
表示阿伏加德罗常数的值,该晶体的密度是________![]() (列出计算式即可)。
(列出计算式即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一处于平衡状态的反应X(g) +3Y(g)![]() 2Z(g) (正反应是放热反应) 。为了使平衡向生成Z的方向移动, 应选择的条件是
2Z(g) (正反应是放热反应) 。为了使平衡向生成Z的方向移动, 应选择的条件是
①升高温度 ②降低温度 ③增大压强 ④降低压强 ⑤加入正催化剂 ⑥分离出Z
A. ①③⑤ B. ②③⑤ C. ②③⑥ D. ②④⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Zn3(PO4)2·2H2O(溶于酸,难溶于水)是一种无毒害作用的防锈颜料,利用锌浮渣(主要含Zn、ZnO、ZnCl2,还含少量的铁、锰、铜、铅及砷的化合物等)制取Zn3(PO4)2·2H2O的工艺流程如图:
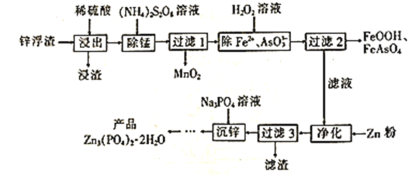
回答下列问题:
(1)“浸出”时,下列措施能提高锌的浸取率的是__(填字母)。
A.用浓硫酸代替稀硫酸 B.适当升高浸取液的温度
C.将“浸渣”再次浸取 D.缩短“浸出”时间
(2)“除锰”时,Mn2+发生反应的离子方程式为__(S2O![]() 被还原为SO
被还原为SO![]() )。
)。
(3)流程中除铁、砷时,当生成8.9gFeOOH和7.8gFeAsO4时,消耗H2O2__mol。
(4)“净化”时加锌粉的目的是__。
(5)“沉锌”时发生反应的化学方程式为__。
(6)“沉锌”至得到“产品”还需要经过的操作是__、洗涤、__。证明产品已洗涤干净的实验方法是__。
(7)Meyer等认为磷酸锌防腐机理是在钢铁表面形成组成近似为Zn2Fe(PO4)2·4H2O的覆盖膜,则在形成该覆盖膜的过程中,负极的电极反应式为__。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com